Оспа обезьян (Monkepox)
Исторические сведения. Заболевания обезьян с появлением у них везикулезной сыпи известны с XVIII в., позднее была установлена связь между спорадическими осповидными заболеваниями человека и обезьян. Вирусологически подтвержденный случай оспы обезьян у человека описан отечественным ученым И.Д.Ладным в Заире.
Этиология. Возбудитель относится к семейству Poxviridae, роду Оrthomyxvirus, по морфологическим, антигенным и культуральным свойствам близкий к вирусу натуральной оспы.
Эпидемиология. Естественный резервуар вируса не установлен. Механизм заражения – аэрогенный с воздушно-капельным путем передачи возбудителя. Наибольшая восприимчивость наблюдается в возрасте до 4 лет. Инфицированный вирусом человек может быть источником инфекции, однако в отличие от натуральной оспы заразившиеся от него лица для окружающих людей эпидемиологически неопасны. В настоящее время болезнь встречается в Заире, Либерии, Камеруне, Нигерии, Кот-д'Ивуаре, Сьерра-Леоне (всего зарегистрировано около 100 случаев болезни).
Патогенез и патологоанатомическая картина. Изучены недостаточно ввиду небольшого числа наблюдений. В общих чертах патогенез заболевания сходен с таковым при натуральной оспе.
Клиническая картина. Клинические проявления оспы обезьян напоминают симптоматику натуральной оспы и могут колебаться от стертых и легких до тяжелых, прогностически неблагоприятных форм болезни.
Начало болезни острое: наблюдаются озноб и быстрое повышение температуры тела до 39—40 °С, астенизация, понижение аппетита, миалгии и артралгии. С 3—4-го дня болезни на фоне температурной ремиссии на коже и слизистых оболочках, вначале на лице, руках, а затем на туловище появляется сыпь, развивающаяся стадийно от макулы до везикулы, пустулы, корочки и рубца. Характерна центробежная локализация элементов, их мономорфность. На слизистых оболочках везикулы быстро мацерируются с образованием болезненных язв. Пустулизация сыпи наблюдается на 7—8-й день болезни и характеризуется высокой лихорадкой и усилением других симптомов интоксикации. Образование корочек с 9—10-го дня сопровождается улучшением состояния больных и свидетельствует о начинающемся выздоровлении.
Прогноз в большинстве случаев благоприятный. Среди описанных случаев – 10 % с летальным исходом.
Диагностика и лечение. Такие же, как при натуральной оспе.
Профилактика. В эндемичных районах проводится плановая вакцинация и по эпидемиологическим показаниям. Контактные лица подлежат изоляции на 17 дней.
Оспа Таны
Вспышки болезни, наблюдавшиеся в 1957 и 1962 гг. в период наводнений реки Тана в Кении, описаны Дауни (1971). Заболевание протекало с 3—4-дневной лихорадкой, сильной головной болью, болями в поясничной области, выраженной астенией. В лихорадочный период возникали единичные осповидные с пупковидным втяжением элементы сыпи, расположенные преимущественно на открытых участках тела, на верхних конечностях, шее, туловище, обычно отсутствовавшие на кистях и стопах. Из элементов сыпи были изолированы вирусы, отнесенные к поксвирусам, однако они не нейтрализуются антителами к другим вирусам этой группы.
Случаи болезни протекали благоприятно.
Предполагается возможность передачи вируса от обезьян человеку при прямом контакте или через комаров Mansonia. Эпидемиологическая роль больного человека не установлена.
Сходные черты имеет белая оспа, встречающаяся в районах Западной Африки.
Легионеллезы
Син.: болезнь легионеров, питтсбургская пневмония, лихорадка Понтиак, лихорадка Форт-Брагг, легионелла-инфекция
Легионеллезы (legionellesis) – группа заболеваний бактериальной этиологии, клинически проявляющихся интоксикацией, респираторным синдромом, тяжелой пневмонией, поражением ЦНС и почек.
Исторические сведения. Открытие этиологии и описание клинической картины заболевания связаны с конгрессом организации «Американский легион», который проходил в Филадельфии в 1976 г. Из 4400 участников конгресса у 182 возникло острое респираторное заболевание с тяжелой пневмонией, 29 больных умерли. В 1977 г. Дж.Е.Макдейд и К.К.Шепард (США) выделили из легочной ткани человека, умершего во время вспышки болезни в Филадельфии, неизвестную ранее грамотрицательную палочку, этиологическая роль которой была доказана наличием специфических антител к микроорганизму.
Вспышка болезни легионеров во многом напоминала вспышки лихорадочных заболеваний в 1965 г. в Вашингтоне (округ Колумбия, США), в 1968 г. в городе Понтиак (Мичиган, США), в 1973 г. в курортном городе Бенидорм (Испания). Ретроспективное изучение сывороток больных, хранившихся в Центре борьбы с болезнями в городе Атланта (США), позволило доказать, что возбудителями этих вспышек были различные виды легионелл.
В 1978 г. на Международном симпозиуме по болезни легионеров возбудитель нового заболевания был назван Legionella pneumophilia.
В 1982 г., согласно рекомендациям ВОЗ, термин «болезнь легионеров» решено было сохранить лишь за эпидемическими заболеваниями, вызванными L. pneumophiliа, а заболевания, вызываемые другими видами легионелл, называть «легионелла-инфекция», или «легионелла-пневмония». Термин «легионеллез» объединяет все формы заболеваний, обусловленные микроорганизмами из семейства Legionellасеае.
Этиология. Возбудители легионеллеза относятся к семейству Legionellасеае, роду Legionella. Известно 8 видов легионелл. Наибольшее количество штаммов относится к виду L. pneumophilia. Легионелла – грамотрицательная, подвижная вследствие наличия жгутиков, палочка размером (2,0—3,0) х (0,5—0,7) мкм. Для культивирования возбудителя используют куриные эмбрионы и организм морской свинки. Фактором патогенности и вирулентности легионелл является термостабильный эндотоксин. Есть данные, подтверждающие наличие у бактерий сильнодействующего экзотоксина.
Легионеллы довольно устойчивы в водной среде: в речной воде они сохраняются до 3 нед, в водопроводной – более года, в дистиллированной – до 140 дней. Дезинфицирующие растворы (70 % раствор спирта, 5 % раствор йода, 1 % раствор формалина, 5 % раствор фенола, гипохлорид кальция и др.) быстро инактивируют возбудителя.
Эпидемиология. Предполагается, что легионеллез является сапронозной (или сапрозоонозной) инфекцией. Источники инфекции пока не установлены. Возбудитель способен размножаться во внешней среде, в воде различных водоемов, почве. Оптимальные места обитания легионелл – теплая вода открытых водоемов (25—30 °С).
Механизм передачи инфекции – аспирационный (аэрогенный). Основными факторами передачи являются воздух, вода (в виде водного аэрозоля) и почва (пыль).
Использование воды в системе кондиционера, душевых, сбрасываемой электростанциями и другими объектами, создает условия для накопления и передачи большой инфицирующей дозы возбудителя человеку.
Легионеллез нередко протекает как нозокомиальная инфекция, с чем связаны вспышки заболеваний в психиатрических больницах, центрах гемодиализа, отделениях реанимации, центрах по трансплантации почек и других специализированных клиниках.
Наиболее подвержены заболеванию легионеллезом лица пожилого возраста, курильщики, хронические алкоголики, наркоманы, а также лица с первичными и вторичными иммунодефицитами. Нередко болезнь возникает у людей, участвующих в земляных и строительных работах. Чаще болеют мужчины.
Максимальное число случаев болезни приходится на летне-осенние месяцы.
Вспышки заболеваний легионеллезом зарегистрированы в США, Великобритании, Испании, Италии, Франции. Спорадические случаи болезни выявлены во всех странах мира, в том числе и в России.
Болезнь выявляют повсеместно и более всего там, где есть условия и возможность для специфической лабораторной диагностики.
Патогенез и патологоанатомическая картина. Входные ворота инфекции – дыхательные пути. Легионеллы могут обнаруживаться в крови и, поступая в различные органы, вовлекать их в патологический процесс. Возбудитель, вызывая воспалительно-геморрагические и некробиотические изменения, гибнет, освобождая эндотоксин.
Эндотоксин вызывает системные поражения, а в тяжелых случаях – развитие инфекционно-токсического шока с острой полиорганной и прежде всего дыхательной и почечной недостаточностью, энцефалопатией, синдромом диссеминированного внутрисосудистого свертывания крови. Инфекционно-токсический шок может стать непосредственной причиной смерти больных.
При патологоанатомическом вскрытии выявляют очаговые и сливные участки консолидации легких, нередко с абсцессом, плевральным выпотом. Лобарные абсцедирующие пневмонии и фибринозный плеврит характерны для тяжелых форм легионеллеза. Методами импрегнации серебром и прямой иммунофлюоресценции показано присутствие легионелл в ткани легкого, медиастинальных лимфатических узлах, а также в селезенке, костном мозге, печени, почках. Гистоморфологическими исследованиями установлено наличие в органах лимфоплазмоцитарной инфильтрации. В печени обнаруживается лобулярный некроз.
Клиническая картина. Инкубационный период колеблется от 2 до 10 сут, чаще составляя 4—7 дней. Выделяют следующие клинические формы легионеллеза: 1) болезнь легионеров, протекающую с тяжелой пневмонией; 2) острое респираторное заболевание без пневмонии (лихорадка Понтиак); 3) острое лихорадочное заболевание с экзантемой (лихорадка Форт-Брагг).
Болезнь легионеров начинается остро с озноба, повышения температуры, головной боли, миалгий и артралгий. В тяжелых случаях наблюдаются нарушение походки, атаксия, затруднение речи, обмороки, галлюцинации. Со 2—4-го дня болезни присоединяются кашель со слизисто-гнойной или кровянистой мокротой, одышка, боли в груди. Перкуторно и аускультативно выявляются очаги притупления над легкими, влажные мелкопузырчатые хрипы, шум трения плевры. Пневмония может быть односторонней или двусторонней, чаще имеет долевой, реже очаговый характер. Обычно поражаются нижние доли легких, особенно правая. В тяжелых случаях наблюдаются абсцедирующая пневмония, экссудативный плеврит. Возможно течение болезни с картиной диффузного бронхиолита или альвеолита.
Язык сухой, обложен коричневым налетом. Живот мягкий, болезненный в эпигастральной области. При пальпации кишечника отмечаются болезненность и урчание. У 1 /3 больных с первых дней болезни возникает диарея, что может вызывать ошибки в диагностике. Печень и селезенка не увеличены.
При тяжелом течения легионеллеза нередко развивается инфекционно-токсический шок со смертельным исходом в первую неделю заболевания. При благоприятном течении болезни признаки интоксикации постепенно исчезают, воспалительные же очаги в легких рассасываются медленно в течение 4—6 нед и более. Летальность при этой форме достигает 20 %. Возможны легкое и средней тяжести течение болезни, которое не отличается от других бактериальных пневмоний.
Острое респираторное заболевание (лихорадка Понтиак) протекает без пневмонии с клинической картиной бронхита и ринита. И при этой форме легионеллеза наблюдаются мышечные боли, неврологические симптомы, рвота, жидкий стул. Летальных исходов не описано.
Острое лихорадочное заболевание с экзантемой (лихорадка Форт-Браг г) не имеет каких-либо характерных, специфических лишь для него проявлений. Экзантема может быть крупнопятнистой, кореподобной, петехиальной с различной локализацией. Шелушение кожи после исчезновения сыпи, как правило, не наблюдается. При этой форме возникают бронхит и общетоксические симптомы.
У больных легионеллезом отмечают нейтрофильный лейкоцитоз со сдвигом лейкоцитарной формулы крови влево, тромбоцитопению. В моче выявляются токсическая альбуминурия, цилиндры, лейкоциты, эритроциты. При биохимическом исследовании крови определяются повышение уровня активности аланинаминотрансферазы, содержания мочевины и креатинина, выявляется метаболический и дыхательный ацидоз.
Прогноз. Наиболее серьезный при болезни легионеров. Во время эпидемических вспышек летальность может достигать 20 %. Остальные формы легионеллеза протекают более благоприятно.
Диагностика. Клиническая диагностика легионеллеза сложна. Лишь при наличии эпидемиологических данных о групповых заболеваниях, чаще возникающих у лиц, отягощенных интеркуррентными заболеваниями, с иммунодефицитами различной природы, можно заподозрить эту инфекцию. Следует учитывать наличие свойственного легионеллезу симптомокомплекса: поражение дыхательных путей, нарушение функции ЦНС, печени, гематурия, диарея. Важно принимать во внимание при клинической диагностике отсутствие эффекта от лечения общепринятыми при пневмонии антибиотиками (тетрациклин, пенициллин, стрептомицин, цефалоспорины).
Лабораторная диагностика легионеллеза проводится путем выявления возбудителя иммунофлюоресцентным методом, получения культуры возбудителя и серологического анализа, направленного на обнаружение специфических антител. Наиболее перспективен метод прямой иммунофлюоресценции, позволяющий выявить возбудителя в мокроте, моче, плевральной жидкости, аутопсийном материале и объектах внешней среды. Быстрое определение бактерий в исследуемых субстратах с использованием метода флюоресцирующих антител может иметь решающее клиническое и эпидемиологическое значение, позволяя своевременно назначить этиотропную терапию.
Бактериологический метод, направленный на выделение культуры возбудителя, сложен и доступен лишь специализированным лабораториям. Для культивирования бактерий используется среда Мюллера – Хинтона.
Внедряются в практику иммуноферментные и радиоиммунные методы обнаружения растворимых антигенов легионелл с применением моноклональных антител. Этими методами выявляют антигены в крови, мокроте и моче.
Широкое применение нашел серологический метод диагностики легионеллеза (реакции микроагглютинации и непрямой иммунофлюоресценции). Антитела в сыворотке крови появляются с 6—7-го дня болезни, титр их нарастает на 2—3-й неделе заболевания. Диагностическим считается нарастание титра антител в 4 раза и более, а при однократном исследовании – высокий уровень содержания специфических антител (титры не менее 1:128).
Дифференциальная диагностика. Ее следует проводить с бактермальными пневмониями стафилококковой и пневмококковой этиологии, орнитозом, Ку-лихорадкой, микоплазмозом и другими заболеваниями, протекающими с поражением легких. Ведущее значение в этих случаях имеет лабораторная диагностика.
Лечение. Наиболее эффективным этиотропным средством является эритромицин. Препарат назначают перорально в суточной дозе 2 г в 4 приема. В тяжелых случаях, когда прием препарата внутрь малоэффективен или невозможен, прибегают к внутривенному введению растворимой формы – эритромицина фосфата по 0,2 г 3—4 раза в день. При улучшении состояния переходят на пероральный прием препарата. В случае очень тяжелых форм заболевания эритромицин рекомендуют вводить внутривенно в суточной дозе 2—4 г. Лечение эритромицином продолжают не менее 3 нед, так как при ранней отмене антибиотика возможны рецидивы.
Целесообразно дополнительно с эритромицином применять рифампицин в суточной дозе 0,6—1,2 г. Левомицетин может быть также использован в комплексной терапии легионеллеза в дозе 4 г в сутки парентерально в виде левомицетина сукцината. Наряду с этиотропной терапией используют комплекс патогенетических средств, направленных на коррекцию водноэлектролитных расстройств, кислотно-основного состояния, газообмена.
При развитии инфекционно-токсического шока вводят коллоидные (реополиглюкин) и кристаллоидные (раствор Рингера и др.) растворы, кортикостероиды. Назначают диуретики – фуросемид (лазикс). При наличии признаков острой почечной недостаточности проводят гемосорбцию, гемодиализ. При прогрессирующей острой дыхательной недостаточности прибегают к искусственной вентиляции легких. Необходимы массаж грудной клетки, меры, направленные на разжижение и эвакуацию мокроты.
Профилактика. Необходимы санитарная охрана водоисточников к обеззараживание воды, используемой для душевых установок и кондиционеров, дезинфекция систем кондиционирования, душевых помещений и установок.
Для профилактики внутрибольничных вспышек инфекции целесообразна тщательная стерилизация больничного оборудования, особенно приборов, используемых в терапии органов дыхания. При возникновении вспышек легионеллеза в лечебных учреждениях временно приостанавливают плановые операции, гемодиализ, пересадку органов.
Больных легионеллезом размещают в отдельных палатах, боксах, полубоксах. Работу с материалом от больных проводят в перчатках, масках. Персонал лабораторий по выделению возбудителя работает в защитном костюме второго типа.
Специфическая профилактика легионеллеза не разработана.
Менингококковая инфекция
Менингококковая инфекция— острое инфекционное заболевание, характеризующееся значительным клиническим полиморфизмом и протекающее в виде назофарингита, менингита и(или) менингококкового сепсиса.
Исторические сведения. Менингококковая инфекция в своей наиболее яркой клинической форме – эпидемического цереброспинального менингита – известна с древних времен. Описания вспышек этой инфекции содержатся в трудах Аретея (II в. до н.э.), Цельса (I в н.э.), Павла Эгинского (VII в.). В качестве самостоятельного заболевания эпидемический цереброспинальный менингит был выделен и подробно описан М.Вьесо в 1805 г. после вспышки в Женеве. Новый этап в изучении менингококковой инфекции начался в 1887 г., когда А.Вейксельбаум обнаружил и подробно описал возбудителя.
Важное значение имело выделение В.Ослером в 1899 г. возбудителя из крови. Оно во многом прояснило вопросы патогенеза заболевания и, главное, послужило доказательством того, что менингит – не единственное проявление менингококковой инфекции. В первые десятилетия XX в. начинается изучение структуры менингококков. Тогда же были сделаны попытки применить специфические сыворотки для лечения менингококковой инфекции. В 30-х годах в терапии стали использовать сульфаниламидные препараты, а в 40—50-х годах – антибиотики.
Этиология. Возбудитель менингококковой инфекции – neisseria meningitides относится к роду Neisseria семейства Nеisseriасеае. Средние размеры менингококка – 0,6—1 мкм. В мазках цереброспинальной жидкости и крови менингококки выявляются в форме кофейного или бобового зерна, располагаются в типичных случаях попарно, выпуклыми краями наружу и находятся внутриклеточно. Встречаются и внеклеточно расположенные микроорганизмы.
Менингококки исключительно требовательны к составу питательных сред, размножаются только в присутствии человеческого или животного белка либо специального набора аминокислот. Экзотоксина не образуют, при гибели микробной клетки высвобождается эндотоксин липополисахаридной природы.
По антигенной структуре менингококки подразделяются на ряд серологических групп: А, В, С, D, X, Y, X и др.
Возбудитель менингококковой инфекции характеризуется низкой устойчивостью во внешней среде: при температуре +50 °С погибает через 5 мин, при +100 °С – за 30 с. Менингококк малоустойчив и к низким температурам: при —10 °С погибает через 2 ч. Прямой солнечный свет убивает менингококки за 2—8 ч, под действием ультрафиолетовых лучей возбудитель погибает практически мгновенно. Менингококки очень чувствительны ко всем дезинфектантам.
Эпидемиология. Менингококковая инфекция – строгий антропоноз. Источником инфекции может быть только человек. Выделяет 3 группы источников менингококковой инфекции: 1) больные генерализованными формами болезни; 2) больные менингококковым назофарингитом; 3) носители менингококков.
Наибольшую заразительность имеют больные с манифестными формами инфекции. Показано, что за один и тот же промежуток времени один больной способен заразить в 6 раз больше людей, чем один носитель. Тем не менее основным источником менингококковой инфекции справедливо считаются носители. Это связано с тем, что на одного больного с клинически выраженными признаками заболевания приходится 1800—2000 носителей менингококка (по данным некоторых авторов, до 50 000). В итоге больные генерализованными формами инфекции являются источником заражения не более чем для 1—3 % от общего числа инфицированных, больные назофарингитом – для 10-30 %, а носители – для 70-80 %.
Механизм передачи инфекции – аэрогенный. Передача возбудителя происходит воздушно-капельным путем во время экспираторных актов: при разговоре, чиханье, громком крике. Рассеиванию возбудителей и интенсификации механизма передачи способствует сочетание менингококковой инфекции (в том числе и носительства) с острыми респираторными заболеваниями.
Восприимчивость к менингококковой инфекции всеобщая. Ее особенностью является то, что у большинства инфицированных лиц заболевание протекает в виде бессимптомного носительства.
Около 80 % случаев болезни приходится на детей и подростков, из них 50 % составляют дети в возрасте 1 года – 5 лет. Среди взрослых наибольшее число случаев болезни падает на молодой возраст (15—30 лет). По-видимому, это связано с социальными факторами и особенностями образа жизни молодых людей (служба в армии, обучение в учебных заведениях, проживание в общежитиях и т.д.). С этими же обстоятельствами связано преобладание в структуре заболеваемости менингококковой инфекцией лиц мужского пола.
Возрастная структура носительства менингококков существенно отличается от структуры заболеваемости. Большая часть носителей выявляется среди взрослых, доля детей среди носителей менингококка невелика.
Заболеваемость менингококковой инфекцией в городах обычно выше, чем в сельской местности. Описаны значительные вспышки заболевания в учебных заведениях закрытого типа и особенно среди военнослужащих.
В результате перенесенной менингококковой инфекции формируется довольно стойкий иммунитет. В последние годы доказано развитие иммунитета и в результате носительства менингококков, что, по-видимому, определяет общие закономерности иммунитета к этой инфекции.
Распространение менингококковой инфекции повсеместное. Периодически, каждые 10—15 лет, наблюдаются подъемы заболеваемости. Для менингококковой инфекции характерна зимне-весенняя сезонность с максимальным числом заболеваний в феврале – апреле.
Патогенез и патологоанатомическая картина. Входными воротами инфекции являются верхние дыхательные пути, чаще всего носоглотка. В месте внедрения возбудителя развивается воспалительный процесс. В случае преодоления защитного барьера слизистых оболочек менингококк проникает в кровь, развивается менингококкемия, которая сопровождается массивной гибелью возбудителей и токсинемией. Циркуляция возбудителя и токсинов в крови приводит к повреждению эндотелия сосудов и развитию множественных кровоизлияний в различные ткани и внутренние органы. В ряде случаев менингококкемия протекает в виде септикопиемии, тогда во внутренних органах формируются вторичные метастатические очаги (менингококковые эндокардиты, артриты, иридоциклиты и др.).
Проникновение менингококков в полость черепа в подавляющем большинстве случаев происходит гематогенным путем в результате преодоления гематоэнцефалического барьера. В редких случаях возбудитель может попадать в субарахноидальное пространство сквозь решетчатую кость по периваскулярным и периневральным лимфатическим путям, минуя общий кровоток.
В результате попадания менингококков в субарахноидальное пространство и размножения возбудителей возникает серозно-гнойное, а затем гнойное воспаление мягких мозговых оболочек.
Воспалительный процесс локализуется чаще всего на поверхности больших полушарий и основании головного мозга, но нередко распространяется и на спинной мозг. Возможно распространение патологического процесса на эпендиму желудочков мозга с развитием гнойного эпендиматита. Макроскопически головной мозг выглядит покрытым гнойной шапочкой или чепчиком, мягкая мозговая оболочка в свободных от скопления гноя местах представляется отечной, гиперемированной и мутной.
При тяжелых формах воспалительный процесс может захватить мозговое вещество с инъекцией и расширением сосудов, мелкими кровоизлияниями, воспалительными фокусами. Описаны случаи распространения патологического процесса на корешки черепных нервов (чаще всего VII и VIII пар, но также и V, VI, III, XII и др.).
В процессе обратного развития гнойного экссудата при не– благоприятных условиях (затяжное течение менингита, неполноценное лечение) может происходить соединительнотканная организация его. В результате спаечного процесса возникает окклюзия отверстий Мажанди, Лушке, Кея, Ретциуса, водопровода среднего мозга (сильвиева водопровода), очаговое или тотальное запустевание подпаутинных пространств, облитерация периваскулярных путей. Это в свою очередь является основой для возникновения гидроцефалии.
В патогенезе особо тяжелых форм менингококковой инфекции на первый план выходят токсический и аллергический (аутоаллергический) компоненты.
Так, центральное место в патогенезе молниеносной менингококкемии современные исследователи отводят инфекционно-токсическому шоку. При этом у больных развиваются расстройства гемостаза (по типу коагулопатии потребления), гемодинамические расстройства и нарушения микроциркуляции в органах и тканях, резкие сдвиги в электролитном и гормональном гомеостазе. Патологоанатомически у погибших людей выявляются типичные изменения в сосудах, тромбозы, кровоизлияния в различные органы, в том числе в надпочечники, некрозы.
При гистологическом исследовании элементов экзантемы наблюдаются поражения сосудов кожи и перифокальные воспалительные изменения. В сосудах обнаруживаются лейкоцитарно-фибринозные тромбы, содержащие менингококки. Следовательно, кожные высыпания при менингококкемии по существу становятся вторичными метастатическими очагами инфекции.
Выраженный токсикоз является основной причиной очень тяжелого, нередко смертельного осложнения менингококковой инфекции – церебральной гипертензии. Этот синдром возникает в результате острого набухания и отека головного мозга, которые развиваются одновременно с гиперпродукцией и нарушением оттока цереброспинальной жидкости (ликвора). Увеличение объема головного мозга вследствие отека и набухания приводит к его смещению и вклинению миндалин мозжечка в большое затылочное отверстие. Происходит сдавливание продолговатого мозга с быстрым развитием паралича дыхания, а затем и сосудистого паралича.
Иногда при тяжелом течении менингококковой инфекции, особенно у детей раннего возраста, развивается не гипертензия, а, напротив, церебральная гипотензия (церебральный коллапс). В генезе этого осложнения имеет значение сочетание резкого токсикоза с тяжелыми расстройствами водно-солевого обмена. Церебральный коллапс в свою очередь является центральным звеном патогенеза субдурального выпота.
Клиническая картина. Длительность инкубационного периода при менингококковой инфекции колеблется от 1 до 10 дней, чаще составляя 5—7 дней.
В соответствии с клинической классификацией менингококковой инфекции выделяют следующие ее формы:
I. Первично-локализованные:
1) менингококковыделительство;
2) острый назофарингит;
3) пневмония.
II. Гематогенно-генерализованные:
1) менингококкемия: типичная, молниеносная, хроническая;
2) менингит;
3) менингоэнцефалит;
4) смешанная (менингококкемия +менингит);
5) редкие формы (эндокардит, артрит, иридоциклит).
Менингококковыделительство не имеет никаких клинических проявлений.
Острый назофарингит. Наиболее постоянными являются жалобы больных на головную боль, преимущественно в лобно-теменной области, першение и боли в горле, сухой кашель, заложенность носа. Эти симптомы чаще всего сочетаются с ухудшением общего самочувствия больных: недомоганием, вялостью, слабостью, снижением аппетита, нарушением сна. У большинства больных температура тела повышается до субфебрильных цифр. Продолжительность лихорадки, как правило, не превышает 1—3 дней, лишь в редких случаях она сохраняется 5—7 дней. Кожные покровы у больных бледные, сосуды конъюнктивы и склер инъецированы. Слизистые оболочки носа гиперемированы, отечны.
Гиперемия миндалин, мягкого неба и небных дужек выражена незначительно, иногда отсутствует. На этом фоне особенно заметны яркая гиперемия и отек задней стенки глотки, а также гиперплазия ее лимфоидных фолликулов. У многих больных задняя стенка глотки покрыта слизистым или слизисто-гнойным экссудатом.
Воспалительные изменения в носоглотке определяются в течение 5—7 дней, гиперплазия лимфоидных фолликулов держится обычно дольше (до 14—16 дней).
В периферической крови можно выявить умеренный лейкоцитоз с нейтрофилезом и сдвигом лейкоцитарной формулы влево, повышение СОЭ.
У 30—50 % больных назофарингит сочетается с другими проявлениями менингококковой инфекции и предшествует развитию генерализованных форм заболевания.
Пневмония. В некоторых случаях менингококки вызывают первичную пневмонию, протекающую без каких-либо проявлений данной инфекции. Менингококковая пневмония может иметь очаговый или лобарный характер. В том и другом случае ее отличает довольно тяжелое и продолжительное течение.
Менингококкемия. Это менингококковый сепсис, протекающий бурно, с выраженными симптомами токсикоза и развитием вторичных метастатических очагов.
Заболевание начинается, как правило, остро. Температура тела с ознобом повышается до 39—41 °С. В дальнейшем лихорадка может носить постоянный характер, быть интермиттирующей, гектической, волнообразной. Возможно безлихорадочное течение менингококкового сепсиса. Степень повышения температуры тела не соответствует тяжести течения заболевания. При развитии инфекционно-токсического шока температура обычно снижается до субфебрильной или нормальной.
Одновременно с лихорадкой возникают другие симптомы интоксикации: головная боль, снижение или отсутствие аппетита, общая слабость, боли в мышцах спины и конечностей, жажда, сухость во рту, бледность и цианоз кожных покровов.
Наблюдаются тахикардия, снижение артериального давления, тахипноэ и нередко одышка. Уменьшается мочеотделение. У большинства больных заметна тенденция к задержке стула, у некоторых, напротив, развиваются поносы. Последние более характерны для детей младшего возраста.
Наиболее ярким, постоянным и диагностически ценным признаком менингококкемии является экзантема. Кожные высыпания возникают через 5—15 ч, иногда на 2-е сутки от начала заболевания. Сыпь при менингококковой инфекции может быть разнообразной по характеру и величине высыпных элементов, а также по локализации. Наиболее типичной является геморрагическая сыпь (петехии, пурпура, экхимозы). Элементы сыпи имеют неправильную (звездчатую) форму, плотны на ощупь, иногда выступают над уровнем кожи. Нередко геморрагическая сыпь сочетается с розеолезной или розеолезно-папулезной. Изредка встречаются везикулезные, буллезные высыпания, сыпь в форме узловатой эритемы. Как правило, сыпь при менингококкемии обильная. Она преимущественно локализуется на конечностях, туловище, ягодичных областях, а реже – на лице. Не являются редкостью случаи болезни, когда экзантема бывает скудной.
Часто встречаются энантема на переходной складке конъюнктивы, кровоизлияния в склеры, описана энантема на слизистой оболочке рта.
Обратное развитие сыпи зависит от характера и величины ее элементов, а также глубины поражения кожи. Глубокие и обширные кровоизлияния могут некротизироваться.
В дальнейшем участки некроза отторгаются и образуются медленно заживающие язвы. На конечностях иногда наблюдаются глубокие некрозы всех мягких тканей с обнажением костей. Нередки случаи некрозов ушных раковин, кончика носа, концевых фаланг пальцев рук и ног.
В соскобах и биоптатах элементов сыпи у нелеченых больных с большим постоянством обнаруживаются менингококки.
Метастазы возбудителя в суставы наблюдаются значительно реже, чем в кожу. Чаще поражаются мелкие суставы. Тяжесть артритов может быть различной – от гнойных поражений до легких изменений с болезненностью при движениях, небольшой гиперемией и отеком кожи над пораженным суставом. Из полости сустава можно получать культуру менингококка.
Артриты возникают позже, чем сыпь, к концу 1-й – началу 2-й недели болезни. Прогноз их благоприятный, при выздоровлении функции суставов полностью восстанавливаются.
Вторичные метастатические очаги инфекции могут возникать в сосудистой оболочке глаза, в пери-, мио– и эндокарде, легких, плевре, что в современных условиях встречается редко. Еще реже подобные очаги возникают в почках, печени, костном мозге.
В гемофамме при менингококкемии обнаруживается умеренный или высокий нейтрофильный лейкоцитоз (20,0—40,0 * 10^9 /л и более) со сдвигом лейкоцитарной формулы влево до юных и миелоцитов, анэозинофилия, повышение СОЭ. Нередко развивается тромбоцитопения.
В моче имеются изменения, свойственные синдрому инфекционно-токсической почки, – протеинурия, цилиндрурия, микрогематурия.
В подавляющем большинстве случаев менингококковый сепсис протекает в сочетании с менингитом. Однако у 4—10 % госпитализированных по поводу менингококковой инфекции больных менингококкемия встречается в «чистом» виде, без поражения мягкой мозговой оболочки. Частота менингококкового сепсиса обычно выше в периоды эпидемий.
Менингококкемия может протекать в легкой, среднетяжелой и тяжелой формах.
Молниеносная менингококкемия (Синонимы: сверхострый менингококковый сепсис, молниеносная пурпура, фульминантная менингококкемия, синдром Уотерхауза – Фридериксена). Это наиболее тяжелая, прогностически крайне неблагоприятная форма менингококковой инфекции. По существу она представляет собой инфекционно-токсический шок. Клинически характеризуется острейшим, внезапным началом и бурным течением. Те пература тела с ознобом быстро повышается до 40—41 °С, однако через несколько часов она может смениться гипотермией. Уже в первые часы болезни возникает обильная геморрагическая сыпь с тенденцией к слиянию и образованию обширных кровоизлияний, которые могут быстро некротизироваться. На коже появляются багрово-цианотичные пятна, перемещающиеся при перемене положения тела (они получили название «трупные пятна» – «livors mortalis»). Кожные покровы бледные, но с тотальным цианозом, влажные, покрыты холодным липким потом, черты лица заостряются. Больные беспокойны, возбуждены, у них нередко появляются судороги, особенно у детей. В первые часы болезни сознание сохранено, при этом больные жалуются на сильные мышечные боли, артралгии, боли в области живота, гиперестезии. Нередко возникает повторная рвота (часто «кофейной гущей»), возможен кровавый понос. Постепенно нарастает прострация, наступает потеря сознания.
Параллельно катастрофически ослабевает сердечная деятельность. Развивается анурия («шоковая почка»). Часто выявляется гепатоспленомегалия. Менингеальный синдром непостоянен, но может быть и резко выраженным.
В гемограмме гиперлейкоцитоз (до 60 *10^9 /л), нейтрофилез, резкий сдвиг лейкоцитарной формулы влево, тромбоцитопения, повышение СОЭ (50—70 мм/ч). Выявляются резкие расстройства гомеостаза – метаболический ацидоз, коагулопатия потребления, снижение фибринолитической активности крови и др.
В отсутствие рациональной терапии больные погибают в первые часы и сутки болезни от острой сердечно-сосудистой или острой почечной недостаточности.
Менингококкемия хроническая. Редкая форма менингококковой инфекции. Продолжительность заболевания различная – от нескольких недель до нескольких лет. Лихорадка обычно интермиттирующая, но встречается и постоянная; сопровождается высыпаниями по типу полиморфной экссудативной эритемы. В периоды ремиссий температура тела может быть нормальной, сыпь бледнеет и даже исчезает, самочувствие больных заметно улучшается. При хронической менингококкемии возможны артриты и полиартриты, нередко наблюдается гепатоспленомегалия.
В периферической крови – лейкоцитоз, нейтрофилез, увеличение СОЭ. В моче – умеренная или небольшая протеинурия, а при развитии специфического гломерулонефрита – соответствующий мочевой синдром. Описаны эндокардиты (панкардиты), а также возникновение менингита через несколько недель или месяцев от начала заболевания.
Прогноз хронического менингококкового сепсиса относительно благоприятный, при правильном лечении – хороший.
Менингит. Может начинаться вслед за менингококковым назофарингитом, но иногда первые признаки заболевания возникают внезапно, среди полного здоровья.
При менингите с большим постоянством обнаруживается следующая триада симптомов: лихорадка, головная боль и рвота. Температура тела обычно повышается быстро, с сильнейшим ознобом и может достигать 40—42 °С в течение нескольких часов. Температурная кривая характерных черт не имеет, встречаются интермиттирующий, ремиттирующий, постоянный, двухволновой типы кривых.
Головные боли при менингите исключительно сильные, мучительные, чаще без определенной локализации, диффузные, в большинстве своем имеют пульсирующий характер. Особой интенсивности они достигают по ночам, усиливаются при перемене положения тела, резком звуке, ярком свете. Нередко больные стонут от болей. Рвота при менингите возникает без предшествующей тошноты, вне связи с приемом пищи, внезапно, не приносит облегчения больному.
Весьма часто при менингите встречаются резкая кожная гиперестезия и повышение чувствительности к слуховым (гиперакузия), световым (фотофобия), болевым (гипералгезия) раздражителям, запахам (гиперосмия). У многих больных уже в первые часы болезни возникают тяжелые судороги: клонические, тонические или смешанные.
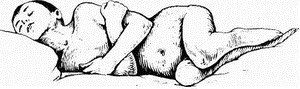
Рис. Характерная поза больного менингитом (по А.Соколову).
Большое место в клинической картине менингококкового менингита занимают расстройства сознания вплоть до его потери (от сопора до комы). Нередко потеря сознания следует за психомоторным возбуждением. Выключение сознания в первые часы болезни является прогностически неблагоприятным признаком. Возможно течение менингита при ясном сознании.
При объективном обследовании на первое место выступают менингеальные симптомы. Они появляются уже в 1 –е сутки болезни, в дальнейшем быстро прогрессируют. Описано около 30 менингеальных знаков. В практической деятельности используются некоторые из них, наиболее постоянные: ригидность затылочных мышц, симптомы Кернига, Брудзинского (нижний, средний, верхний), а также Гийона, Бехтерева, Мейтуса и др.
Выраженность менингеального синдрома может не соответствовать тяжести заболевания, а выраженность различных симптомов не всегда одинакова у одного и того же больного.
В самых тяжелых запущенных случаях больной принимает характерную вынужденную позу – лежит на боку с запрокинутой головой, ноги согнуты в коленных и тазобедренных су– ставах, притянуты к животу (положение взведенного курка – «chien en fusil» . Как правило, у больных менингитом наблюдаются асимметрия и повышение сухожильных периостальных и кожных рефлексов, которые в дальнейшем, по мере углубления интоксикации, могут снижаться и исчезать совсем. В ряде случаев можно выявить патологические рефлексы (Бабинского, Гордона, Россолимо, Оппенгеймера, клонус стоп), а также симптомы поражения некоторых черепных нервов (чаще всего III, IV, VII, VIII пар). Страдает вегетативная нервная система, что проявляется наличием стойкого красного дермографизма.
Многочисленные симптомы поражения других органов и систем обусловлены интоксикацией. В первые часы развивается тахикардия, затем появляется относительная брадикардия. Артериальное давление снижается. Тоны сердца приглушены, нередко аритмичны. Может быть умеренно выраженное тахипноэ. Язык обложен грязно-коричневым налетом, сухой. Живот втянут, мышцы брюшного пресса у некоторых больных напряжены.
У большинства заболевших развиваются запор, иногда рефлекторная задержка мочеиспускания.
Весьма характерен внешний вид больных менингитом. В первые дни лицо и шея гиперемированы, сосуды склер инъецированы. Как и при некоторых других тяжелых заболеваниях, при менингите оживляется латентная герпетическая инфекция и появляются пузырьковые высыпания на губах, крыльях носа, слизистых оболочках рта.
В гемограмме – высокий нейтрофильный лейкоцитоз со сдвигом лейкоцитарной формулы влево, увеличение СОЭ. В моче – небольшая протеинурия, микрогематурия, цилиндрурия.
Осложнения менингококкового менингита. У части больных развиваются осложненные варианты заболевания.
Молниеносное течение менингита с синдромом набухания и отека головного мозга — крайне неблагоприятный вариант, протекающий с гипертоксикозом и высокой летальностью. Главные симптомы являются следствием вклинения головного мозга в большое затылочное отверстие и ущемления продолговатого мозга миндалинами мозжечка.
Быстро развиваются угрожающие симптомы нарушения деятельности сердечно-сосудистой и дыхательной систем. Появляется брадикардия, которая сменяется тахикардией, артериальное давление лабильно, может катастрофически падать, но чаще повышается до предельно высоких цифр. Возникают тахипноэ (до 40—60 в 1 мин) с участием вспомогательной дыхательной мускулатуры, резкая одышка, затем возможна аритмия дыхания типа Чейна – Стокса. Расстройства дыхания приводят к внезапной остановке его.
Указанные симптомы разворачиваются при нарастающей гипертермии, клонических судорогах и потере сознания.
У больных отмечается резкая потливость, кожные покровы цианотичны, лицо гиперемировано. Определяются пирамидальные знаки, иногда симптомы поражения черепных нервов, угасание корнеальных рефлексов, сужение зрачков и снижение их реакции на свет.
Больные погибают при этом варианте течения менингококкового менингита, как правило, от остановки дыхания. Смерть может наступить в первые часы болезни, но иногда – на 2—3-й и даже 5—7-й день.
Менингит с синдромом церебральной гипотензии – редкий вариант течения менингококкового менингита, диагностируемый преимущественно у детей младшего возраста.
Заболевание развивается бурно, протекает с резкими токсикозом и эксикозом. Быстро развивается ступор, возможны судороги, менингеальные знаки не выражены, что затрудняет диагностику. Внутричерепное давление резко падает, при этом уменьшается объем жидкости в желудочках головного мозга, развивается вентрикулярный коллапс. Большой родничок у грудных детей западает. У старших детей и взрослых опорными моментами в диагностике являются клинические признаки обезвоживания и низкое давление цереброспинальной жидкости, которая при люмбальном проколе вытекает редкими каплями. Падение внутричерепного давления при менингите может привести к развитию крайне тяжелого осложнения – субдуральной гематомы (выпота).
Менингит с синдромом эпендиматита (вентрикулита) — в современных условиях редкая форма менингита, которая развивается главным образом при запоздалом или недостаточном лечении больных. Особая тяжесть заболевания обусловлена распространением воспаления на оболочку, выстилающую желудочки мозга (эпендиму), а также вовлечением в патологический процесс вещества головного мозга (субэпендимарный энцефалит).
Основные клинические симптомы: тотальная ригидность (больные принимают вынужденную позу – ноги вытянуты и перекрещиваются в нижних отделах голеней, кисти рук сжаты в кулаки), расстройства психики, сонливость, мощные тонические и клонические судороги. Температура тела нормальная или субфебрильная при общем тяжелом состоянии больного. Постоянным симптомом является рвота, нередко упорная. Возможны парезы сфинктеров с непроизвольным отхождением кала и недержанием мечи. При длительном течении и(или) безуспешной терапии эпендиматита развиваются гидроцефалия, кахексия и наступает смерть. В случае изолированного или преимущественного поражения эпендимы IV желудочка главными в клинической картине будут расстройства дыхания, сердечно-сосудистой деятельности и другие симптомы повреждения ядер черепных нервов ромбовидной ямки (дно IV желудочка).
Менингоэнцефалит. Относительно редкая форма менингококковой инфекции, при которой преобладают симптомы энцефалита, а менингеальный синдром выражен слабо.
Для менингококковых энцефалитов характерно быстрое начало и бурное развитие нарушений психики, судорог, парезов, параличей. Прогноз неблагоприятный, даже в современных условиях летальность остается высокой, а выздоровление неполным.
Смешанная форма (менингококковая + менингит). Встречается в 25—50 % случаев генерализованной менингококковой инфекции, причем в последние годы определилась тенденция к нарастанию частоты смешанной формы в общей структуре заболеваемости, особенно в периоды эпидемических вспышек. Клинически характеризуется сочетанием симптомов менингококкового сепсиса и поражением мозговых оболочек.
Редкие формы. Редкие формы менингококковой инфекции (артриты и полиартриты, эндокардит, иридоциклиты) в подавляющем большинстве случаев, по-видимому, являются следствием менингококкемии. Прогноз их при своевременной и достаточной терапии благоприятный.
Диагностика. Диагноз всех форм менингококковой инфекции базируется на комплексе данных, полученных эпидемиологическим, анамнестическим и клиническим методами, и окончательно устанавливается с помощью лабораторных исследований. Отдельные методы имеют неодинаковую диагностическую ценность при различных клинических формах менингококковой инфекции. Так, диагноз менингококковыделительства возможен лишь при использовании бактериологического метода, когда материалом для изучения является слизь проксимальных отделов верхних дыхательных путей.
В диагностике менингококкового назофарингита главное место занимают эпидемиологический и бактериологический методы, так как клинически разграничить менингококковый назофарингит от другого генеза невозможно или крайне трудно.
В распознавании генерализованных форм реальную диагностическую ценность приобретает анамнестический и клинический методы диагностики, особенно при сочетании менингококкемии и менингита. В диагностике менингита большое значение имеет исследование цереброспинальной жидкости.
При генерализованных формах менингококковой инфекции окончательный диагноз верифицируется бактериологическим методом.
Из иммунологических методов наиболее чувствительны и информативны РНГА, ИФА.
Лечение. Терапевтическая тактика при менингококковой инфекции зависит от клинической формы, тяжести течения заболевания, наличия осложнений, преморбидного фона.
Этиологическая терапия. Лечение менингококкового назофарингита. При назофарингите средней тяжести показаны антибактериальные препараты. Чаще всего применяют пероральные антибиотики: ампиокс, оксациллин, левомицетин, тетрациклин, эритромицин и другие макролиды, в соответствии с результатами изучения чувствительности выделенного возбудителя. Применяемые дозы антибиотиков – среднетерапевтические, возрастные. Продолжительность терапии – 3—5 дней и более. Используют также сульфаниламидные препараты пролонгированного действия в обычных дозах. При легком течении назофарингита назначение антибиотиков и сульфаниламидов необязательно.
Всем больным следует рекомендовать частые полоскания горла растворами антисептиков. При наличии интоксикации – обильное и частое питье.
Лечение генерализованных форм менингококковой инфекции. Центральное место в терапии принадлежит антибиотикам, в первую очередь солям бензилпенициллина. Применяют бензил– пенициллин в суточной дозе 200 000—500 000 ЕД на 1 кг массы больного.
В запущенных случаях менингита, при поступлении больного в стационар в бессознательном состоянии, а также при наличии эпендиматита (вентрикулита) или признаков консолидации гноя доза вводимого пенициллина повышается до 800 000—1 000 000 ЕД/кг в сутки. В подобных обстоятельствах прибегают к внутривенному введению натриевой соли бензил– пенициллина (введение в вену больших доз калиевой соли недопустимо из-за опасности гиперкалиемии) в дозе 2 000 000—12 000 000 ЕД в сутки, сохраняя внутримышечную дозу препарата. Внутривенную дозу пенициллина лучше вводить капельным способом. Эндолюмбальное введение пенициллина в последние годы практически не применяется.
Суточная доза пенициллина вводится больному через каждые 3 ч. В некоторых случаях допустимо увеличение интервалов между инъекциями до 4 ч. Продолжительность пенициллинотерапии устанавливается каждый раз индивидуально, исходя из клинических и ликворологических данных. Опыт свидетельствует, что необходимая и достаточная продолжительность терапии пенициллином составляет обычно 5—8 дней.
Достаточно высокой эффективностью при менингококковой инфекции обладают полусинтетические пенициллины. Это наиболее надежные и предпочтительные препараты для «старт-терапии» больных с гнойным менингитом до установления
этиологического диагноза.
Наиболее эффективен при терапии менингококковой инфекции ампициллин, который назначают в суточной дозе 200—300 мг/кг, внутримышечно через каждые 4 ч. В самых тяжелых случаях часть ампициллина вводят внутривенно, а суточную дозу повышают до 400 мг/кг. Оксациллин применяют в дозе не менее 300 мг/кг в сутки с интервалами между инъекциями 3 ч. Метициллин вводят через каждые 4 ч в суточной дозе 200—300 мг/кг.
Высокоэффективен при менингококковой инфекции левомицетин. Он является препаратом выбора при молниеносной менингококкемии. Показано, что при лечении левомицетином эндотоксические реакции у больных возникают значительно реже, чем при пенициллинотерапии. В случае менингоэнцефалитов, напротив, левомицетин не показан из-за токсического действия на клетки головного мозга. Левомицетин для парентерального введения (левомицетина сукцинат растворимый) применяют внутримышечно по 50—100 мг/кг в сутки в 3—4 приема (через каждые 6—8 ч). При молниеносной менингококкемии левомицетин применяют внутривенно через каждые 4 ч до стабилизации артериального давления, после чего продолжают введение внутримышечно. Средняя продолжительность лечения больных этим антибиотиком составляет 6—10 дней.
Ряд авторов отмечают удовлетворительные результаты терапии при менингококковой инфекции препаратами из группы тетрациклинов. Тетрациклин можно вводить в дозе 25 мг/кг в сутки внутривенно и внутримышечно в тех случаях, когда имеется устойчивость возбудителя к другим антибиотикам.
В терапии генерализованных форм менингококковой инфекции, протекающих легко, применяют также сульфаниламидные препараты пролонгированного действия, в том числе для парентерального введения.
Патогенетическая терапия. Исключительное значение в системе терапевтических мероприятий при менингококковой инфекции имеют средства патогенетического лечения.
Патогенетическая терапия проводится одновременно с этиотропной. Ее основой является борьба с токсикозом. Используют кристаллоидные растворы (Рингера, 5 % раствор глюкозы и др.), макромолекулярные коллоидные растворы (препараты поливинилалкоголя, поливинилпирролидона, декстрана, желатиноль), плазму, альбумин и др. Обычно вводят 40—50 мл жидкости на 1 кг массы тела в сутки под контролем диуреза. При сохраненном сознании часть кристаллоидных растворов можно вводить перорально.
Одновременно проводят профилактику гипергидратации головного мозга путем введения мочегонных средств (фуросемид, или лазикс, этакриновая кислота, или урегит), маннитола. Мочевина применяется с осторожностью из-за вероятности развития «феномена отдачи» (усиление отека после прекращения действия препарата).
Вместе с инфузионными растворами вводят витамины С, В1 , В2 , В6 глутаминовую кислоту, кокарбоксилазу, АТФ.
В тяжелых случаях менингококковой инфекции показаны глюкокортикостероидные гормоны. Полная доза устанавливается индивидуально, она зависит от динамики основных симптомов и наличия осложнений. Обычно применяют гидрокортизон в дозе 3—7 мг/кг в сутки, преднизолон в дозе 1—2 мг/кг в сутки или другие кортикостероиды в соответствующей дозировке.
Большое значение в лечении больных имеют оксигенотерапия, ультрафиолетовое облучение крови.
Лечение молниеносной менингококкемии заключается в мероприятиях по выведению больного из шока. Как правило, необходима закрытая катетеризация подключичной или другой вены или венесекция и катетеризация открытым способом вены достаточного диаметра. Иногда приходится начинать реанимационные мероприятия с внутриартериального введения жидкостей. Использование адреналина и адреномиметиков не показано из-за возможности капилляроспазма, усугубления гипоксии мозга и почек и развития острой почечной недостаточности. Применение этих препаратов возможно лишь при отсутствии эффекта в качестве «терапии отчаяния».
В случае возникновения острой почечной недостаточности в результате токсемии и шока показан ранний гемодиализ.
Профилактика. Мероприятия, направленные на источники менингококковой инфекции, включают в себя раннее и исчерпывающее выявление больных, санацию носителей менингококков, изоляцию и лечение больных. В очаге инфекции устанавливается медицинское наблюдение за контактными лицами в течение 10 дней.
Меры, направленные на разрыв механизма передачи инфекции, заключаются в проведении санитарно-гигиенических мероприятий и дезинфекции. Необходимо по возможности ликвидировать скученность, особенно в закрытых учреждениях (детские сады, казармы и т.п.). В помещениях проводятся влажная уборка с использованием хлорсодержащих дезинфектантов, частое проветривание, ультрафиолетовое облучение воздуха и т.д.
Мероприятия, направленные на восприимчивые контингента, включают в себя повышение неспецифической устойчивости людей (закаливание, своевременное лечение заболеваний верхних дыхательных путей, миндалин) и формирование специфической защиты от менингококковой инфекции. Наиболее перспективна активная иммунизация с помощью менингококковых вакцин.
К настоящему времени создано несколько вакцин, в частности полисахаридные вакцины А и С. Получена также вакцина из менингококков группы В.

