Полуторавековое ожидание родственника
Все приходит в свое время для тех, кто умеет ждать.
ОНОРЕ ДЕ БАЛЬЗАК
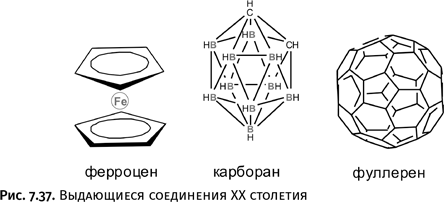
«Биографии» некоторых химических соединений складываются своеобразно, иногда совершенно неожиданно. Например, появление трех соединений – ферроцена, карборана и фуллерена – сопровождалось буквально взрывным количеством публикаций. Каждое из них создало новую главу в химической науке (рис. 7.37 и 7.38).
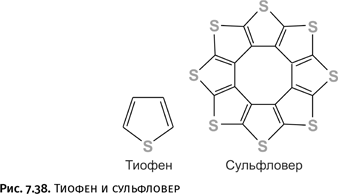
Судьба большинства других соединений не столь эффектна, их появление бывает замеченным, но постепенно интерес к ним пропадает, и только немногим удается со временем вновь привлечь к себе внимание. Например, тиофен, открытый в 1882 г. В. Мейером (в результате неудачи при демонстрационном опыте), вызвал интерес, который быстро угас. В течение длительного времени его рассматривали как загрязнение, мешающее проведению некоторых аналитических и спектральных работ. Планомерное изучение химии тиофена не помогло ему выдвинуться на заметное место. Но недавно тиофену все же удалось эффектно заявить о себе благодаря работам профессора В.Г. Ненайденко, который сумел получить циклическую конструкцию из восьми спаянных молекул тиофена. Автор предложил для нового соединения образное название: сульфловер, и сегодня он упоминается уже в сотне работ.
Продукт полимеризации пропилена – (CH3–CH=CH2), полипропилен – в течение нескольких десятилетий никого не интересовал, поскольку представлял собой мягкий липкий продукт. В 1954 г. катализатор Циглера – Натты позволил провести полимеризацию пропилена так, чтобы звенья в полимерной цепи расположились строго определенным образом. В результате был получен прочный теплостойкий материал, ежегодное производство которого в наши дни составляет десятки миллионов тонн. Сегодня изделия из такого полипропилена можно встретить буквально на каждом шагу.
Схожая судьба и у некоторых химических элементов и превращений. Уран с момента открытия ожидал целое столетие до своего масштабного применения в атомных станциях, а совместная циклизация алкинов и азидов, обнаруженная более 100 лет назад, недавно пережила второе рождение, дав начало новому научному направлению – клик-химии (click-chemistry), это реакции, протекающие мгновенно и без побочных продуктов. Аналогичная ситуация имеет место и в других областях науки, например в физической химии. Так, сверхкритическое состояние вещества «дремало» полтора столетия до момента, когда его начали использовать в промышленном масштабе, а жидкокристаллическое состояние вещества привело к появлению одноименных дисплеев спустя 80 лет после открытия этого явления. Сколько еще таких научных открытий ждут своего часа!
В ТЕНИ БОЛЬШОГО БРАТА
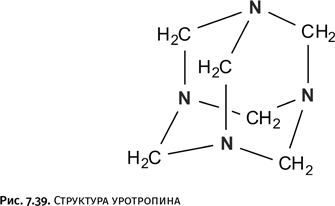
А теперь поговорим об уротропине. Уротропин был синтезирован А.М. Бутлеровым в 1859 г. Проводя взаимодействие формальдегида с аммиаком, он неожиданно получил белое кристаллическое вещество, не содержащее кислорода. Его состав соответствовал формуле (CH2)6N4, Бутлеров назвал его гексаметилентетрамином. Со временем соединение получило название «уротропин», ставшее общепринятым. Структура этого соединения была установлена много позже, в 1922 г., Р. Дикинсоном и А. Реймондом из США (рис. 7.39). Примечательно, что это было первое органическое соединение, строение которого было установлено рентгеноструктурным анализом. Удивительно, что необычная изящная структура каркаса уротропина не привлекла особого внимания.
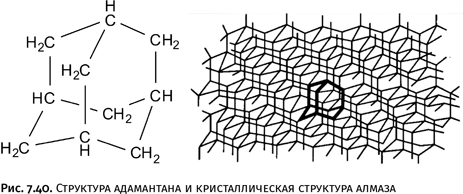
Повышенный интерес к структурам такого типа возник после того, как в 1933 г. чешские химики С. Ланда и В. Махачек выделили из годонинской нефти соединение C10H16. Они предложили структуру этого соединения (ее позже подтвердили структурные исследования) и дали ему название адамантан (от греч. adamantos – алмаз), поскольку каркас молекулы воспроизводит фрагмент кристаллической структуры алмаза (рис. 7.40).
Получить адамантан в лаборатории удалось швейцарскому химику В. Прелогу в 1941 г. пятистадийным синтезом с выходом менее одного процента. Позже были найдены более простые и результативные методики.
Химию этого соединения со столь торжественным названием (что не так уж малозначимо) стали интенсивно изучать. Были получены соединения с различными органическими группами, обрамляющими каркас, и содержащие в структуре атомы O, N, P, S, Si и др. Обилие публикаций привело к появлению монографий, посвященных адамантану.
На этом фоне уротропин, по существу открывший каркасы такого типа, оказался в тени. Он удостоился только упоминания, что это тоже структура адамантанового типа, т. е. один из представителей азаадамантанов (соединения, содержащие атомы N в структуре каркаса). Интересных значимых химических превращений уротропина не было найдено, и в течение многих лет он скромно вел полезное существование. В синтетической органической химии его используют как реагент при получении алифатических и ароматических аминов из соответствующих галогенидов, ароматических альдегидов из бензилгалогенидов и др.
Наиболее известно применение уротропина в качестве лекарственного препарата для лечения инфекции мочевыводящих путей (действующий компонент – образующийся при распаде в кислой среде формалин). Уротропин применяют также в производстве фенольных смол (он поставляет метиленовые группы СН2, обеспечивая образование сшитой структуры), в пищевой промышленности он зарегистрирован как добавка-консервант и, кроме того, представляет собой компонент в производстве взрывчатого вещества гексогена. Нельзя не упомянуть использование уротропина в быту в качестве сухого спирта. Он горит некоптящим пламенем, не образует растекающуюся жидкую массу и сгорает полностью, не оставляя пепла.

