Передвинуть атомы, сохранив структуру каркаса
Последующая часть главы написана по результатам работы сотрудников Института органической химии Российской академии наук доктора химических наук, профессора С.Л. Иоффе и доктора химических наук А. Сухорукова
Вначале обратим внимание на то, что в структуре уротропина атомы азота занимают узловые точки, т. е. вершины каркаса, а фрагменты – СН2– представляют собой мостиковые группы. Существует крупный класс соединений – азаадамантаны с разнообразными органическими группами, окружающими каркас. Они содержат в каркасе от одного до четырех атомов N, однако практически всегда атомы азота занимают вершины каркаса.
Знакомясь с работами, описывающими адамантановые структуры, содержащие различные гетероатомы, авторы обратили внимание на то, что при введении атомов О или S в каркас они становятся мостиковыми группами – Х–, а атомы P, N или группировки RSi располагаются в вершинах каркаса – Y<. Таким образом, синтезом всех рассмотренных структур командует природа, руководствуясь традиционным понятием валентности.
Авторов заинтересовало, можно ли целенаправленно вмешаться в этот процесс, поместив в мостиковую позицию те атомы, которые традиционно занимали только узловые места. Таким образом, возникла на первый взгляд необычная задача, возможность решения которой была не очевидна, решено было поменять местами атомы углерода и азота в уротропине.
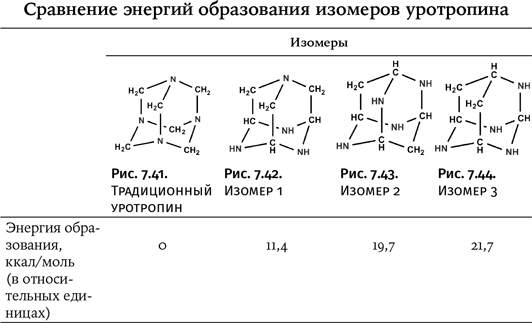
Вначале предстояло решить, какой из возможных вариантов следует выбрать. Вначале рассмотрим три теоретически возможных изомера, по составу полностью совпадающих с классическим уротропином (см. таблицу), при этом варианты, содержащие связи азот – азот, не рассматриваем. Квантовохимическими расчетами была определена энтальпия образования (энергия, выделяющаяся при образовании вещества) каждого изомера, которую сравнивали с этой же величиной для уротропина, чтобы определить, какой из изомеров энергетически более выгоден (рис. 7.41–7.44). В таблице показано сравнение энтальпий изомеров, причем энтальпия образования уротропина принята равной нулю, а отклонения от нуля указывают, насколько каждый из изомеров энергетически более выгоден в сравнении с обычным уротропином.
Результаты расчетов указывали, что среди трех предполагаемых изомеров наименее энергетически выгоден традиционный уротропин. Разница в энергии образования остальных изомеров невелика, наименьшая величина у изомера 1, но авторы работы сосредоточили внимание именно на нем, поскольку у этого изомера имеются преимущества. Атомы азота в нем неравноценны, один атом N не содержит атомов Н, он представляет собой третичный амин, а три остальных содержат по одному атому Н – это вторичные амины. Таким образом, реакционные возможности изомера 1 выше в сравнении с изомерами 2 и 3, содержащими только группы, соответствующие вторичным аминам.
После того как был сделан выбор, следовало наметить путь синтеза изомера 1. Заранее было понятно, что получение новой адамантановой структуры не может быть простым, если вспомнить, сколь трудным был первый синтез адамантана.
Наметилась принципиально новая схема формирования каркаса адамантанового типа. Вначале следует получить молекулу с атомом N, от которого отходят три ветви, содержащие на конце тоже атомы N и, кроме того, реакционные группы. Эти группы представляют собой фрагменты C=N, которые позволят объединить попарно три ветви при раскрытии двойных связей.
Для наглядности изобразим процесс упрощенно с помощью геометрических моделей (рис. 7.45). Раскроем в каждой двойной связи одну связь. Отогнем усики (показано изогнутыми стрелками), направим к атомам C и N, расположенным в соседних ветвях, и соединим атом азота с атомом углерода соседней ветви, образовав, таким образом, новые связи C – N.
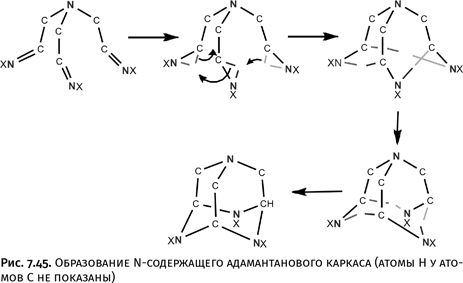
В итоге все три ветви окажутся связанными единым шестичленным циклом, возникшим в нижней части каркаса. Обобщенное название реакций такого типа – «циклотримеризация», т. е. образование цикла из трех фрагментов (в нашем случае это группировки C=N).
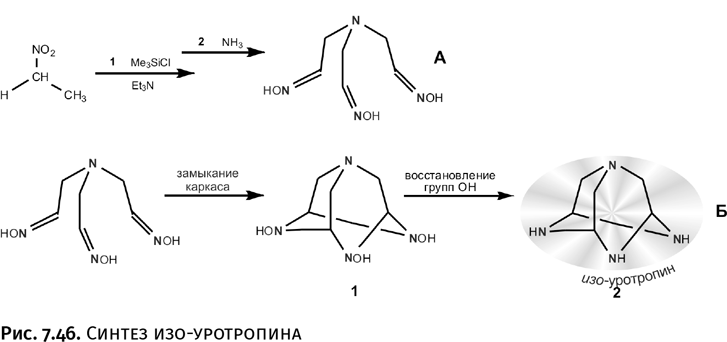
Первый этап, т. е. синтез намеченной трехлучевой заготовки, был проведен в две стадии. Исходное соединение нитроэтан CH3-CH2NO2. Его взаимодействие на первой стадии с триметилхлорсиланом Me3SiCl (в присутствии амина), а затем на следующей стадии с аммиаком приводит к нужному соединению (рис. 7.46, реакция А). Молекула аммиака служит источником того атома азота, который становится центром ветвления.
Полученная трехлучевая молекула была превращена в адамантановую структуру по намеченной ранее схеме. Эксперименты показали, что наиболее полно это превращение проходит в присутствии уксусной кислоты (рис. 7.46, реакция Б). В результате с выходом более 80 % образуется нужный каркас (соединение Б1), но это пока не изомер уротропина – у атомов N находятся группы ОН. После восстановления этих групп водородом (с никелевым катализатором) образуется истинный изо-уротопин, по составу полностью соответствующий классическому и отличающийся только расположением атомов (соединение Б2).
Если получено новое соединение, то всегда возникает желание узнать, на что оно «способно» и каковы его возможности при различных превращениях. Вначале рассмотрим потенциальные реакционные точки – атомы углерода.
К настоящему моменту выделить производные традиционного уротропина, содержащие заместители у атома углерода, не удалось из-за их нестабильности, зато проделать то же самое с изо-уротропином несложно, причем получающиеся соединения устойчивы. Допустим, вы, строя дом, собрали коробку из бетонных плит, а затем в этих плитах вырезаете отверстия для окон. Проще при формовке плит заранее сделать нужные отверстия, а потом собирать из этих плит дом. Точно так же нет необходимости теребить нашу изящную структуру, пытаясь ввести заместители, изо-уротропин дает возможность осуществить это до сборки каркаса. Достаточно включить заранее намеченную группу (например, CH3) в исходное соединение, т. е. в нитроэтан, и провести синтез на основе, например, изомерного нитропропана CH3-CH(СН3)NO2. Точно так же можно присоединить к группам СН и другие органические группы, например бензильную группу.
В процессе работы выяснилась интересная деталь. Оказалось, что замыкание каркаса проходит несравненно легче, если к узловому атому N заранее добавить четвертый заместитель – фрагмент углеводорода. Дело в том, что этот атом N легко присоединяет галогенуглеводороды (рис. 7.47, превращение 1), образуя ионные соединения (точно так же, как из аммиака и хлороводорода образуется аммонийхлорид [NH4]+Cl).
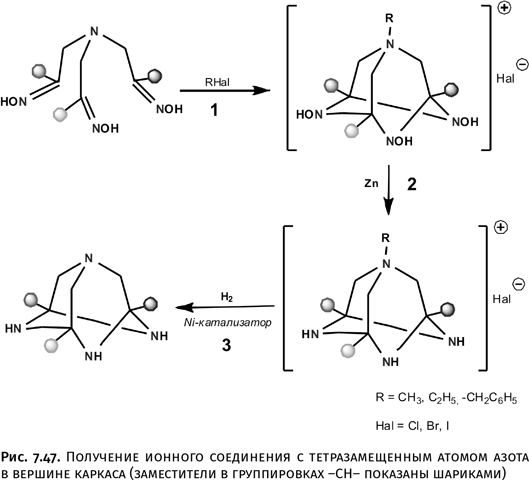
Затем можно превратить группы N – OH в NH, восстановив их цинком (рис. 7.47, превращение 2), а при необходимости на следующем этапе удалить с азота «навешенную» органическую группу действием Н2 в присутствии палладиевого катализатора (рис. 7.47, превращение 3).

