Книга: Вопрос жизни. Энергия, эволюция и происхождение сложности
Назад: Глава 1 Что такое жизнь?
Дальше: Часть II О жизни
Глава 2
Что значит жить?
Они хладнокровные и расчетливые убийцы. Они совершенствовали свои навыки много миллионов поколений. Они перемещаются по организму, с легкостью обманывая иммунную систему. Распознавая и связывая белки на поверхности клеток, они силой или обманом получают доступ к сокровенному содержимому. Они могут безнаказанно угнездиться в ядре клетки, даже в клеточном геноме, и таиться там долгие годы. В других случаях они приступают сразу к делу: подчиняют себе биохимические процессы клетки, заставляя ее производить тысячи таких же убийц, облаченных в маскировочные костюмы из белков и липидов. Когда множество убийц-клонов выходит наружу, каждый из них готов внедриться в новую клетку и запустить цикл разрушения. Они способны убить человека, разрушая одну клетку тела за другой; могут вызывать эпидемии; способны в одночасье сделать безжизненными сотни миль океанских вод. При этом большинство биологов даже не считает их живыми. Впрочем, вирусам нет дела до того, как именно их классифицируют.
Почему вирусы можно считать неживыми? Потому что у них нет собственного метаболизма, их единственный источник энергии – ресурсы клетки-хозяина. Является ли метаболическая активность неотъемлемым признаком жизни? Принято считать, что да. Но почему? Среда обитания вируса – это внутреннее содержимое клетки, он пользуется ее ресурсами для самовоспроизведения. Но ведь мы и сами, по сути, делаем то же самое – поедаем других животных и растения, дышим кислородом. Если человек отгородится от окружающей среды – например надев на голову полиэтиленовый пакет, – то через несколько минут погибнет. Так что мы паразитируем, как и вирусы. То же самое относится к растениям. Растения необходимы нам так же, как и мы – им. Чтобы фотосинтезировать и расти, им нужны солнечный свет, вода и углекислый газ (CO2). Растения не способны расти в отсутствие CO2, в темных пещерах и безводных пустынях. Они не испытывают недостатка в CO2 благодаря животным, грибам и бактериям, которые непрерывно разлагают органику, в конечном счете превращая ее в атмосферный CO2. Кроме того, мы обогащаем атмосферу углекислым газом, сжигая ископаемое топливо. Хотя это может привести к ужасным последствиям для планеты, для растений это благо: чем больше СО2, тем быстрее они растут. Так что растения паразитируют, как и мы, на окружающей среде.
Увиденные с этой точки зрения растения и животные отличаются от вирусов лишь тем, что живут в несколько менее питательной среде. Вирусы кормятся внутренностями клеток, а в клетке сытнее и уютнее, чем в утробе матери: там есть почти все, что только можно пожелать. Поэтому вирусы могут позволить себе вступить на путь радикального упрощения и стать тем, что Питер Медавар назвал “дурной вестью в белковом конверте” (именно из-за того, что среда обитания вирусов настолько удобна). Другая крайность – это растения, способные жить почти везде, где есть вода, свет и воздух. Им пришлось приобрести чрезвычайно сложное внутреннее строение для того, чтобы выживать в столь суровых условиях. С точки зрения биохимии, растения в прямом смысле способны добыть из воздуха все, что им нужно. Мы с вами где-то посередине. Кроме питательных веществ, в нашей пище должны присутствовать некоторые витамины, без которых у нас развиваются опасные болезни, например цинга. Мы не способны самостоятельно производить витамины из их простых предшественников, поскольку утратили соответствующие предковые биохимические процессы. Без внешнего источника витаминов мы оказались бы в положении вируса, который не нашел клетку-хозяина.
Так что все организмы зависимы от среды обитания. Вопрос лишь в том, насколько сильна эта зависимость. Даже самые простые вирусы превосходят по сложности мобильные генетические элементы, например ретротранспозоны – “прыгающие гены”. Мобильные генетические элементы лишь распространяют свои копии по всему геному, никогда не покидая клетки-хозяина. Некоторые плазмиды – небольшие кольцевые молекулы ДНК, кодирующие небольшое число генов, независимые от остального генома, – способны непосредственно передаваться от одной бактерии к другой через специальные межклеточные контакты, не соприкасаясь с внешней средой. Вирусы, ретротранспозоны и плазмиды объединяет способность направлять ресурсы среды обитания на создание собственных копий. Так являются ли они живыми? Правильнее всего ответить так: пытаться провести границу между живым и неживым – бессмысленно. Они плавно переходят друг в друга. Большинство определений жизни относится к живым организмам и не учитывает их паразитов. Вот определение, которое дает НАСА: жизнь – это “самоподдерживающаяся химическая система, способная к дарвиновской эволюции”. Соответствуют ли вирусы этому определению? Скорее нет – хотя это зависит от того, что мы понимаем под “самоподдерживающаяся”. В любом случае это определение не подчеркивает неразрывность жизни и среды обитания. Среда воспринимается априори как нечто отдельное от жизни, но мы увидим, что это не так: жизненные формы и среда их обитания всегда связаны.
Что происходит с живыми организмами, отрезанными от среды обитания? Например, мы умираем, поскольку другого выбора у нас нет. Но это не единственно возможное развитие событий. Вирусы не разрушаются и не “умирают”, будучи отрезанными от ресурсов клетки-хозяина – для них это естественное положение вещей. В миллилитре морской воды на каждую бактерию приходится по десятку вирусов, готовых в любой момент “ожить”. По своей устойчивости вирусы напоминают бактериальные споры, которые способны на долгие годы впадать в анабиоз. Споры сохраняют жизнеспособность, пролежав тысячи лет в вечной мерзлоте, они выживают даже в открытом космосе. При этом у них останавливается метаболизм. Семена растений и некоторые животные, например тихоходки, также способны (без пищи и воды) выдерживать экстремальные условия – и полное высушивание, и радиацию, в тысячи раз превышающую летальную дозу для человека, и давление в океанских глубинах, и космический вакуум.
Почему споры бактерий, тела вирусов и тихоходок не рассыпаются в прах, как предписывает им второе начало термодинамики? Конечно, если прицельно выжечь их космическими лучами или переехать автобусом, им придет конец – но в целом они очень устойчивы, когда впадают в анабиоз. Это может прояснить для нас разницу между “жизнью” и тем, что значит “жить”. Хотя споры фактически не проявляют признаков жизни, большинство ученых все же относит их к живым организмам, поскольку они способны оживать. Буквально так: они могут ожить, следовательно, они не мертвы. Тогда я не вижу причин, почему мы не можем сказать то же самое о вирусах: попадая в подходящую среду, они также оживают. То же самое относится к тихоходкам. Термин “жизнь” относится к структуре организма (которая в основном определяется генами и эволюционным процессом), а “жить” – к взаимодействию организма со средой обитания. Мы знаем чрезвычайно много о том, как гены кодируют клеточные компоненты, но почти ничего – о том, как физические ограничения определяют структуру и ход эволюции клеток.
О структуре, энергии и энтропии
Второе начало термодинамики гласит, что энтропия – мера хаоса – всегда возрастает. Поэтому, на первый взгляд, странно, что вирусы и бактериальные споры так устойчивы. У энтропии, в отличие от жизни, есть строгое определение, и ее даже можно измерить – в Дж/(моль·К). Проведем мысленный эксперимент: возьмем спору, раздробим ее на молекулы и посмотрим, как изменится энтропия. Мы, конечно, ожидаем, что она должна возрасти. То, что было прекрасной упорядоченной системой, способной вернуться к жизни, попав в подходящие условия, превратилось в случайный нефункциональный набор обломков, энтропия которого по определению высока. Но все не так! Согласно измерениям биофизика Теда Бэттли, энтропия почти не изменится. Это объясняется тем, что мы должны учитывать не только изменение энтропии самой споры, но и изменение энтропии окружающей среды.
Спора состоит из взаимодействующих частиц, плотно прилегающих друг к другу. Энергия межмолекулярных взаимодействий отделяет липидные (то есть жировые) мембраны от воды. Если приготовить смесь липидов с водой, хорошенько ее потрясти и дать отстояться, липиды начнут самопроизвольно собираться в тонкие двухслойные мембраны, а те, в свою очередь, будут формировать пузырьки: наиболее стабильное состояние системы (рис. 7). По той же причине нефть в океане образует тонкую пленку, способную затянуть сотни квадратных километров водной поверхности и вызвать экологическую катастрофу. Нефть не смешивается с водой: из-за сил притяжения и отталкивания молекулы нефти и воды предпочитают взаимодействовать с себе подобными, а не друг с другом. Белки ведут себя похоже. Белки с большим количеством электрических зарядов хорошо растворяются в воде, а незаряженные белки гораздо легче взаимодействуют с жирами: такие белки называют гидрофобными, “боящимися воды”. При слипании молекул масла и при растворении заряженных белков в воде выделяется энергия: так система приходит в наиболее стабильное низкоэнергетическое состояние. Энергия выделяется в форме тепла, а оно не что иное, как беспорядочное движение молекул. Чем больше выделяется тепла, тем быстрее движутся молекулы, тем менее они упорядочены и тем выше энтропия. Следовательно, при разделении смеси воды и масла энтропия увеличивается – за счет выделяющегося тепла. Поэтому, если рассматривать общую энтропию системы, энтропия упорядоченной липидной мембраны, покрывающей клетку, выше энтропии случайной смеси молекул, хоть первая и выглядит более упорядоченной.

Рис. 7. Строение липидной мембраны.
Оригинальная жидкостно-мозаичная модель липидного бислоя, предложенная Сингером и Николсоном в 1972. Белки плавают в липидном море. Некоторые погружены частично, другие пронизывают мембрану насквозь. Липиды состоят из гидрофильных головок (обычно это фосфоглицерат) и гидрофобных хвостов. У бактерий и эукариот хвосты образованы жирными кислотами. Мембрана организована в виде бислоя: гидрофильные головки взаимодействуют с водным содержимым цитоплазмы и с внешней средой, а гидрофобные хвосты находятся внутри мембраны и соприкасаются лишь друг с другом. Это низкоэнергетическое, “комфортное” состояние: несмотря на то, что эта структура выглядит упорядоченной, формирование липидного бислоя повышает общую энтропию за счет выделения в окружающую среду энергии в виде тепла.
Если раздробить спору, общая энтропия мало изменится: хотя сама спора после дробления становится менее упорядоченной, энергия ее частей повышается. Жиры смешиваются с водой, в тесном соседстве оказываются не смешиваемые друг с другом белки. Поддержание этого физически “некомфортного” состояния энергозатратно. Физически комфортное состояние предполагает выделение энергии в виде тепла в окружающую среду, с системами в физически “некомфортном” состоянии дело обстоит наоборот. Такая система должна поглощать энергию из среды, охлаждая ее и понижая ее энтропию. Писатели в жанре хоррор точно выразили суть этого процесса в леденящих душу сюжетах. Призраки, полтергейсты и дементоры замораживают все вокруг, высасывая энергию для поддержания своего противоестественного существования.
Если при рассмотрении случая со спорой учесть все это, получается, что общая энтропия едва изменится. На молекулярном уровне структура полимеров соответствует локальному минимуму энергии. Избыток энергии выделяется в окружающую среду в виде тепла, повышая ее энтропию. В естественных условиях белки сворачиваются, принимая форму с максимально низким возможным уровнем энергии. Их гидрофобные части спрятаны глубоко внутри, как можно дальше от воды. Электрические заряды притягиваются или отталкиваются друг от друга: положительные заряды удерживаются на месте благодаря тому, что они уравновешены отрицательными, это стабилизирует трехмерную структуру белка. Таким образом, белки самопроизвольно сворачиваются, принимая определенную форму, пусть не всегда оптимальную. Прионы – это совершенно нормальные белки, способные спонтанно перестраиваться в квазикристаллические структуры, которые затем инициируют образование новых прионов. Общая энтропия при этом меняется незначительно. У белка может быть несколько стабильных форм, из которых лишь одна полезна для клетки, но в отношении энтропии эти формы мало различаются. Наверное, самое удивительное то, что общая энтропия беспорядочной смеси аминокислот (“строительных блоков” белков) очень незначительно отличается от общей энтропии аккуратно уложенного белка. Когда белок разворачивается, это возвращает его к состоянию, больше похожему на смесь аминокислот, и повышает его энтропию. Но при этом гидрофобные аминокислоты оказываются в воде, и белок, находясь в таком физически некомфортном состоянии, начинает высасывать энергию из внешней среды, охлаждая ее (можно назвать это “эффектом полтергейста”). Казалось бы, живые системы должны обладать низкой энтропией – ведь они более упорядочены, чем смесь аминокислот. Но эта идея не совсем верна.
Об этом и говорил Эрвин Шредингер, когда утверждал, что живое высасывает отрицательную энтропию из окружающей среды. Он имел в виду, что живое каким-то образом заимствует “упорядоченность” извне. Что ж, даже несмотря на то, что “бульон” из аминокислот может иметь такую же энтропию, как и белок с правильной укладкой, – из этих двух вариантов образование белка менее вероятно и потому требует затрат энергии.
Во-первых, аминокислоты в “бульоне” не будут самопроизвольно соединяться друг с другом. Белки – это цепочки соединенных аминокислот, однако сами по себе аминокислоты не реакционноспособны. Клеткам сначала нужно их активировать. Лишь после этого аминокислоты станут реагировать друг с другом, формируя цепь. При этом выделяется примерно столько же энергии, сколько было затрачено на активацию, и общая энтропия не изменяется. В процессе укладки белка энергия теряется в виде тепла, увеличивая энтропию окружающей среды. Таким образом, между стабильными в равной степени состояниями существует энергетический барьер. Он препятствует и формированию белков, и их распаду. Чтобы разложить белок на составляющие, понадобится энергия (и пищеварительные ферменты). Следует понимать, что склонность органических молекул к взаимодействию с образованием более крупных структур (белков, ДНК или мембран) не загадочней тенденции к формированию крупных кристаллов в остывающей лаве. При наличии достаточного количества реакционноспособных “строительных блоков” образование крупных структур приводит к наиболее стабильному состоянию. Вопрос в том, где взять такие “строительные блоки”.
Это подводит нас ко второй проблеме. Существование “бульона” из аминокислот, пусть активированных, в современных условиях вряд ли возможно: в конце концов он прореагирует с кислородом и превратится в смесь углекислого газа, азота, оксидов серы и паров воды. Иными словами, при образовании аминокислот затрачивается энергия, и эта же энергия выделяется при их разложении. Поэтому-то мы способны некоторое время жить без пищи, расщепляя белки наших мышц и используя их в качестве топлива. Эта энергия не извлекается из самого белка, а выделяется при “сжигании” аминокислот, входящих в его состав. Таким образом, семена, споры и вирусы не очень стабильны в современном мире, наполненном кислородом. Их компоненты будут медленно, но непрерывно окисляться. В итоге их структуры и функции окажутся нарушенными, и они не смогут вернуться к жизни, попав в подходящие условия. Так умирают семена. Но измените состав атмосферы, уберите из нее кислород – и они останутся нетленными. Из-за того, что живые организмы не находятся в равновесии с насыщенной кислородом средой, они склонны окисляться, если не защищать их специально. (Впрочем, в следующей главе мы увидим, что это не всегда так.)
В обычных условиях (в присутствии кислорода) образование аминокислот и других “строительных блоков”, например нуклеотидов, требует энергии. Чтобы объединять их в ДНК, белки и другие полимеры, также нужна энергия, несмотря на то, что разница в энтропии невелика. В этом и состоит жизнь: создание новых компонентов и их объединение, рост и размножение. Рост означает еще и активный транспорт материалов вовнутрь и наружу клетки. Все эти процессы нуждаются в непрерывном потоке энергии: Шредингер называл это “свободной энергией”. Вот уравнение, на которое он опирался. Это достаточно простое уравнение связывает энтропию и тепло со свободной энергией:
∆G = ∆H – T∆S.
В чем здесь смысл? Греческая буква дельта (∆) означает изменение. ∆G – это изменение свободной энергии Гиббса (названной так в честь великого американского физика-затворника XIX века Дж. Уилларда Гиббса), которая может “свободно” обеспечивать в клетке механическую работу – например мышечное сокращение. ∆H – это тепло, которое выделяется в окружающую среду и повышает ее энтропию. Реакция, в ходе которой во внешнюю среду выделяется тепло, должна вызывать охлаждение самой системы, потому что после реакции в ней становится меньше энергии. Таким образом, если из системы уходит тепло, то ∆H системы приобретает отрицательный знак. T – это температура. Вклад теплового эффекта в разных температурных условиях отличается. Высвобождение фиксированного количества тепла в холодную среду имеет больший эффект, чем выделение такого же количества тепла в теплую среду. Наконец, ∆S – это изменение энтропии системы. Оно имеет отрицательный знак, если энтропия системы снижается – и положительный, если энтропия повышается и система становится более хаотичной.
Свободная энергия ∆G любой самопроизвольной реакции отрицательна. Это верно для всех реакций, обеспечивающих жизнь. То есть реакция будет самопроизвольно идти, только если ∆G отрицательна. Из уравнения следует, что ∆G принимает отрицательные значения (реакция протекает самопроизвольно) либо когда в системе увеличивается энтропия, либо когда система теряет тепло, либо то и другое вместе. Это значит, что локальная энтропия может снижаться до тех пор, пока ∆H это компенсирует (это означает выделение большого количества тепла в окружающее пространство). А главное вот что: чтобы обеспечивать рост и размножение, некоторые реакции должны непрерывно выделять тепло в окружающую среду, разупорядочивая ее. Вспомните о звездах. Они платят за свое упорядоченное существование, отдавая Вселенной огромную энергию. Мы и сами платим за свое непрерывное существование теплом, которое высвобождается в результате непрерывно протекающей реакции дыхания. Мы постоянно окисляем пищу кислородом, нагревая окружающее пространство. Потеря тепла – не побочный эффект, а совершенно необходимый для поддержания жизни процесс. Чем больше потеря тепла, тем выше доступный уровень сложности.
Все процессы в живой клетке самопроизвольны. Они запустятся, если дать им правильную стартовую точку. Их ∆G всегда отрицательна. В отношении энергии это похоже на катание с горы. Но это означает, что стартовая точка должна находиться очень высоко. Чтобы получился белок, должно произойти событие с низкой вероятностью: в одном месте должно скопиться достаточное количество активированных аминокислот. Тогда они начнут объединяться в цепи, формируя белок с определенной укладкой. Выделение энергии при этом процессе будет повышать энтропию окружающей среды. Даже активированные аминокислоты будут образовываться самопроизвольно, если есть достаточное количество подходящих реакционноспособных предшественников. И эти предшественники также образуются самопроизвольно, если находятся в среде с высокой реакционной способностью. Таким образом, энергия для роста появляется из высокоэнергетичных компонентов среды, которые непрерывно поступают в живые клетки (в нашем случае в форме пищи и кислорода, в случае растений – в виде света). Живые клетки используют этот непрерывный поток энергии, чтобы, сопротивляясь распаду, расти. Они делают это при помощи хитроумных структур, частично программируемых генами. Но какими бы ни были эти структуры, они сами – результат роста и размножения, естественного отбора и эволюции, и ни один из этих процессов невозможен в отсутствие непрерывного притока энергии извне.
Удивительно узкий спектр форм биологической энергии
Организмам требуется неимоверно много энергии, чтобы жить. Энергетическая “валюта”, которая в ходу у клеток, называется аденозинтрифосфат (АТФ). АТФ работает как монета, которую кидают в игровой автомат. Она заставляет автомат сработать один раз, после чего он выключается. В случае АТФ роль такой машины, как правило, играет белок. АТФ обеспечивает переход из одной стабильной конформации в другую – как бы щелкает переключателем. Чтобы вернуть белок в исходное состояние, требуется снова затратить АТФ – как и в ситуации с автоматом: чтобы его запустить, придется скормить еще одну монетку. Представьте живую клетку в виде огромной галереи игровых автоматов, где работают белковые машины, приводимые в действие монетками-АТФ. Одна клетка ежесекундно расходует около 10 млн молекул АТФ! В человеческом теле около 40 триллионов клеток, а ежедневный суммарный оборот АТФ составляет 60–100 килограммов (это примерно соответствует массе целого организма). В действительности в нашем теле содержится около 60 граммов АТФ, из чего следует, что каждая молекула АТФ перезаряжается один или два раза в минуту.
Что это значит – перезаряжается? При расщеплении АТФ выделяется свободная энергия, которая делает ∆G конформационного перехода отрицательной. АТФ, как правило, распадается на два неравных фрагмента: АДФ (аденозиндифосфат) и неорганический фосфат (PO43-) – тот самый фосфат, который входит в состав удобрений и обозначается Фн. Чтобы вновь получить АТФ из АДФ и фосфата, нужно затратить энергию. Для этого используется энергия, которая высвобождается в ходе окисления питательных веществ кислородом. Так это и происходит. Этот бесконечный цикл можно записать в виде простой формулы:
АДФ + Фн + энергия ↔ АТФ
Так устроены не только мы, люди. Бактерии, например Escherichia coli, способны делиться каждые 20 минут. Чтобы расти, E. coli тратит на каждое деление около 50 млрд АТФ. По массе это в 50–100 раз больше массы отдельной клетки и четырехкратно превосходит наш собственный темп синтеза АТФ. Переведите эти цифры в единицы мощности – ватты – и увидите, что это просто невероятные величины. Мы используем примерно 2 милливатта энергии на 1 г тела – 130 Вт на одного среднего человека весом 65 кг (это чуть больше, чем стандартная лампочка в 100 Вт). В пересчете на 1 г это в 10 тыс. раз больше, чем у Солнца (небольшая часть которого в настоящий момент подвергается ядерному распаду). Жизнь больше похожа на ракету, чем на свечу.
Теоретически жизнь не представляет собой ничего мистического: она не противоречит ни одному закону природы. Ежесекундно клетки пропускают сквозь себя астрономическое количество энергии, но на Землю ее поступает во много раз больше – в виде солнечного света (потому что Солнце не в пример крупнее, хотя его мощность в пересчете на грамм вещества меньше). Поскольку доля этой энергии доступна для обеспечения биохимических процессов, можно подумать, что жизнь может быть реализована почти любым возможным образом. Как и в случае с генетической информацией, по-видимому, нет никаких фундаментальных ограничений касательно того, как можно использовать энергию – лишь бы она имелась в достаточном количестве. Тем удивительнее, что жизнь на Земле оказывается очень стесненной.
Есть два неожиданных аспекта использования энергии живыми организмами. Во-первых, клетки получают энергию за счет химических реакций лишь одного типа: окислительно-восстановительных. (Или – редокс-реакций: от англ. reduction – восстановление и oxidation – окисление.) Это просто перенос электронов от донора к акцептору. Когда донор отдает электроны, говорят, что он окисляется. Именно это происходит с такими веществами, как железо, когда они реагируют с кислородом: железо отдает электроны кислороду, окисляясь и превращаясь в ржавчину. Про вещество, которое принимает электроны (в этом случае кислород), говорят, что оно восстанавливается. В ходе дыхания или горения кислород (O2) восстанавливается до воды (H2O), так как каждый атом кислорода принимает два электрона (становится O2-) и два протона, которые компенсируют заряд. Реакция идет, потому что в процессе высвобождается энергия в виде тепла и повышается энтропия. Все химические реакции в конечном счете повышают температуру среды и уменьшают энергию самой системы. Реакция железа или питательных веществ с кислородом служит отличным примером этого правила. В ходе них выделяется большое количество энергии (как если бы они горели в огне). При дыхании часть энергии, выделяющейся в реакции, запасается в форме АТФ, пусть и ненадолго: до тех пор, пока АТФ не распадется снова. Расщепляясь, АТФ отдает в форме тепла оставшуюся энергию, которая заключена в связи АДФ – Фн. По сути, дыхание и горение – это одно и то же, но в пламени все сгорает моментально, а в ходе дыхания – несколько медленней. Эту небольшую задержку мы и называем жизнью.
Из-за того, что электроны и протоны обычно (но не всегда) объединяются друг с другом, восстановление иногда определяют как перенос атома водорода. Но чтобы разобраться в окислительно-восстановительных процессах, для начала следует сосредоточиться на электронах. Последовательность окислительно-восстановительных реакций сводится к путешествию электрона по цепи связанных друг с другом переносчиков. (Не слишком отличается от течения тока по проводам.) Именно это происходит при дыхании. Электроны от питательных веществ переходят на кислород не сразу (как при горении, когда энергия выделяется вся и сразу), а в несколько стадий, прыгая с одного переносчика на другой, будто с кочки на кочку. Обычно “кочками” служат ионы железа (Fe3+), встроенные в белки дыхательной цепи. Как правило, ион железа входит в состав неорганической кристаллической структуры, которая называется железосерным кластером (рис. 8). С одного кластера электрон перепрыгивает на другой, очень похожий, но с чуть более высоким сродством к электрону (более “жадного”). Когда электрон передается от одного кластера к другому, каждый раз сначала происходит восстановление (принимая электрон, Fe3+ восстанавливается до Fe2+), а затем окисление (потеря электрона и обратный переход в Fe3+). Наконец, совершив пятнадцать или больше прыжков, электрон достигает кислорода. На первый взгляд, у фотосинтеза у растений и дыхания у животных мало общего, однако в главном они совпадают. В основе обоих процессов лежит перенос электрона по “дыхательным цепям”. Почему? Жизнь могла бы существовать за счет тепловой или механической энергии, радиоактивного или ультрафиолетового излучения, или электрических разрядов. Число вариантов ограничено лишь вашим воображением. Но нет: все живое существует благодаря окислительно-восстановительным реакциям, которые происходят на удивительно сходных дыхательных цепях.
Второй неожиданный аспект использования энергии живыми организмами – это хитроумный механизм хранения энергии в химических связях АТФ. Живые организмы синтезируют АТФ не непосредственно, а путем создания протонных градиентов на тонких мембранах. Вскоре мы дойдем до объяснения, что это означает и как работает. А пока вспомним, что о существовании такого странного механизма никто долго и помыслить не мог (по словам молекулярного биолога Лесли Оргела, это “самая парадоксальная идея со времен Дарвина”). На сегодняшний день до мельчайших деталей изучены молекулярные механизмы создания и поддержания протонных градиентов. Мы знаем, что все живое на Земле использует протонные градиенты – это такая же неотъемлемая часть жизни, как ДНК. Но и теперь мы почти ничего не знаем о том, как возник биологический механизм генерации энергии. Какими бы ни были причины – жизнь, похоже, использует поразительно ограниченный и довольно странный набор из всех возможных энергетических механизмов. Каприз истории? Или эти способы настолько лучше прочих, что в конце концов лишь они остались в употреблении? Или же (а вот это интересней) мы имеем дело с единственным возможным вариантом?
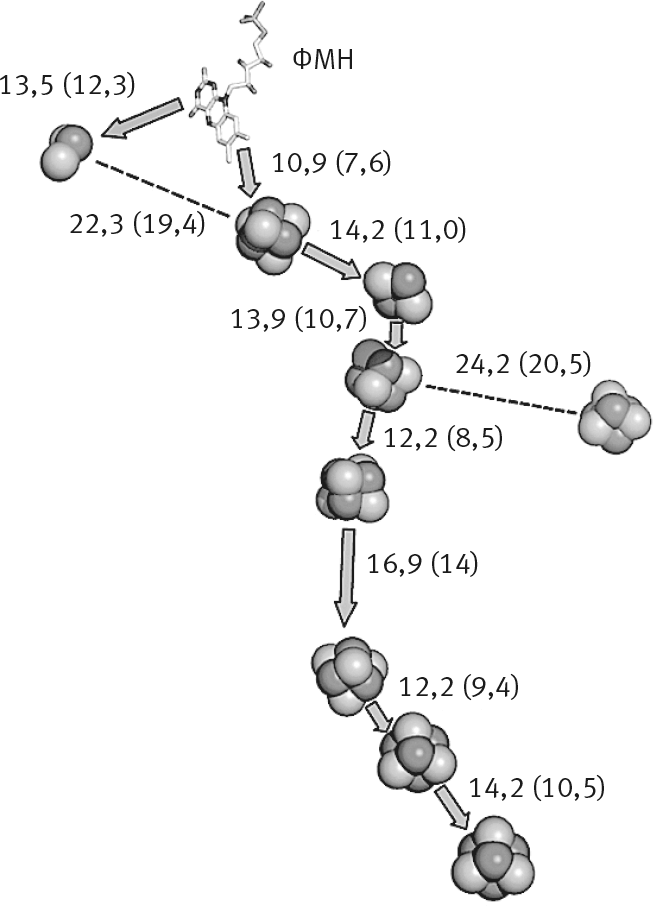

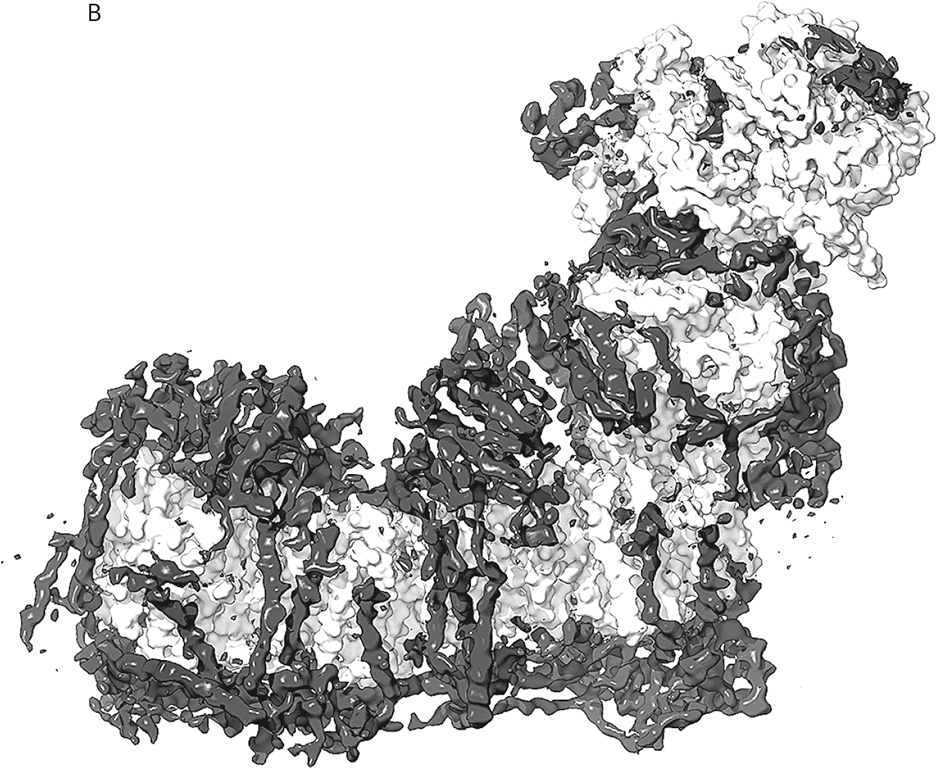
Рис. 8. Дыхательный комплекс I.
А. Железосерные кластеры расположены на более или менее одинаковом расстоянии друг от друга (14 ангстрем или меньше). Электроны перескакивают между кластерами путем квантового туннелирования в указанном стрелками направлении. Цифрами обозначено расстояние (в ангстремах) между окислительно-восстановительными центрами (кластерами). Цифры в скобках указывают расстояние от одного края до другого.
Б. Общий вид структуры бактериального комплекса I. Это изображение получено Лео Сазановым при помощи рентгеноструктурного анализа. Вертикальная “рука” переносит электроны от ФМН – места вхождения электронов в дыхательную цепь – на коэнзим Q (убихинон), который перемещает электрон на следующий белковый комплекс. Расположение железосерных кластеров в белке можно увидеть на рисунке А.
В. Комплекс I у млекопитающих, состоящий из тех же субъединиц, что и бактериальный, но частично скрытый под 30 дополнительными субъединицами. (Здесь они показаны как темные тени.) Это изображение получено Джуди Херст при помощи электронной криомикроскопии.
Это прямо сейчас происходит у вас внутри. Представьте, что вы тайно проникли внутрь собственной клетки: скажем, в клетку сердечной мышечной ткани. Она ритмично сокращается благодаря молекулам АТФ, выходящим из множества крупных митохондрий – энергетических станций клетки. А теперь вообразите, что вы уменьшились до размера молекулы АТФ и просочились в белковую пору во внешней мембране митохондрии. Вы в тесном пространстве, похожем на машинное отделение корабля, полном, насколько хватает взгляда, белковых механизмов. Внизу мельтешат сотни маленьких шариков. Они вылетают из белковых машин и через несколько миллисекунд исчезают, а потом появляются новые. Это протоны: положительно заряженные ядра атомов водорода. Все так и пляшет перед глазами. Теперь проберемся сквозь одну из белковых машин в матрикс митохондрии. Там взору открывается потрясающий вид. Вокруг – пещеристое пространство, мягкие стены так и ходят ходуном, а из них торчат гигантские клацающие машины, из которых тянутся нити, как от веретен. Осторожно, берегите голову! Огромные белковые комплексы, глубоко утопленные в стены, лениво переплывают с места на место, как по волнам, но их части движутся с невероятной скоростью. Некоторые ходят ходуном вверх-вниз так быстро, что глаз не может уследить за ними: как поршень парового двигателя. Другие вертятся вокруг своей оси, как пропеллеры, грозя в любой момент оторваться и улететь. Десятки тысяч двигателей неистово жужжат со всех сторон.
Мы глубоко внутри митохондрии, в термодинамическом эпицентре клетки, где осуществляется клеточное дыхание. Водород отрывается от продуктов молекулярного переваривания поглощенной нами пищи и попадает внутрь первого и крупнейшего дыхательного комплекса – комплекса I. Он состоит из 45 белков, и каждый – это цепь из нескольких сотен аминокислот. Вы помните, что вы размером с АТФ? Так вот, комплекс I выглядит как подвижная машина размером с небоскреб, живущая по собственным законам, приводящая в трепет своей сложностью. Электроны отделяются от протонов, попадают в пасть этого огромного комплекса и засасываются внутрь. Далее их путь пролегает глубоко в мембране, и, наконец, они извергаются наружу. Но на этом путь не заканчивается – им приходится еще пройти два огромных белковых комплекса. Все комплексы составляют дыхательную цепь. Каждый имеет несколько окислительно-восстановительных центров (в комплексе I их около 9), в которых электроны на короткое время задерживаются, прыгая с одного центра на другой (рис. 8). На самом деле “прыжки” – скорее туннелирование, некая разновидность “квантовой магии”, благодаря которой электронам удается телепортироваться между центрами: они стремительно пропадают и возникают в другом месте в соответствии с законами квантовой неопределенности. А возникают они, как правило, на следующем по ходу окислительно-восстановительном центре, если только он не слишком далеко. Здесь расстояния измеряются в ангстремах (Å). Один ангстрем примерно соответствует размеру атома. Если расстояние между окислительно-восстановительными центрами – около 14 Å и каждый следующий центр имеет несколько более высокое сродство к электрону, чем предыдущий, то электроны будут прыгать по цепочке, как по кочкам на болоте. Электроны проходят через три гигантских дыхательных комплекса, не замечая их – как и вы не обращали бы особого внимания на болото, прыгая с кочки на кочку. Они стремятся вперед, к кислороду, который притягивает электроны с огромной силой. Это не воздействие на расстоянии – они оказываются на кислороде просто потому, что вероятность нахождения там для них выше, чем в любом другом месте. Это похоже на провод с изоляцией из белков и липидов, по которому идет ток электронов от питательного вещества к кислороду. Добро пожаловать в дыхательную цепь!
Все, что здесь есть, приводится в движение электрическим током. Электроны прыгают вперед, стремясь к кислороду, безразличные к лязгу машин, возвышающихся тут и там, как станки-качалки над нефтяными скважинами. Однако огромные белковые комплексы полны развилок – стрелок, которые могут быть переведены. Когда в окислительно-восстановительном центре белка находится электрон, белок имеет определенную структуру, а когда электрон уходит, структура меняется. Часть белка меняет свое положение, отрицательный заряд уходит, возникает положительный, перестраиваются целые сети слабых связей, и белковая махина за доли секунды меняет свою конформацию. Небольшие изменения в одном месте белка могут повлечь открытие канала в другом месте. Но прибывает другой электрон, и белковая машина возвращается к предыдущему состоянию. Этот процесс повторяется десятки раз в секунду. Структура дыхательных комплексов уже изучена очень подробно, с точностью до нескольких ангстрем, почти в атомном разрешении. Мы знаем, как протоны связываются с иммобилизованными молекулами воды, которые, в свою очередь, удерживаются на месте благодаря зарядам белка. Мы знаем, как молекулы воды смещаются, когда изменяется состояние каналов, и как протоны переходят с одной молекулы воды на другую через динамические мостики, быстро возникающие и исчезающие. Нам известны все превратности их тернистого пути через белок, который сразу после прохождения протона закрывается, предотвращая его обратное движение. Прямо как в приключениях Индианы Джонса, только вместо Храма Судьбы – Белок Судьбы. Эта огромная, очень сложная и подвижная машинерия служит единственной цели: она обеспечивает перемещение протонов с одной стороны мембраны на другую.
На каждую пару электронов, проходящую через первый комплекс дыхательной цепи, приходится четыре протона, которые перебрасываются через мембрану. Затем пара электронов переходит на второй комплекс (вообще-то он называется комплексом III, а комплекс II – это альтернативная точка входа электронов), который переправляет сквозь мембрану еще четыре протона. В недрах последнего грандиозного дыхательного комплекса электроны, сливаясь с кислородом, уходят в нирвану (но не раньше, чем еще два протона переместятся через мембрану). На каждую пару электронов, оторванных от пищи, приходится десять протонов, переправленных на другую сторону мембраны – вот так (рис. 9). Чуть менее половины энергии, выделяющейся в процессе движения электрона к кислороду, сохраняется в форме протонного градиента. Все эти ухищрения, все эти огромные белковые структуры нужны лишь для того, чтобы перекачивать протоны через внутреннюю митохондриальную мембрану. В одной митохондрии десятки тысяч дыхательных комплексов каждого вида. Одна клетка содержит сотни, даже тысячи митохондрий. Ваши 40 млрд клеток несут по меньшей мере квадриллион митохондрий, а общая площадь поверхности их складчатых мембран составляет около 14 тыс. м2 (примерно четыре футбольных поля). Предназначение этих мембран – транспорт протонов. За секунду в нашем теле перекачивается более 1021 протонов: во Вселенной примерно столько же звезд.

Рис. 9. Принцип работы митохондрий.
А. Электронная микрофотография митохондрий. Заметны складки внутренней мембраны (кристы), где осуществляется клеточное дыхание.
Б. Схема дыхательной цепи, на которой показаны три встроенных во внутреннюю мембрану главных белковых комплекса. Электроны (e–) входят в цепь слева и передаются на кислород через цепочку из трех больших белковых комплексов. Сначала электроны передаются на комплекс I (рис. 8), затем на комплекс III, а следом – на комплекс IV. Комплекс II (не показан) – это отдельная точка входа электронов в дыхательную цепь. Он передает электроны сразу на комплекс III. Маленькие кружки в толще мембраны – убихиноны, переносящие электроны от комплексов I и II к комплексу III. Белок, заякоренный на поверхности мембраны – цитохром c, переносящий электроны от комплекса III к комплексу IV. Направление потока электронов на кислород показано стрелкой. В ходе транспорта электронов выделяется энергия, за счет которой дыхательные комплексы I, III и IV перебрасывают протоны через мембрану (комплекс II передает электроны, но протоны не перекачивает). На каждую пару электронов, прошедших через ЭТЦ к кислороду, комплексы I и III перекачивают по четыре протона, комплекс IV – два протона. Протоны возвращаются в матрикс через АТФ-синтазу, и за счет выделяющейся энергии происходит синтез АТФ из АДФ и Фн(вправойчастирисунка).
Но это лишь половина их работы. Вторая половина – синтезировать АТФ, используя накопленную энергию. Внутренняя мембрана митохондрий почти непроницаема для протонов – они могут проходить только через особые динамические каналы, которые, пропустив протон, захлопываются. Протоны крошечные (по сути, это ядра атомов водорода, самого малого из атомов), поэтому удержать их – нелегкая задача. Протоны невероятно быстро перемещаются в водной среде, перепрыгивая с молекулы на молекулу, поэтому митохондриальная мембрана должна быть совершенно непроницаема для воды. Кроме того, протоны заряжены – они несут единичный положительный заряд. Поэтому перекачка протонов через непроницаемую для них мембрану приводит, во-первых, к тому, что возникает разность концентраций протонов между двумя сторонами мембраны. Во-вторых, на мембране появляется разность зарядов, потому что снаружи положительных зарядов становится больше, чем внутри. Иными словами, на мембране возникает разность электрохимических потенциалов в 150–200 милливольт. Из-за того, что мембрана очень тонкая (около 6 нанометров), внутри нее появляется чрезвычайно высокая напряженность электрического поля. Если вы снова уменьшитесь до размера молекулы АТФ и попробуете приблизиться к мембране, то сможете в этом убедиться: напряженность там достигает 30 мегавольт на метр – в тысячу раз выше, чем в бытовой электросети. (Почти как у разряда молнии.)
Этот огромный электрический потенциал – протон-движущая сила – приводит в движение АТФ-синтазу: поражающую воображение белковую наномашину (рис. 10). АТФ-синтаза – самый настоящий роторный двигатель, в котором поток протонов вращает коленчатый вал, взаимодействующий с каталитической головкой. За счет энергии этого взаимодействия происходит синтез АТФ. АТФ-синтаза похожа на турбину гидроэлектростанции: мембрана, как плотина, сдерживает напор протонов, которым ничего не остается, как хлынуть через турбину, вращая ротор. Это не поэтическое видение, а точное описание. Впрочем, даже оно не передает удивительной сложности белкового двигателя. Например, до сих пор не вполне ясно, как протоны связываются с погруженным в мембрану участком C-кольца; какие электростатические взаимодействия вращают это кольцо (строго в одном направлении); как кольцо сообщает вращение ротору, вызывая конформационные изменения в каталитической головке, а также как двигаются субъединицы этой головки, захватывая молекулы АДФ, Фн и спрессовывая их в молекулу АТФ. Эта наномашина с высочайшим уровнем точности столь совершенна, что ее работа сродни магии. Чем больше мы узнаем о ней, тем больше она удивляет. Некоторые даже видят в ее совершенстве доказательство существования Бога. Я считаю “чудо” результатом естественного отбора. В любом случае это, несомненно, одна из самых удивительных природных машин.
На каждые десять протонов, прошедших через АТФ-синтазу, ротор делает один полный оборот, и в матрикс высвобождается три новообразованных молекулы АТФ. Ротор может совершать более сотни оборотов в секунду. АТФ называют энергетической “валютой” жизни. АТФ-синтаза и протон-движущая сила – это также универсальные и консервативные признаки жизни. АТФ-синтаза имеется у всех бактерий, архей и эукариот (то есть во всех трех доменах жизни), за исключением небольшого числа организмов, полностью перешедших на брожение. Протонный градиент и АТФ-синтаза универсальны, как и генетический код. В моей книге АТФ-синтаза – это такой же символ жизни, как двойная спираль ДНК. Я надеюсь, что она станет таким символом и для вас.

Рис. 10. Структура АТФ-синтазы.
АТФ-синтаза – удивительный роторный двигатель, погруженный своим основанием в мембрану (внизу). Этот прекрасный рисунок Дэвида Гудселла выполнен с соблюдением пропорций, и мы можем оценить относительные размеры молекул АТФ и протонов в сравнении с белком и толщиной мембраны. Поток протонов, проходя через мембранную субъединицу (показана стрелкой), вращает встроенный в мембрану FО – ротор и прикрепленный к нему вал (стебелек). (Вращение показано стрелкой.) Вращение вала вызывает конформационные изменения в каталитической головке (субъединице F1), за счет которых осуществляется синтез АТФ из АДФ и фосфат-ионов. Сама головка не вращается, поскольку зафиксирована статором: торчащим слева жестким стержнем. Протоны изображены снизу от мембраны в форме ионов гидроксония (H3O+), то есть связанными с водой.
Главная загадка биологии
Концепцию протон-движущей силы предложил Питер Митчелл – один из самых тихих ученых-революционеров XX века. Я называю его “тихим” лишь из-за того, что область его научных изысканий – биоэнергетика – была и остается тихой заводью в бурлящем мире науки, завороженном величием ДНК. Повальное увлечение ДНК началось в 50-х годах ХХ века в Кембридже, с работ Крика и Уотсона. Митчелл был их современником. В 1978 году он также получил Нобелевскую премию, но его идеи были восприняты совсем не так легко, как идея двойной спирали, о которой Уотсон справедливо заметил, что она “настолько проста, что не могла не оказаться верной”. Идеи Митчелла были настолько непросты, что, казалось, идут вразрез со здравым смыслом. Сам по себе Митчелл был абсолютно невыносим, неутомим в споре и невероятно прекрасен (именно в этом порядке). В начале 60-х годов он из-за язвенной болезни желудка был вынужден уйти из Эдинбургского университета – вскоре после того, как опубликовал свою “хемиосмотическую теорию” (она была напечатана в “Нейчур”, как и знаменитая статья Уотсона и Крика). Термин “хемиосмос” Митчелл применил к транспорту протонов через мембрану. Примечательно, что он использовал греческое слово “осмотический” в исходном значении – буквально “проталкивающий” (чаще осмосом называют прохождение воды через полупроницаемую мембрану). Дыхательные комплексы в ходе окислительно-восстановительных реакций проталкивают протоны через тонкую мембрану против градиента концентрации.
За счет частных средств Митчелл за два года превратил в лабораторию старинный особняк неподалеку от Бодмина в Корнуолле и в 1965 году открыл там Глинновский институт. Следующие двадцать лет Митчелл и несколько других видных биоэнергетиков занимались проверкой хемиосмотической гипотезы. Взаимоотношения этих ученых не были простыми. Этот период вошел в историю биологии под названием войн из-за окислительного фосфорилирования (ox phos wars). Окислительное фосфорилирование – это механизм, сопрягающий передачу электронов на кислород с синтезом АТФ. Сейчас трудно представить, но факты, которым я посвятил несколько последних страниц, не были известны до 70-х годов. Многие из них до сих пор активно исследуются.
Почему идеи Митчелла вызвали такое недоверие? Отчасти потому, что они были совершенно неочевидными. То ли дело – структура ДНК, абсолютно логичная и приводящая в восторг своей красотой: две цепи служат друг для друга матрицами, а последовательность азотистых оснований кодирует аминокислотную последовательность белка. На этом фоне хемиосмотическая гипотеза смотрелась довольно дико, а в исполнении Митчелла ее вообще можно было принять за бред душевнобольного. Мы знаем, что жизнь, по сути, – это ряд химических реакций. Чтобы получить АТФ, нужно лишь перенести активированный фосфат с некоего интермедиата на АДФ. Реакционноспособных интермедиатов в клетке очень много, и задача заключалась в том, чтобы найти среди них нужный. Вернее, именно таким образом ученые рассуждали несколько десятков лет. А потом явился Митчелл. Он писал уравнения, которые никто не мог понять, утверждал, что дыхание не сводится к химическим процессам и что интермедиата, который так упорно ищут, вообще не существует, а механизм, сопрягающий транспорт электронов и синтез АТФ, в действительности представляет собой градиент протонов на непроницаемой для них мембране – протон-движущую силу. Неудивительно, что он приводил коллег в бешенство!
Это уже стало легендой, примером того, что наука может развиваться в абсолютно непредсказуемом направлении. В теории научных революций Томаса Куна это называется “сменой парадигм”. Сейчас, когда хемиосмос описан в любом учебнике биохимии, все считают его самим собой разумеющимся. Структуры всех компонентов дыхательной цепи были определены с атомным разрешением. За открытие структуры АТФ-синтазы Джон Уокер в 1997 году получил Нобелевскую премию. Определение структуры комплекса I было еще более сложной задачей. Знания углубляются, хотя со стороны это больше похоже на увязание в деталях. Кажется, что в биоэнергетике уже не может быть никаких революционных открытий, сопоставимых с открытием Митчелла. И это до смешного странно, поскольку сам Митчелл думал не о деталях процесса дыхания, а о другой, куда более простой и фундаментальной проблеме: как клеткам (он рассматривал бактерий) удается сохранять постоянство своей внутренней среды? С самого начала он считал, что организмы и среда их обитания неразрывно связаны друг с другом посредством мембран. Эта точка зрения – краеугольный камень моей книги. Митчелл как никто другой понимал, как важны были мембранные процессы для возникновения жизни и как важны они для нее сейчас. В 1957 году, за четыре года до опубликования хемиосмотической гипотезы, в Москве Митчелл прочитал лекцию, посвященную происхождению жизни. Я приведу отрывок из нее:
Я не могу рассматривать организм вне среды его обитания… Формально организм и среду обитания можно рассматривать как две равнозначные фазы, динамический контакт между которыми поддерживается мембранами, разграничивающими и связывающими их.
Эти рассуждения имеют более философский характер, чем выросшая из них хемиосмотическая гипотеза, но я считаю, что они заслуживают не меньшего внимания. Сейчас, сосредоточившись на молекулярной биологии, мы позабыли об идее, которой был одержим Митчелл: о мембране как посреднике между внешней и внутренней средами, о том, что Митчелл называл “векторной химией”, где направление в пространстве имеет решающее значение. Эта химия совсем не похожа на происходящее в пробирке, где все компоненты смешаны в растворе. Почти все формы жизни используют окислительно-восстановительные реакции для создания протонного градиента на мембране. Но с какой стати все устроено так? Если сейчас эти идеи не кажутся такими бредовыми, как казались в 60-х годах, то лишь потому, что мы привыкли к ним. Они успели покрыться благородной пылью и прочно обосновались в учебниках, так что никому не приходит в голову снова подвергнуть их сомнению. Сейчас мы знаем, что эти идеи оказались верны, но почему они верны? Этот вопрос сводится к двум пунктам: почему все живые клетки в качестве источника свободной энергии используют окислительно-восстановительные реакции, и – почему все клетки запасают эту энергию в форме протонных градиентов на мембране? Или: почему они используют для этого электроны с протонами?
Электроны и жизнь
Почему все живое на планете использует окислительно-восстановительные процессы? Этот вопрос, наверное, из самых простых. Все известные живые организмы сложены в основном из углерода, причем в частично восстановленной форме. В первом, очень грубом приближении (без учета относительно небольших количеств азота, фосфора и других элементов) “формулу” жизни можно записать так: CH2O. Предположим, что углерод исходно пребывает в форме двуокиси. В этом случае живой организм должен осуществлять перенос электронов и протонов на CO2 от водорода (H2) или от подобного ему вещества. В целом не имеет значения, где брать эти электроны: их источником может послужить вода (H2O), сероводород (H2S) или даже ионы железа (Fe2+). Важно, что электроны в итоге переходят на CO2. Подобные переходы и составляют предмет окислительно-восстановительной химии. Кстати, термин “частично восстановленная форма” означает, что углерод в ней восстановлен в меньшей степени, чем в метане.
Возможно ли существование неуглеродных форм жизни? Вообразить их возможно. Всем известно о роботах из металла или кремния, так что особенного в углероде? На самом деле – довольно много чего. Каждый атом углерода может образовать четыре прочные связи – они гораздо прочнее, чем у кремния, химического аналога углерода. Такие связи делают возможным существование множества длинноцепочечных молекул, самые важные из которых – белки, липиды, сахара и ДНК. Кремний не способен обеспечить такое химическое разнообразие. К тому же, в отличие от углерода, он не образует газообразные оксиды. Мне нравится представлять CO2 в виде кирпичика “Лего”. Его можно извлечь из воздуха и присоединить с его помощью один атом углерода к какой-нибудь молекуле. А если попробовать вместо этого оксиды кремния… Это как пытаться строить из песка. Мы, существа с высоким интеллектом, научились подчинять своим нуждам кремний и другие элементы, но трудно представить, как из кремния сама по себе могла бы появиться жизнь. Я не говорю, что существование кремниевых форм жизни в бесконечной Вселенной вовсе невозможно – кто знает! Но в плане вероятности и предсказуемости (а моя книга посвящена именно таким материям) это не слишком вероятно. Кроме того, что углерод гораздо лучше подходит по свойствам, его во Вселенной еще и гораздо больше. Таким образом, в первом приближении жизнь должна быть углеродной.
Но потребность в частично восстановленном углероде – лишь небольшая часть ответа на поставленный вопрос. У большинства современных организмов метаболизм углерода и энергетический метаболизм в значительной степени разделены. Объединяет их лишь АТФ и несколько других общих реакционноспособных интермедиатов, таких как тиоэфиры (из них наиболее важен ацетил-кофермент А). Однако эти интермедиаты не являются обязательными продуктами окислительно-восстановительных реакций: не все организмы их используют. Некоторые организмы существуют за счет брожения, хотя этот способ не является ни древним, ни энергетически выгодным. Впрочем, есть множество остроумных предположений, какой была в химическом отношении начальная точка развития жизни. Одна из самых популярных (и сомнительных) версий предлагает цианид, который мог образоваться из азота и метана под воздействием ультрафиолетового излучения. Можно ли считать это возможным? В предыдущей главе я упоминал, что кристаллы цирконов не содержат ни намека на то, что в древней атмосфере было много метана. Впрочем, на какой-либо другой планете такой сценарий вполне мог реализоваться. Но если развитие жизни из цианида возможно, то почему это не происходит сейчас? К этому вопросу мы обратимся ниже. (Я думаю, это маловероятно по другим причинам.)
Взглянем на проблему под другим углом: чем хороша окислительно-восстановительная химия дыхания? Похоже, у нее много положительных качеств. Рассмотрим процесс дыхания в более широком смысле, не ограничиваясь тем типом, которым пользуемся мы. Мы отрываем электроны от пищи и прогоняем их по дыхательным цепям к кислороду, но очень важно отметить, что и источники, и конечные акцепторы электронов бывают разными. Сжигание пищи в кислороде позволяет получить большой энергетический выход, но принцип, лежащий в основе дыхания, гораздо шире. Например, необязательно употреблять в пищу именно органику. И водород, и сероводород, и двухвалентное железо также могут выступать донорами электронов. Они способны отдавать свои электроны в дыхательную цепь при условии, что акцептор на другом ее конце будет окислителем достаточно сильным для того, чтобы обеспечить движение этих электронов. Это означает, что бактерии могут “поедать” скалы, минералы и нефтепродукты, используя, по сути, ту же белковую машинерию, которой при дыхании пользуемся мы. В следующий раз, когда увидите на бетонной стене цветное пятно, которым колония бактерий обозначила свое присутствие, – вспомните на секунду о том, что, какими бы странными ни казались эти существа, они живут, пользуясь теми же базовыми механизмами, что и мы.
На кислороде свет клином не сошелся. Многие другие окислители могут выполнять его функцию почти столь же хорошо – например нитрат или нитрит, сульфат или сульфит (список можно продолжить). Все эти окислители (они называются так потому, что, как и кислород, окисляют вещества) способны притягивать электроны из пищи или других источников. В каждом из этих случаев при переносе электронов от донора к акцептору выделяется энергия, которая затем запасается в связях АТФ. Перечисление всех известных пар доноров и акцепторов электронов – окислительно-восстановительных пар, которые используют бактерии и археи, заняло бы несколько страниц. Бактерии умеют не только “питаться” камнями, но еще и “дышать” ими. Эукариотические клетки в сравнении с ними выглядят довольно жалко. Одна-единственная бактерия по метаболическому многообразию не уступает всем эукариотам вместе взятым, включая растения, животных, водоросли, грибы и протисты.
Такая универсальность в использовании доноров и акцепторов обусловлена невысокой реакционноспособностью большинства из них. Ранее мы отметили, что все биохимические реакции происходят самопроизвольно и всегда должны осуществляться в активной среде. Однако если среда чересчур активна, реакции в ней будут идти неконтролируемо и свободной энергии для обеспечения биологических процессов не останется. Так, атмосфера не может содержать фтор – он бы немедленно прореагировал со всем, чем можно, и исчез бы. Но многие вещества могут накапливаться до концентраций, значительно превышающих термодинамически равновесные, потому что они очень медленно вступают в реакции. Кислород, лишь дай ему волю, бурно реагировал бы с органической материей, сжигая все на планете. Однако, к счастью, его молекулы стабильны, и это не дает реализоваться его разрушительному потенциалу: он мирно сосуществует с органикой. Метан и водород реагируют с кислородом еще более бурно (вспомните катастрофу дирижабля “Гинденбург”), но, опять же, наличие у этой реакции кинетического барьера означает, что эти газы могут очень долго сосуществовать в воздухе, находясь при этом в далеком от равновесия состоянии. Это относится и ко многим другим веществам – от сероводорода до нитрата. Их можно вынудить реагировать друг с другом (при этом будет выделяться огромное количество энергии, которая может быть использована живыми клетками), но без подходящего катализатора реакция не пойдет. Жизнь эксплуатирует эти энергетические барьеры и служит более мощным источником энтропии, чем другие процессы. На этом даже основаны некоторые определения, согласно которым жизнь – это генератор энтропии. Хотя жизнь существует именно благодаря наличию кинетических барьеров, ее суть в том, чтобы их преодолевать. Жизнь – это лазейка в энергетическом барьере.
Многие доноры и акцепторы электронов стабильны и растворимы, так что могут входить в клетку и выходить из нее, не причиняя ей вреда. Поэтому активную среду, необходимую в термодинамическом плане, можно безопасно поместить внутрь клетки, прямо под ее мембраны, на которых и осуществляются процессы дыхания. Поэтому окислительно-восстановительные процессы в качестве источника энергии гораздо удобнее, чем тепло, механической энергия, ультрафиолетовое излучение или электрические разряды. Минздрав подтверждает.
Те же самые процессы послужили основой фотосинтеза. Напомню, существует несколько его разновидностей. Во всех случаях энергия солнечного света (в форме фотонов) поглощается пигментом (обычно хлорофиллом), после чего его возбужденный электрон следует по цепи окислительно-восстановительных центров к акцептору (в данном случае это диоксид углерода). Пигмент, лишившийся электрона, благодарно принимает взамен утраченного другой, от ближайшего донора. Таким донором может выступать вода, сероводород или двухвалентный ион железа. Как и при дыхании, здесь не имеет значения, каким именно будет донор электронов. В “аноксигенных” формах фотосинтеза донорами выступают сероводород или железо, а в качестве побочных продуктов образуются отложения серы или ржавчина. При оксигенном фотосинтезе донор гораздо упрямее – это вода, а в виде отходов выделяется кислород. Но важно вот что: фотосинтез всех этих типов, очевидно, произошел от дыхания. И при дыхании, и при фотосинтезе используются одни и те же дыхательные белки, окислительно-восстановительные центры одних типов, один и тот же протонный градиент на мембране, все та же АТФ-синтаза. Единственное значительное отличие – приобретение пигмента хлорофилла, который тем не менее является близким аналогом гема, входящего в состав многих древних дыхательных белков. Энергия солнечного света изменила мир, но на молекулярном уровне она лишь заставляла электроны бежать быстрее по дыхательным цепям.
Огромное преимущество дыхания состоит в его универсальности. По сути, с помощью любой окислительно-восстановительной пары (донор и акцептор электронов) можно обеспечить движение электронов по дыхательной цепи. Специальные белки, которые отбирают электроны у аммония, немного отличаются от тех, что отбирают их у сероводорода: очень близкие вариации. Белки, передающие электроны на нитрат или нитрит, пусть и отличаются от тех белков, которые восстанавливают кислород, но также родственны им. Они настолько похожи, что один такой белок можно заменить другим, и все будет работать. Эти белки образуют общую “операционную” систему, и из них можно формировать разные наборы в соответствии со стоящими перед организмом задачами. И это не просто теоретические рассуждения: в природе такое встречается сплошь и рядом. В последние десятилетия выяснилось, что горизонтальный перенос генов (одна клетка передает другой гены в составе маленьких фрагментов ДНК – будто подкидывает подруге немного мелочи) широко распространен у бактерий и архей. Гены, кодирующие дыхательные белки, – из наиболее частых объектов горизонтального переноса. Вместе эти гены составляют, по выражению биохимика Вольфганга Ничке, “белковый окислительно-восстановительный конструктор”. Вы переселились в среду, где сероводород и кислород распространены одинаково широко – в какую-нибудь впадину на дне морском? Нет проблем. Просто обзаведитесь соответствующими генами, и они будут превосходно работать, сэр. Закончился кислород? Попробуйте нитрит, мадам! Не беспокойтесь: стоит вставить себе ген нитрит-редуктазы, и все будет в порядке!
Это говорит о том, что окислительно-восстановительные процессы должны быть важны для жизни в любом месте Вселенной. Можно представить и другие источники энергии, но, учитывая, что окислительно-восстановительные процессы необходимы для восстановления углерода, а у дыхания столько преимуществ, не удивительно, что жизнь на Земле существует именно за счет окислительно-восстановительных процессов. Но куда менее понятно, почему основой дыхания служит градиент протонов на мембранах. Дыхательные белки могут передаваться путем горизонтального переноса, взаимозаменяться и объединяться, потому что они составляют общую “операционную систему”, ядро которой – хемиосмотическое сопряжение. Но почему окислительно-восстановительные процессы должны быть связаны с протонными градиентами? Отсутствием вразумительного ответа на этот вопрос частично объясняется неприятие идей Митчелла и “войны” тех далеких лет. За последние полвека мы многое узнали о том, как живое использует протоны. Но пока не узнаем, почему оно их использует, мы не сможем предсказать многие свойства жизни на Земле – или где-то еще во Вселенной.
Главное – это протоны
Появление хемиосмотического сопряжения – большая загадка. Вся жизнь хемиосмотична, а значит, хемиосмотическое сопряжение возникло очень рано. Если бы оно появилось позднее, трудно объяснить, как и почему оно стало универсальным – почему протонные градиенты пришли на смену всему остальному. Такая универсальность встречается удивительно редко. Все живые организмы имеют общий генетический код (с некоторыми исключениями, подтверждающими правило). Некоторые основные информационные процессы также универсальны и консервативны – например образование РНК при транскрипции на матрице ДНК и синтез белка рибосомами на матрице этой РНК. Но отличия между бактериями и археями поразительны. Как вы помните, археи и бактерии – это два огромных домена прокариот. Внешне они почти неотличимы друг от друга, но биохимически и генетически значительно различаются.
Взять, например, репликацию ДНК. Казалось бы, она должна быть столь же универсальной, как и генетический код. Но, оказывается, черты этого процесса, включая большинство участвующих в нем ферментов, у бактерий и архей сильно различаются. Так же дело обстоит с клеточной стенкой – жесткой внешней оболочкой, которая защищает нежную клетку снаружи: ее химический состав у бактерий и архей абсолютно разный. Биохимические пути брожения также различны. Даже клеточные мембраны, необходимые для хемиосмотического сопряжения (а это основа мембранной биоэнергетики), у бактерий и архей различаются по химическому составу. Выходит, что и структура барьеров, отделяющих клетку от внешней среды, и репликация наследственного материала не являются глубоко консервативными. А ведь это едва ли не самое важное в жизни клеток! Лишь хемиосмотическое сопряжение универсально: сколь сильно ни различались бы организмы, его они используют всегда.
Различия между археями и бактериями действительно очень глубоки, поэтому их происхождение вызывает много вопросов. Если предположить, что их общие свойства унаследованы от общего предка, а различия появились независимо, каким должен был быть этот общий предок? Увы, о нем можно сказать очень мало. Мы можем получить лишь очень расплывчатое представление, каким он был: отчасти похожим на современную клетку, а в остальном… Каким же он был в остальном? Мы можем различить лишь смутный биохимический силуэт – известно только, что у него имелись транскрипция, трансляция с участием рибосом, АТФ-синтаза, отдельные фрагменты биосинтеза аминокислот. Этим общие признаки бактерий и архей исчерпываются, а вместе с ними и черты общего предка.
А как обстоит дело с мембранами? Мембранная биоэнергетика универсальна, мембраны – нет. Можно вообразить, что последний общий предок имел мембрану бактериального типа, а археи видоизменили ее, чтобы приспособиться (так, мембраны архей устойчивее при высоких температурах). На первый взгляд, идея выглядит правдоподобной, но есть две серьезные проблемы.
Во-первых, большинство архей не является гипертермофилами и обитает в умеренных условиях, где специфические мембранные липиды не предоставляют очевидного преимущества. И наоборот, многие бактерии счастливо живут в горячих источниках и их мембраны отлично справляются с высокими температурами. Археи и бактерии почти в любой среде обитают бок о бок и даже входят в симбиотические отношения. Зачем же одной из этих групп когда-то могло понадобиться менять все мембранные липиды – несмотря на связанные с этим процессом серьезные проблемы? Если такая трансформация мембран возможна, то почему мы не наблюдаем полного замещения мембранных липидов, когда клетки адаптируются к изменениям среды? Ведь это должно быть гораздо проще, чем заново изобретать новые липиды. Почему бы некоторым бактериям, живущим в горячих источниках, не обзавестись архейными липидами?
Во-вторых, главное различие мембран архей и бактерий напоминает случайность: бактерии используют один оптический изомер (зеркальную форму) глицерола, а археи – другой. Даже если археи действительно заменили все свои липиды, чтобы приспособиться к высоким температурам, сложно представить причину, в силу которой могло понадобиться менять один оптический изомер глицерола на другой. Это просто извращение. Ведь фермент, который производит левостороннюю форму глицерола, весьма далек от фермента, который участвует в образовании правосторонней формы. Чтобы перейти с одного изомера на другой, нужно сначала “изобрести” новый фермент (чтобы делать новый изомер), а затем настойчиво избавляться от старого (полностью функционального) фермента в каждой клетке, несмотря на то, что новый вариант не предоставляет никакого эволюционного преимущества. Мне не верится, что такое могло быть. Но если ни один тип липидов не заменялся на другой, то какой была мембрана у последнего общего предка? Она должна была сильно отличаться от всех современных мембран. Почему?
Сама идея, что хемиосмотическое сопряжение возникло рано, спорна. Одно из затруднений – очень высокая сложность механизма. Мы успели отдать должное гигантским дыхательным комплексам и АТФ-синтазе – поразительным молекулярным машинам с роторами и поршнями. Могли ли они появиться на заре эволюции, когда еще не было даже ДНК-репликации? Конечно нет! Такова первая мысль, но надо понимать, что этот ответ продиктован чувствами. АТФ-синтаза не намного сложнее рибосомы, а ведь никто не станет спорить, что рибосомы должны были возникнуть рано. Вторая проблема – сама мембрана. Даже если не задумываться о том, какого типа она была, вопрос о ранней сложности возникает и здесь. У современных клеток хемиосмотическое сопряжение работает лишь в том случае, если мембрана непроницаема для протонов. Но все эксперименты с реконструкцией древних мембран показывают, что они беспрепятственно пропускали протоны. Удерживать протоны снаружи – невероятно сложная задача, и проблема в том, что хемиосмотическое сопряжение, похоже, остается бесполезным без множества сложных белков, встроенных в непроницаемую для протонов мембрану. В этом и только в этом случае выполняет свою функцию хемиосмотическое сопряжение. Так в каком же, черт возьми, порядке возникли эти составляющие? Это проблема курицы и яйца. Какой смысл учиться перекачивать протоны, если нельзя воспользоваться градиентом? И зачем учиться использовать градиент, если вы не умеете его создавать? В гл. 4 я предлагаю возможное решение этой проблемы.
Я заканчиваю главу несколькими большими вопросами. Почему жизнь на Земле появилась так рано? Почему она на несколько миллиардов лет застыла на одном уровне морфологической сложности? Почему сложные эукариотические клетки за 4 млрд лет возникли лишь единожды? Почему у всех эукариот имеется целый ряд особенностей, которые никогда не встречаются у бактерий и архей – от наличия двух полов до старения? И почему все живое сохраняет энергию в форме протонных градиентов на мембранах? Как и когда начался этот процесс?
Я думаю, эти два ряда вопросов связаны. Ниже я докажу, что появление жизни на Земле инициировал природный протонный градиент, поэтому это должно было произойти в специфических условиях. На самом деле такие условия встречаются почти во всей Вселенной: горная порода, вода и углекислый газ (CO2). Я покажу, что хемиосмотическое сопряжение миллиарды лет удерживало эволюцию на прокариотическом уровне и лишь однажды, когда одна бактерия каким-то образом проникла в другую, жизнь вышла из энергетического застоя. Эндосимбиоз дал начало эукариотам, размеры генома которых выросли на порядки, предоставляя материал для морфологической сложности. Я докажу, что многие странные свойства эукариот обусловлены взаимоотношениями клетки-хозяина и ее эндосимбионтов, которые впоследствии стали митохондриями. Похоже, эволюция идет одними путями, которые пролегают между барьерами, одинаковыми во всей Вселенной. Не думаю, что прав во всем, но, надеюсь, общая картина верна – и тогда, возможно, из моих рассуждений вырастет новая биология, которая предскажет больше. Может быть, однажды мы сможем предсказать, какой должна быть жизнь в любом месте Вселенной, опираясь на химический состав космического пространства.
Назад: Глава 1 Что такое жизнь?
Дальше: Часть II О жизни

