Глава 18
Текущий ремонт
– Есть два типа женщин: с малыми запросами и с большими.– К какому же типу принадлежу я?– К самому худшему. Запросы у тебя большие, а ты думаешь, что маленькие.Цитата из фильма «Когда Гарри встретил Салли» (автор сценария – Нора Эфрон)
Учителя биологии любят играть со своими учениками в одну игру: они просят их дать определение жизни, придумать простой критерий того, является ли тот или иной объект живым или нет. В нее можно играть на всех ступенях обучения от начальной школы до аспирантуры и далее, и каждый раз этот вопрос порождает очень похожие споры (основная разница заключается в том, что аспиранты используют много умных слов, считая, что они придают их доводам убедительности).
Даже ученики начальной школы быстро отбрасывают такие ложные критерии, как способность двигаться, указывая на неподвижные живые организмы, например кораллы, и подвижные неживые объекты, например капли дождя. Нетрудно понять и ложность такого критерия, как реакция на стимулы: живые грибы не реагируют на прикосновение, а неживые мышеловки очень даже реагируют. Нередко определяющей характеристикой жизни называют способность к размножению. Об этом можно прочитать даже в учебниках биологии, хотя, казалось бы, их авторы должны были бы разобраться, что к чему. Несостоятельность этой идеи очевидна: если довести ее до логического завершения, то придется отнести к неживой природе красные кровяные клетки, мулов, рабочих муравьев и женщин после менопаузы. Более продвинутые студенты предлагают в качестве критерия способность к самоорганизации, но и это не панацея: некоторые неживые объекты, такие как кристаллы, ячейки конвекции, а также волновые структуры некоторых химических реакций (например, реакции Белоусова – Жаботинского), проявляют по крайней мере некоторые признаки самоорганизации.
Тем не менее одна универсальная особенность живого мира все-таки есть. Это способность живых организмов использовать полученную извне энергию для поддержания и обновления организма. В такой форме этот критерий предложил Пьер Луиджи Луизи, который основывался на более ранних формулировках Александра Опарина и Жака Моно (все эти ученые внесли огромный вклад в наше понимание феномена возникновения жизни). Необходимость в обновлении отчасти связана со случайными внешними повреждениями, которым подвержены все организмы, а отчасти – с непрочностью, по природе свойственной материалам нашего тела. Эта непрочность выражается в том, что, даже когда тело не подвергается ударам, укусам, ссадинам или ожогам, его молекулы лишь недолго выживают в химическом «котле» клетки и должны часто заменяться. Такая непрочность свойственна и рукотворным объектам, отдельные части которых приходится многократно заменять в течение срока службы. Разница в том, что такие объекты не способны сами создавать и встраивать в себя новые компоненты. Если в машине надо заменить тормозные колодки, мне нужно заказать их у поставщика и установить вручную. К сожалению, если я просто занесу необходимые материалы или новые колодки в гараж, моя машина не сможет сама заменить изношенные части, пока я буду заниматься своим делом. Эта способность к самоподдержанию и обновлению и представляет собой абсолютную разницу между живыми существами и неживыми машинами, как мы понимаем ее сегодня. Возможно, это различие будет валидно, даже если в один прекрасный день нам удастся построить самонастраивающуюся и самоподдерживающуюся машину, так как такую машину будет вполне резонно считать живым организмом.
Таким образом, конструирование тела, о котором шла речь в этой книге, – лишь прелюдия к его долгому самоподдержанию. Поскольку в ходе самоподдержания приходится опять делать те же самые вещи, которые были сделаны в ходе развития, естественно задать вопрос: повторяют ли механизмы «ремонта» механизмы развития или же в корне отличаются от них? Этот вопрос имеет далеко не только теоретический интерес. Четкий ответ на него важен, если мы хотим улучшить нашу способность восстанавливать наши тела или даже попробовать полностью победить старение.
Заменить изношенные компоненты машин можно практически в любом размерном масштабе. Иногда мелкие компоненты можно заменить по отдельности, а в других случаях приходится менять большую часть, содержащую сотни мелких компонентов. В моем стареньком «лендровере» мне приходилось менять как мелкие детали, например стопорные шайбы, так и многокомпонентные модули, такие как генератор и мотор вентилятора. Если у него по-прежнему будет в самый неподходящий момент вылетать третья передача, мне, вероятно, придется заменить всю коробку передач, состоящую из многих сотен деталей, потому что это гораздо проще, чем разбирать ее и чинить один испорченный вал. При этом новая коробка передач будет абсолютно такой же, как та, что была поставлена на автомобиль при сборке.
В организме млекопитающих замены многокомпонентных модулей не происходит. Поврежденные белки в клетках и поврежденные клетки в тканях замещаются белками и клетками, но это аналогично замене отдельных деталей машины. Ткани и органы никогда не заменяются целиком (разве что в дело вмешается хирург-трансплантолог). Вместо этого в них постоянно идет текущий ремонт. Это объясняется тремя основными причинами. Во-первых, многие органы возникают на эмбриональной стадии развития из тканей, которых в организме взрослого человека уже нет. Примерами структур, существующих лишь краткое время в жизни эмбриона, являются энтодермальная выстилка желточного мешка, из которого формируется кишечник, и сомиты, из которых развиваются позвонки, мышцы и внутренняя часть кожи. Создать новые версии таких органов и тканей невозможно просто потому, что структур, из которых они образовались, у взрослых организмов нет. Во-вторых, многие активно изнашивающиеся части тела, например верхние слои кожи и выстилка кишечника, существуют около недели, а затем заменяются. На этапе эмбрионального развития на их создание уходит гораздо больше времени, и взрослый организм просто не успел бы заменить старый орган новым. В-третьих, полная замена органов в сложившемся организме, с его многочисленными плотно упакованными частями, представляла бы непреодолимую геометрическую и логистическую трудность. Поэтому «ремонт» должен опираться на механизмы, в корне отличные от механизмов эмбрионального развития.
В принципе можно представить себе простой способ замены изношенных клеток – это пролиферации идентичных им соседних клеток. Назовем это «заменой равных равными». Такая замена может быть связана с определенными трудностями, например, клеткам, чтобы делиться, придется «впасть в детство», то есть отказаться от сложной формы и особого метаболизма, характерных для зрелого состояния. Тем не менее эти трудности, вероятно, преодолимы. В конце концов, клетке нужно всего лишь заменить себе подобную, и сложные механизмы дифференцировки, характерные для эмбрионального развития, ей не понадобятся. Все, что нужно, – это механизм, с помощью которого клетки могли бы понять, что соседние клетки нуждаются в замене.
При всей внешней простоте поддержание организма только за счет «замены равных равными» привело бы к серьезными проблемам у долгоживущих животных. Многие клетки находятся в агрессивной среде, где постоянно подвергаются воздействию повреждающих агентов. Слизистая кишечника, например, контактирует с желудочным соком, созданным специально для переваривания клеточных компонентов, а наружные слои кожи подвержены воздействию сухого воздуха, ультрафиолетового излучения, ветра и бактерий. Все клетки в органах, по сути, находятся «в одной лодке», и если вредное воздействие достигает такого уровня, что клетка умирает, то велика вероятность того, что и соседняя клетка сильно повреждена. После смены нескольких поколений отмерших клеток за счет пролиферации поврежденных «соседей» здоровой ткани останется немного.
Есть два способа, с помощью которых животное может справиться с этой проблемой, не отказываясь от идеи «замены равных равными». Один способ – это жить недолго и избегать вредных воздействий. Не исключено, что многие мелкие животные взяли на вооружение именно эту стратегию (хотя, насколько мне известно, вопрос о том, используют ли они только метод «замены равных равными», остается открытым). Второй способ – вложить много затрат в контроль за повреждениями и ремонтные механизмы в клетках. Такие механизмы, безусловно, существуют. Есть набор ферментов и других белков, которые могут обнаружить повреждения ДНК и восстановить ее; есть мембранные насосы, которые могут выводить небольшие количества токсинов из клеток; есть разрушающие белки ферменты, которые быстро разрушают клеточные белки, чтобы их можно было тут же заменить новыми. Если клетка вложит много энергии и ресурсов в эти системы, она останется здоровой в агрессивной среде, и «замена равными равных» будет более реальна. Проблема в том, что такие вложения потребуют слишком значительных (пищевых) ресурсов и могут оказаться не по средствам организму. И даже если ресурсов хватит, такие затраты на клеточную защиту, скорее всего, приведут к непозволительному снижению ресурсов, которые животное сможет направить на рост и развитие.
Ключевой особенностью системы «замены равных равными» является то, что, если все клетки равны, их следует беречь в равной степени, а значит, с равными затратами. Если бы животное защищало лишь некоторые клетки и использовало бы их для замены обычных поврежденных клеток, это позволило бы существенно сократить расходы. В идеале хорошо защищенные клетки должны располагаться в каком-то безопасном месте. И уже совсем хорошо с точки зрения экономии ресурсов было бы, если бы малочисленные клетки с высоким уровнем защиты могли давать начало любым типам клеток в ткани. Такие клетки, расположенные на стволе генеалогического древа различных типов клеток, называются «стволовыми». Поддержание ткани за счет стволовых клеток имеет значительные преимущества по сравнению с системой «замены равных равными». Если «замена равных равными» используется для быстрого залечивания небольших ран, обновление тканей за счет стволовых клеток у больших животных, например мышей и людей, позволяет тканям существовать на протяжении многих месяцев и лет.
Одним из наиболее изученных примеров обновления тканей за счет стволовых клеток является слизистая кишечника. Ее внутренняя поверхность подвергается химическому воздействию целого коктейля пищеварительных ферментов и солей желчных кислот, а также физическому воздействию частично переваренной пищи. Поэтому не приходится удивляться, что, несмотря на то что эти клетки в какой-то степени защищены слизью, большинство из них живет недолго. У мышей, хорошо изученных в отношении клеточной биологии кишечника, большая часть поверхностных клеток живет только пять дней. Скорее всего, у человека они живут примерно столько же. В подобной ситуации маловероятно, что поврежденные клетки в принципе могут заменяться за счет соседей неопределенно долгий срок. И действительно, они заменяются за счет популяции кишечных стволовых клеток, спрятанных в относительно безопасном месте. Чтобы понять, как кишечные стволовые клетки выполняют свою работу, необходимо сначала рассмотреть строение кишечной стенки.
Основной функцией кишечника является усвоение питательных веществ из пищи и повторное поглощение воды, добавленной к пище в процессе пищеварения. Усвоение происходит на внутренней поверхности кишки, а его эффективность во многом определяется общей площадью этой поверхности. У позвоночных выработалось два основных способа увеличения площади поглощающей поверхности. Одним из них является максимально компактная упаковка кишечника в брюшной полости: он не вытянут в прямую трубку, а образует многочисленные петли. Другой способ – придание выстилке сложной структуры. Выросты и гребни существенно увеличивают площадь всасывающей поверхности. Внутренняя поверхность тонкого кишечника густо покрыта ворсинками – мелкими пальцеобразными выростами (рис. 81). Они есть уже при рождении, а вскоре после него области между ворсинками складываются внутрь, образуя узкие углубления – крипты. Дно крипты образовано клетками Панета, которые секретируют бактерицидные белки (дефензины). Многочисленные клетки на стенках крипты выделяют слизь. Итак, углубленное положение защищает крипты от механических повреждений, слизь – от химического воздействия, а дефензины – от бактерий. Таким образом, крипты – значительно более безопасное место, чем ворсинки. Неудивительно, что именно в криптах залегают кишечные стволовые клетки.
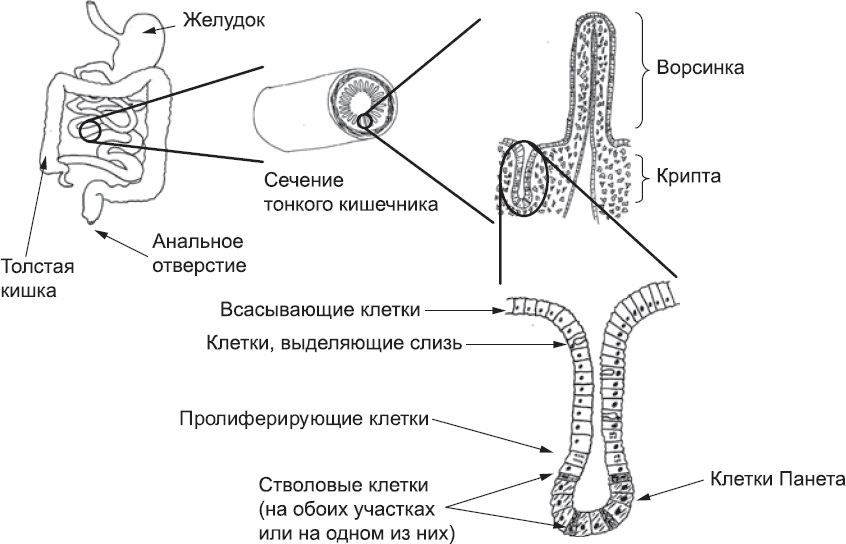
Рис. 81. Строение кишечной стенки и структура типичной крипты
Кишечные стволовые клетки могут находиться либо между клетками Панета на самом дне крипты, либо над ними, либо на обоих участках. Там они размножаются примерно раз в четыре дня. Дочерние клетки принимают решение – стать новыми стволовыми клетками или оставить эту нишу и начать двигаться вверх по стенке крипты. Мы пока не знаем, определяется ли решение клетки ее положением или наоборот. Так или иначе, популяция стволовых клеток сохраняется, а некоторые дочерние клетки покидают ее и продвигаются вверх по крипте. По мере продвижения эти клетки продолжают делиться, так что дочерняя клетка, образовавшаяся в результате деления одной стволовой клетки, примерно за три дня образует до шестидесяти четырех отдельных клеток. В ходе этого процесса эти клетки дают начало кишечным клеткам разных типов: одни станут всасывающими клетками, другие – клетками, выделяющими слизь, третьи – клетками Панета, а четвертые – редкими, специализированными клетками, которые синтезируют гормоны. Они продолжают двигаться вверх, потому что их выталкивают новые поколения образующихся внизу клеток. Тем не менее движение клеток не вполне пассивно, потому что немногие клетки, ставшие новыми клетками Панета, способны двигаться в противоположном направлении к нижней части крипты. Судя по всему, они следуют сигналам того же типа (EPH/ EPHRIN), которые использовались для разметки пути аксонов от глаза к мозгу (глава 13). К тому времени, когда клетки поднялись наверх и покинули крипту (то есть через несколько дней после деления исходной стволовой клетки), они уже достаточно созрели, чтобы в полной мере участвовать в деятельности кишечника по всасыванию питательных веществ и заменить отмершие клетки. Еще через несколько дней некоторые клетки поднимутся по ворсинкам и останутся там, пока не погибнут и не заместятся новыми клетками, образовавшимися в крипте.
Скорость отмирания клеток кишечника варьирует в зависимости от здоровья и рациона конкретного человека. У тех, кто ест мало и употребляет мягкую пищу, кишечные клетки гибнут относительно медленно. Скорость гибели кишечных клеток будет гораздо быстрее, если человек ест много жесткой, волокнистой пищи, имеет серьезную кишечную инфекцию или отравился токсинами. Понятно, что стволовые клетки и пролиферирующие дочерние клетки должны «чувствовать», как быстро они должны делиться: слишком медленное деление приведет к нехватке клеток кишечной стенки, а слишком быстрое деление вызовет закупорку кишечника массой ненужных клеток.
Механизмы, за счет которых кишечные стволовые клетки могут чувствовать нужную скорость деления, изучены не до конца, но мы уже знаем, что в этот процесс вовлечены сигнальные белки WNT, которые играют важную роль во многих процессах эмбрионального развития. Есть веские доказательства того, что ближайшие «потомки» стволовых клеток и, вероятно, сами стволовые клетки получают сигнал WNT от близлежащих клеток Панета и из более удаленных источников. Более того, у мышей, генетически модифицированных так, что эти клетки не могут отвечать на сигналы WNT, стволовые клетки не делятся, и стенки кишечника не функционируют. У мышей с противоположным типом мутации – клетки реагировали на WNT, которого на самом деле не было, – клетки делились слишком активно.
Источником сигнала WNT являются клетки, расположенные вокруг стволовых клеток. Учитывая, что пролиферация стволовых клеток, по-видимому, управляется сигналами WNT, надо полагать, что между уровнем определяемого стволовыми клетками сигнала и объемом текущего ремонта должна быть какая-то связь. Тем не менее этот механизм до сих пор окутан туманом. Непонятен и механизм, с помощью которого пролиферирующие клетки, движущиеся вверх по крипте, принимают правильное решение о том, в какой тип клеток дифференцироваться, и, таким образом, поддерживают правильное соотношение между количеством всасывающих клеток, защитных клеток и клеток, производящих слизь. Не исключено, что существует самоорганизующаяся система, в которой зрелые клетки каждого типа выделяют следовые количества определенного сигнала, говорящего о том, что незрелая клетка ни в коем случае не должна становиться клеткой этого типа. Если в такой системе клеток одного типа слишком много, их совокупный сигнал будет сильным, и «молодые» клетки будут становиться клетками другого типа. С другой стороны, если клеток определенного типа будет не хватать, уровень «запрещающего» сигнала будет очень низким, и близлежащие клетки будут, как правило, превращаться в клетки именно этого типа. Однако это пока лишь гипотезы. Интересно будет посмотреть, что покажут эксперименты.
Еще одна часть организма, подверженная довольно жесткому воздействию среды, – это роговица. Она не только защищает глаз снаружи, но и служит линзой, помогающей фокусировать свет на сетчатку. Собственно говоря, глаз функционирует как линза на две трети за счет роговицы и только на одну треть за счет хрусталика.
Роговица подвергается ультрафиолетовому облучению (особенно у неразумных людей, которые находятся на ярком солнце без солнцезащитных очков), ее царапают песок и пыльца, по ней несколько раз в минуту проходит моргающее веко. Роговицу может раздражать сигаретный дым, особенно если курит сам хозяин роговицы. Поскольку роговица должна быть прозрачной, в ней нет обильного кровоснабжения, очень важного для здоровья большинства тканей.
На эмбриональном этапе развития роговица формируется из эктодермы, обрастающей хрусталик на раннем этапе формирования глаз. Это уникальное событие, которое не может повториться. Как только роговица сформирована, она заменяет эктодерму, из которой образовалась, так что создать новую роговицу таким же образом, каким была создана исходная, нельзя. Изношенные клетки роговицы заменяются за счет стволовых клеток. Как и в случае кишечника, стволовые клетки находятся в более защищенном месте, чем полная опасности область, которую они обслуживают, а именно в лимбе – кольце по краю роговицы (рис. 82). Популяция стволовых клеток размножается, поддерживая саму себя и создавая дочерние клетки, предназначенные для роговицы. Как и в кишечнике, дочерние стволовые клетки пролиферируют относительно быстро, так что каждое деление исходных стволовых клеток дает начало многим клеткам роговицы. Пролиферирующие клетки покидают зону стволовых клеток глаза и движутся радиально внутрь, к самому центру зрачка – наиболее удаленной от стволовых клеток области глаза. Движение клеток от лимба к центру глаза было ярко продемонстрировано в экспериментах на химерных мышах, названных так по имени Химеры – мифического существа, состоящего из частей разных животных. Химерные мыши получаются из смеси эмбриональных клеток, часть которых нормальные, а часть несет экспериментально введенный маркерный ген, который может быть обнаружен либо при жизни животного, либо после его смерти с помощью метода специфического окрашивания. У химерных мышей некоторые стволовые клетки несут маркерный ген, а некоторые – нет. Когда глаза взрослой мыши исследуют на экспрессию маркерного гена, выявляется целая серия полос, которые, как спицы в колесе, сходятся в центре роговицы. Хотя эти полосы выглядят так, как будто они исходят от центра, на самом деле они создаются клетками, движущимися со стороны лимба, как было показано при изучении молодых мышей, у которых эти полосы еще не достигли центра.
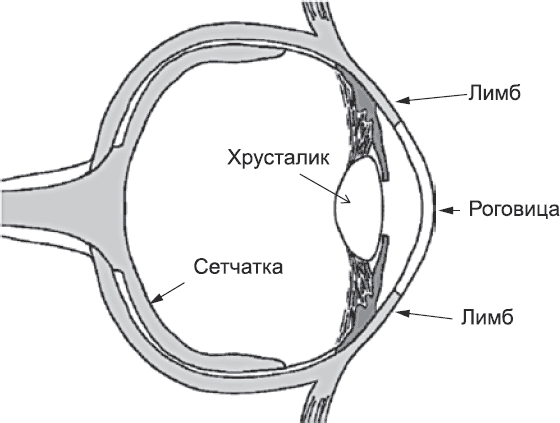
Рис. 82. Строение глаза и расположение лимб
Кишечник и роговица подвергаются агрессивному воздействию окружающей среды, поэтому их зрелые клетки активно изнашиваются, а стволовые клетки размножаются относительно быстро. Многие другие ткани находятся в гораздо менее жестких условиях, и их зрелые клетки могут жить месяцы или даже годы. Стволовые клетки, обслуживающие такие ткани, делятся очень редко, но они все равно очень важны, особенно если нужен крупномасштабный ремонт после инфекции или травмы. Хорошим примером такой популяции являются стволовые клетки почек.
В почечных канальцах здорового человека клетки, как правило, живут долго, но они могут получить сильные повреждения и погибнуть в результате инфекции или отравления. При развитии почек (глава 10) длинные, сложные трубочки нефронов формировались из групп клеток, которые собирались вместе и образовывали цистообразный шар, который затем удлинялся и изгибался, формируя трубку. Этот процесс формирования новых канальцев из клеток, которые изначально не были частью нефронов, происходит только при эмбриональном развитии. После рождения в организме человека новые канальцы не могут образовываться с нуля, но, судя по всему, клетки канальцев могут заменяться за счет маленькой популяции стволовых клеток, существующей в особой зоне каждой трубочки, между клубочком и самой трубочкой (рис. 83).
В здоровом организме уровень пролиферации этих стволовых клеток очень низок. Когда стволовые клетки «улавливают» повреждение клубочка или канальца (какими-то пока неизвестными способами), они делятся, и их дочерние клетки перемещаются в каналец или в клубочек, по мере своего продвижения переставая быть стволовыми клетками и приобретая свойства дифференцированных клеток. Добравшись до места назначения, они заполняют пробитую повреждением брешь.
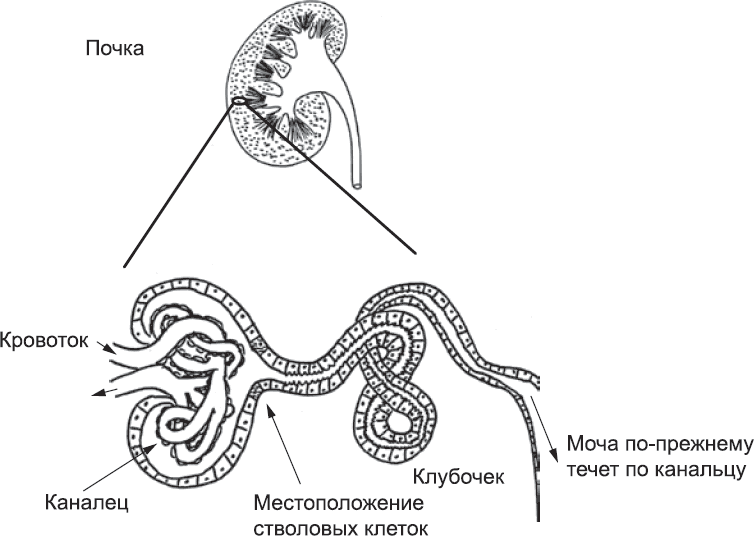
Рис. 83. Местоположение стволовых клеток в канальцах зрелых почек (стволовые клетки могут также находиться в других местах)
На данный момент есть одна система, в которой нам известны по крайней мере некоторые сигналы. Это популяция стволовых клеток крови. Кровь в системе кровообращения содержит несколько типов зрелых клеток. Наиболее распространены эритроциты, содержащие гемоглобин – пигмент, который переносит кислород и придает крови ее характерный цвет. В гораздо меньших количествах в крови присутствуют различные клетки иммунной системы, в том числе фагоциты, В-клетки и Т-клетки (глава 17), а также кровяные пластинки (тромбоциты), играющие важную роль в процессе свертывания крови. На ранней стадии развития первые клетки крови образовались при взаимодействии тканей рядом с временными почками (глава 9), но затем эти ткани исчезли, и поддержание кровеносной системы переключилось на использование механизма, основанного на стволовых клетках. На какое-то время стволовые клетки поселяются в печени эмбриона, а после появления длинных костей перемещаются в их центральную часть. Стволовые клетки и развивающиеся клетки крови образуют большую часть костного мозга.
Как и в случае кишечника, сами стволовые клетки (гематопоэтические стволовые клетки, или ГСК) находятся в основании разветвленного древа разных типов дочерних клеток (рис. 84). Популяция ГСК делится медленно, поддерживая себя и давая начало дочерним клеткам, которые затем выбирают путь созревания. Дочерние клетки размножаются быстро и создают постоянно растущие колонии клеток, которые позже изберут свою судьбу, пройдя ряд определенных этапов (рис. 84). И в этом случае пролиферация клеток должна соответствовать потребностям организма – на смену погибающим клеткам крови должно приходить то же количество новых. Если бы в костном мозге образовалось слишком много новых клеток, кровь превратилась бы в густой «суп», а если бы клеток образовалось слишком мало, кровь не могла бы переносить достаточное количество кислорода или эффективно защищать организм. Баланс типов клеток тоже должен тщательно регулироваться и может меняться в зависимости от обстоятельств: например, во время поражения организма инфекциями количество защитных клеток увеличивается.
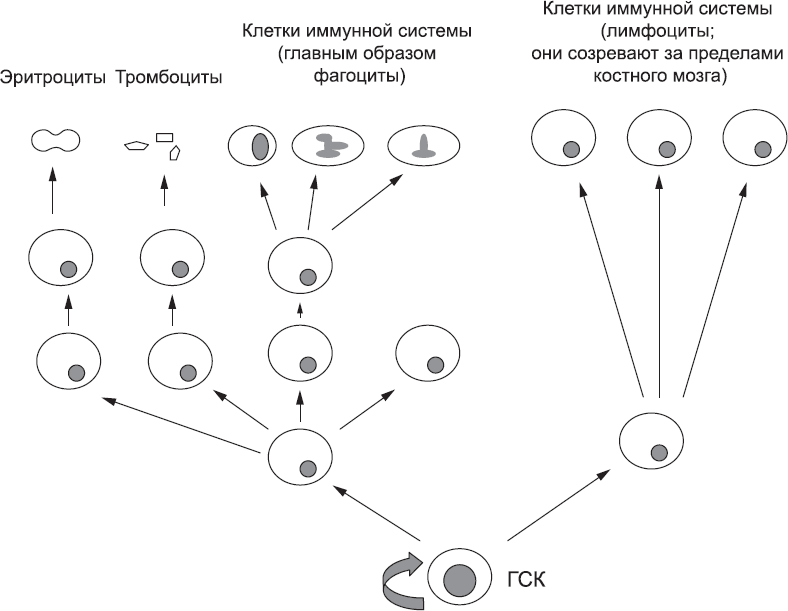
Рис. 84. «Генеалогическое древо» клеток, образующихся в костном мозге из гематопоэтических стволовых клеток (ГСК). Популяция этих стволовых клеток постоянно самоподдерживается и дает начало клеткам, расположенным выше на схеме. Эти клетки тоже размножаются, и поэтому каждое деление ГСК в нижней части «древа» приводит к образованию огромного количества терминально дифференцированных, зрелых клеток
Хитроумные эксперименты с клетками костного мозга, выращенными в лабораторных условиях, позволили выявить множество сигнальных молекул, влияющих на скорость пролиферации клеток костного мозга. Каждый тип клеток реагирует на определенный набор сигналов. Клетки, которые уже приняли решение стать эритроцитами, несут на своих поверхностях рецепторы для гормона эритропоэтина. При низком содержании этого гормона клетки делятся очень неактивно – можно сказать, выжидают. Если эритропоэтина мало, клетки энергично пролиферируют, и их дочерние клетки превращаются в новые эритроциты. Сам эритропоэтин производится в основном в той части почки, где кровоснабжение по анатомическим причинам довольно скудно даже у здорового человека. Клетки почек «ощущают» концентрацию кислорода вокруг них, используя ту же молекулярную систему, что и клетки, «запрашивающие» новые кровеносные сосуды (глава 9). Чем ниже концентрация кислорода, тем больше эритропоэтина выделяют и высвобождают клетки почек. Этот эритропоэтин идет к костному мозгу, где стимулирует пролиферацию клеток и, следовательно, производство новых эритроцитов. В результате кровь переносит больше кислорода, и его содержание в тканях повышается. Чувствуя это, клетки почек сокращают производство эритропоэтина, и система приостанавливает свою работу, так что производство эритроцитов только балансирует потери и поддерживает оптимальное число этих клеток.
Таким образом, система в целом самоорганизуется и производит ровно столько новых эритроцитов, сколько нужно. При этом ее отдельные компоненты не должны ничего «знать», а должны только правильно реагировать на простой химический сигнал. Этот механизм вполне надежен, если единственный источник эритропоэтина находится в здоровых тканях организма, но может нарушаться при болезненных состояниях, создающих ложные сигналы. Когда кровоснабжение почки снижается (например, при болезни или повреждении почечной артерии), клетки почки испытывают острую нехватку кислорода, в то время как остальные ткани организма находятся в полном порядке. Тогда клетки почек производят эритропоэтин в очень больших количествах, и новых эритроцитов производится слишком много. Аналогичным образом, если в организм вводят дополнительное количество эритропоэтина, костный мозг ведет себя так, как если бы количество эритроцитов достигло критически малого уровня, и производит новые клетки. Целый ряд спортивных скандалов последнего времени связан с тем, что спортсмены использовали эритропоэтин, чтобы увеличить кислородную емкость крови и, следовательно, максимальную мощность мышц.
Производство клеток иммунной системы и их предшественников в костном мозге также регулируется сигналами организма. Например, под действием микробного заражения существующие защитные клетки – Т-клетки и фагоциты (глава 17) – производят сигнальные молекулы дальнего действия. Они распространяются через кровеносную систему по всему организму и достигают костного мозга, где стимулируют клетки вырабатывать «коктейль» локальных сигнальных молекул. Эти сигналы запускают пролиферацию клеток, уже вступивших на путь дифференцировки в клетки иммунной системы, а также активируют быстрое созревание клеток иммунной системы. Таким образом костный мозг реагирует на заражение в любом месте организма и быстро посылает туда подкрепление.
Ситуационно зависимая стимуляция производства эритроцитов эритропоэтином и производства клеток иммунной системы другими сигналами решает проблему поддержания нужного количества клеток в кровеносной системе, но создает новую проблему в самом костном мозге. Популяция предшественников эритроцитов, пролиферация и созревание которых активируются эритропоэтином, не может самоподдерживаться бесконечно. Рано или поздно все клетки созреют и покинут костный мозг уже в качестве эритроцитов. Следовательно, им нужна замена за счет деления клеток, расположенных ниже на «генеалогическом древе» (рис. 84). Эти клетки тоже рано или поздно кончатся, и тогда придется делиться самим стволовым клеткам (ГСК). Это означает, что проблема контроля над пролиферацией охватывает все уровни «древа». Такое впечатление, что эта проблема решается с помощью относительно простого общего механизма сигнализации, который работает для всех клеток одинаково, хотя для разных типов клеток используются разные молекулы. В принципе каждая клетка выделяет молекулы, которые ингибируют пролиферацию типа клеток, расположенного ниже на «генеалогическом древе». Если на высшем уровне достаточно клеток, вместе они будут производить достаточно ингибирующих сигналов, чтобы клетки под ними могли спать спокойно. Если количество клеток на более высоком уровне снижается из-за того, что клетки созревают и покидают костный мозг, то ингибирующих сигналов будет меньше, и поэтому клетки на более низких уровнях будут делиться более активно, а их дочерние клетки заполнят уровень над ними. Эта система ступенчато спускается вниз до уровня ГСК. В костном мозге явно есть и другие сигналы, но результаты компьютерного моделирования говорят о том, что эти нисходящие ингибирующие сигналы являются главными регуляторами пролиферации.
Важность костного мозга как хранилища стволовых клеток крови была открыта уже несколько десятков лет назад, хотя многие детали работы этого хранилища все еще ждут своих исследователей. Одним из самых последних открытий является то, что стволовые клетки, расположенные в костном мозге, могут также давать начало клеткам других тканей организма. На самом деле, не исключено, что костный мозг способен производить клетки для поддержания любого типа соединительной ткани. Это открытие потрясает основы нашего понимания биологии человека. Эти стволовые клетки называются мезенхимными стволовыми клетками и, видимо, являются дочерними клетками ГСК, о которых я только что говорил. Если удалить их из организма и выращивать в лабораторных условиях, мезенхимные стволовые клетки могут давать начало огромному спектру зрелых клеток, в том числе клеток соединительной ткани, жира, хрящей и костей. Разные условия культивирования приводят к получению разных типов клеток.
Тот факт, что мезенхимные стволовые клетки из костного мозга могут производить те или иные типы клеток в лаборатории, не означает, что они на самом деле делают это в организме. Однако один непреднамеренный «эксперимент», поставленный непосредственно на людях, показал, что эти клетки действительно способствуют поддержанию удаленных соединительных тканей. Жизнь людей с разрушенным костным мозгом (например, под воздействием высоких доз радиации или агрессивной химиотерапии, применяемой против лейкемии) можно спасти, пересадив им здоровый костный мозг от донора. Если организмы донора и реципиента достаточно сходны и отторжения не происходит, донорские клетки поселяются в костном мозге реципиента и там начинают делать новую кровь. Совместимость донора и реципиента зависит в том числе от совместимости белков клеточной поверхности, которые производят их клетки. Это немного похоже на систему групп крови для донорства, только гораздо сложнее. Пол донора и реципиента не имеет значения, и нередко донор и реципиент являются братом и сестрой или отцом и дочерью.
Во всех клетках мужского организма есть Y-хромосома, а в клетках женского ее нет (глава 12). Когда костный мозг от мужчины-донора пересаживается женщине-реципиенту, Y-хромосома донорских клеток является четким генетическим признаком, отсутствующим в клетках реципиента. Если операция проходит успешно, то женщина-реципиент может прожить долгие годы, и ее организм будет самоподдерживаться. Если мезенхимные стволовые клетки в костном мозге в естественных условиях способствуют обновлению соединительной ткани организма, то некоторые клетки соединительной ткани должны содержать Y-хромосому, что можно проверить путем микроскопирования образцов ткани, полученных с помощью биопсии или аутопсии. По всей видимости, это так и есть: соединительные ткани женщин-реципиентов, получивших костный мозг от доноров-мужчин, действительно содержат клетки с Y-хромосомой. Такие клетки были описаны в соединительной ткани сердца, кишечника,,, мозга,, и почек и всегда были, по видимому, неотъемлемой частью этих тканей (а не просто, например, клетками проходящей через них крови). Y-хромосома иногда даже обнаруживалась в некоторых тканях, которые в принципе не являются соединительными, например в канальцах печени и почек, в выстилке кишечника и в нервных клетках головного мозга. Клетки, по происхождению связанные с костным мозгом, входили в состав таких патологических структур, как клеточные массы эндометриоза (доброкачественного разрастания слизистой матки в неправильном месте) и злокачественная карцинома. Донорские клетки, несущие Y-хромосому, обнаруживались даже в составе матки женщины-реципиента, что еще раз подчеркивает тот факт, что большинство клеток организма принимают решение о том, создавать им мужские или женские структуры, вовсе не на основании наличия или отсутствия Y-хромосомы, а под действием их окружения и гормонов (глава 12).,
Эти данные не доказывают, что мезенхимные стволовые клетки являются источником клеток любого типа, но свидетельствуют о том, что какие-то стволовые клетки такого рода в костном мозге есть. На это же указывают и результаты других исследований, никак не связанных с трансплантацией, а использующих, например, спонтанные генетические изменения в костном мозге некоторых людей как маркеры определенных клеток костного мозга.
Странно, но факт: клетки, несущие Y-хромосому, были также обнаружены в тканях женщин, которые никогда не переносили трансплантацию, но родили мальчиков., По-видимому, стволовые клетки мужского эмбриона проникли через плаценту и поселились в организме матери. Они обнаруживались спустя годы после родов, а в одном исследовании даже присутствовали во всех проанализированных тканях. Можно сказать, что ребенок навсегда оставил след в сердце своей матери, и в данном случае это не просто метафора.
Даже если мы признаем, что костный мозг может участвовать в обслуживании отдаленных тканей, пока непонятно, насколько его вклад важен по сравнению со стволовыми клетками, которые находятся непосредственно в тканях. Методы, используемые для оценки вклада костного мозга, очень чувствительны, и не исключено, что они зарегистрировали крайне интересный, но по большому счету незначительный способ поддержания тканей. Например, вклад клеток костного мозга в обслуживание тканей кишечника очень мал по сравнению с вкладом стволовых клеток крипт. Однако даже если вклад костного мозга в восстановление тканей организма незначителен, он может оказаться полезным с медицинской точки зрения. Я расскажу об этом в последней главе.
Как я уже говорил, стволовые клетки обычно очень берегут себя. Например, они тратят много энергии и ресурсов на создание насосов и каналов для отведения токсинов. Они также очень чувствительны к повреждениям ДНК и скорее совершат самоубийство, чем будут с ними бороться. Можно предположить, что такое положение дел сложилось в ходе естественного отбора и связано с пагубными последствиями пролиферации поврежденных клеток. Забота стволовых клеток о себе любимых и их склонность к «самоубийству» при сильных повреждениях – это реальность, которая может обернуться темной стороной, если человек болен. Одним из примеров является острая лучевая болезнь. Через несколько дней после умеренного или сильного воздействия ионизирующего излучения у человека обычно развивается сильнейший понос с кровью, рвота, выпадение волос и оппортунистические инфекции. Одной из причин диареи является гибель множества кишечных стволовых клеток в криптах, которые обнаружили повреждение ДНК и самоустранились. С таким количеством отмерших клеток выстилка кишечника, и сама по себе поврежденная, больше не может обновляться. Люди, которые переживают этот этап, часто умирают в течение нескольких недель из-за аналогичной потери стволовых клеток костного мозга и, следовательно, неспособности обновлять клетки крови (в том числе клетки иммунной системы). Общее состояние обычных клеток организма может быть, несмотря на повреждения, не таким уж плохим, но нетерпимость стволовых клеток к повреждениям обрекает человека на медленную и мучительную смерть. Так погибли жертвы печально известных событий в Лос-Аламосе, Хиросиме, Нагасаки, Бикини, Кыштыме, Винче, К-19, К-8, К-431 и Чернобыле.
Системы обнаружения повреждений стволовых клеток могут давать сбой, и тогда даже эти клетки могут быть затронуты мутациями. Многие из этих мутаций «молчащие», то есть они не сказываются на поведении клетки, но некоторые могут оказаться серьезными. Мы уже говорили о важности системы WNT-сигнализации в управлении скоростью деления стволовых клеток кишечника и их дочерних клеток и отметили, что у мышей мутации, принудительно запускающие WNT-сигнализацию в этих клетках, приводят к сильному увеличению темпа пролиферации. Кишечные опухоли – третий по распространенности вид рака у людей, и большинство из них связано с активирующими мутациями в системе WNT-сигнализации. К моменту образования агрессивной, распространяющейся опухоли в клетках уже есть и другие мутации, но частота встречаемости мутаций WNT заставляет полагать, что именно они являются основной причиной этого вида рака.
По крайней мере при некоторых видах рака толстой кишки нормальная схема работы стволовых клеток кишечника, которые возобновляют свою популяцию и дают начало пролиферативным дочерним клеткам, сохраняется даже тогда, когда клетки мутировали и образовали опухоль. С этого момента размножение стволовых клеток выходит из-под контроля, и точно так же ведут себя их дочерние клетки. Однако если мутировавшие стволовые клетки могут поддерживать свою популяцию, их дочерние клетки после многократного деления исчерпывают себя и погибают, вытесняемые более поздними дочерними клетками. Аналогичным образом раковые стволовые клетки могут образовать новую опухоль при пересадке другому животному, а другие клетки опухоли не могут. Поскольку нормальное строение стенки кишечника при опухоли нарушено, действия мутировавших стволовых клеток и их дочерних клеток уже не имеют анатомического смысла, но их основная логика сохраняется. Кроме того, стволовые клетки сохраняют «привычку» поддерживать себя в хорошей форме. Раковые опухоли, которые нельзя удалить хирургическим путем, как правило, лечат с помощью химиотерапии, то есть с помощью препаратов, которые токсичны для делящихся клеток. Проблема в том, что стволовые клетки отлично умеют избавляться от этих препаратов и устранять вызванные ими повреждения. Кроме того, хотя стволовые клетки продолжают делиться, они обычно делятся гораздо медленнее, чем дочерние клетки, которые (в норме) должны выйти из крипты. В кишечнике здорового человека стволовые клетки делятся примерно раз в четыре дня, а их дочерние клетки, которые продвигаются по крипте, – примерно раз в двенадцать часов. Таким образом, стволовые клетки в меньшей степени подвержены воздействию препаратов, направленных на делящиеся клетки, а также лучше их выводят. Таким образом, существует реальная опасность того, что лекарства уничтожат всю опухоль кроме самих стволовых клеток, которые, учитывая их уникальную способность образовывать новые опухоли, следовало бы убить в первую очередь. При раке этого типа рецидив опухоли после нескольких лет кажущейся свободы от болезни связан с выживанием небольшого числа стволовых клеток.
Следует подчеркнуть, что, несмотря на убедительные аргументы в пользу того, что определенные опухоли связаны с мутациями стволовых клеток, далеко не все онкобиологи согласны, что эта модель описывает все виды рака или хотя бы их большинство., Этот вопрос необходимо разрешить как можно скорее, так как ответ на него помог бы определить стратегию разработки методов лечения, которые, возможно, должны быть прицельно направлены на стволовые клетки. Учитывая, что у каждой стороны есть веские доводы, может просто оказаться, что в основе одних видов рака лежат раковые стволовые клетки, а в основе других – нет. Тогда первоочередной задачей онколога должно стать выяснение того, какой тип опухоли имеет пациент.
Рак – не единственная болезнь, связанная с аномальным поведением стволовых клеток в тканях. Слишком сильная пролиферация стволовых клеток и их дочерних клеток может вызвать серьезные проблемы в тканях, даже если эти клетки не затронуты раком. Сразу после открытия стволовых клеток почечных канальцев (см. выше) ученые поняли, что главная проблема серьезных заболеваний почек, скорее всего, связана с неправильным поведением стволовых клеток. Основным патологическим признаком серповидного гломерулонефрита является повреждение фильтрующих клубочков на концах канальцев и замена их бесполезной в качестве фильтра массой неспециализированных клеток, расположенных в форме полумесяца. Если такая замена затрагивает много почечных канальцев, это может привести к почечной недостаточности. Судя по экспрессии белков в этих клетках, они являются дочерними клетками стволовых клеток почечных канальцев, которые делились слишком активно и, вместо того чтобы стать клетками клубочков, образовали клеточную массу. Избыточная пролиферация не имеет ничего общего с раком и, вероятно, связана с какой-то первопричиной заболевания, которая заставляет почку сигнализировать клеткам о необходимости делиться, хотя на самом деле такой потребности нет.
Недостаточно активное деление стволовых клеток приводит к коллапсу ткани, которую они обслуживают. При кератопатии, связанной с аниридией, прозрачная роговица глаза заменяется молочно-белой тканью, похожей на шрам. Видимо, это происходит из-за нарушения деления лимбальных стволовых клеток (хотя, возможно, это не единственная причина). В результате развивается слепота. При этом заболевании основная проблема, видимо, связана не с самими стволовыми клетками, а с неправильной средой лимба, нарушающей их нормальное поведение.
Описанные выше нарушения работы стволовых клеток встречаются у относительно немногих людей. Однако одна проблема, связанная с работой стволовых клеток, затрагивает всех без исключения. Замена поврежденных и изношенных клеток нашего тела новыми несовершенна, и в ходе жизни мы постепенно накапливаем повреждения. Иными словами, мы стареем. Существует множество различных теорий того, почему мы стареем (небольшие и просто устроенные организмы этого не делают). Согласно одной из них, дело просто в том, что мы накапливаем случайные повреждения (от излучения, свободных радикалов, ядов и т. п.) быстрее, чем они устраняются или компенсируются за счет деления клеток. Даже если в организме еще много неповрежденных стволовых клеток, постепенная деградация основной массы тканей приводит к трудностям при их ремонте. Поврежденные клетки посылают сумбурные сигналы, межклеточные контакты препятствуют «уборке территории» и т. п. Эти проблемы, поначалу мелкие, накапливаются медленно, но неумолимо, и естественный ремонт перестает справляться с ними. Со временем старение ускоряется. Когда изменения начинают серьезно нарушать работу какой-нибудь из важнейших систем организма, например почек или сердца, вся внутренняя среда становится аномальной, и рано или поздно наступает момент, когда она уже не подлежит восстановлению.
В принципе организм может вкладывать в ремонт больше ресурсов и стареть медленнее. В многочисленных генетических экспериментах были получены организмы, стареющие гораздо медленнее нормальных, хотя и они в конечном итоге все же стареют и умирают. Чтобы понять, почему мы, как и другие организмы, не несем наборы генов, обеспечивающие максимально долгую жизнь, нужно попытаться понять, как работает эволюция.
Рассмотрим начальную популяцию животных, в которой относительный объем ресурсов, вкладываемых в ремонт организма, варьируется от особи к особи: одни вкладывают много и живут долго, другие вкладывают мало и живут энергично, но недолго. Представленность каждой из этих двух категорий животных в следующем поколении будет зависеть от того, сколько потомства каждой категории дожили до зрелости. Потенциально долгоживущие животные могут многократно размножаться, что является несомненным плюсом, но для успешного размножения нужно искать партнеров, пищу и территорию. Их соперники, которые сделали ставку на энергичную и короткую жизнь с небольшими затратами на «ремонт» организма, будут иметь меньше времени на размножение, но если им хватит энергии на то, чтобы более эффективно найти партнеров, пищу и территорию, то, может, они и смогут размножиться. Если бы все было так просто, то долгая жизнь, возможно, была бы наилучшим вариантом для получения наибольшего количества потомства, и долгоживущие животные стали бы доминировать. Однако баланс может быстро измениться под действием хищников и болезней. Если существует высокая вероятность погибнуть в любой момент, то вложения в механизмы ремонта, обеспечивающие долгую жизнь, становятся намного менее выгодными, ведь значительная часть таких вложений может пропасть зря. Нет смысла вкладываться в систему восстановления организма, которая позволяет жить веками, если шансы быть съеденным составляют около 50 % каждый год. В таких условиях альтернативные вложения в быструю жизнь и бурное размножение без заботы о завтрашнем дне дают реальные преимущества.
Теория о том, что риск гибели от хищников обуславливает выбор генных наборов, которые не вкладывают слишком много ресурсов в долгожительство, в определенной мере подтверждается сравнением сходных животных, которые находятся под разным давлением хищников. На мелких летучих мышей, например, мало кто охотится. Они вкладывают много ресурсов в долгосрочное поддержание организма и живут в природе около тридцати лет. На обычных мышей примерно такого же размера охотится множество хищников. Они быстро размножаются, но вкладывают мало ресурсов в поддержание организма. Даже ручные мыши, которых держат как домашних питомцев и оберегают от всех опасностей, живут лишь около трех лет, то есть десятую часть жизни летучей мыши.
Палеонтологическая летопись человека свидетельствует, что наш вид – Homo sapiens – отделился из других гоминид лишь несколько сотен тысяч лет назад в Африке, где было много хищников. Хотя к тому времени наши предки использовали различные орудия в течение нескольких миллионов лет, они, скорее всего, были в той же мере уязвимы для хищников, что и другие гоминиды, – во всяком случае, до внезапного технологического прорыва, случившегося около десяти тысяч лет назад и ознаменовавшего начало неолита. Десять тысяч лет – то есть всего пятьсот поколений – небольшой отрезок времени с точки зрения эволюции, и, вероятно, поэтому мы до сих пор являемся компромиссным вариантом между энергичной короткой жизнью и вложением в долголетие, который сложился у наших предков под воздействием хищничества на африканской равнине. Даже сейчас, когда для тех из нас, кому посчастливилось жить в странах «первого мира», риски умереть от болезней и хищников сведены к минимуму, отбор на долгожительство практически отсутствует. На самом деле тот факт, что даже осиротевший ребенок остается под надежным присмотром, нейтрализует один из немногих эволюционных факторов, увязывающих долголетие родителей с успехом потомства. Поэтому наши естественные системы поддержания организма вряд ли когда-либо позволят нам жить больше ста лет. Если мы хотим обзавестись более эффективными системами ремонта и жить дольше, мы должны сделать что-то сами, применяя на практике знания о нормальном развитии и обновлении организма.
Назад: Глава 17 Друзья и враги
Дальше: Часть IV Перспективы

