Получение нуклеотидов из продуктов атмосферной фотохимии
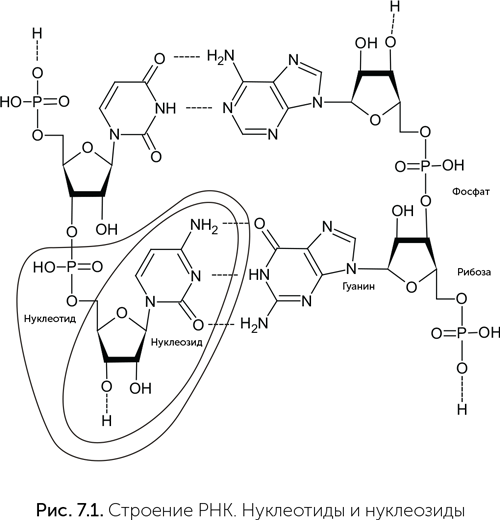
Вспомним, как устроены нуклеиновые кислоты: РНК и ДНК. Их длинные молекулы состоят из повторяющихся единиц — нуклеотидов. Каждый нуклеотид состоит из трех основных деталей: азотистого основания, сахара (рибоза в РНК и дезоксирибоза в ДНК) и фосфата. Остов молекулы составляют соединенные в цепочку сахара и фосфаты, а азотистые основания прикреплены к сахарам сбоку (рис. 7.1). В двухцепочечной форме две цепи РНК или ДНК лежат рядом и образуют двойную спираль. Их азотистые основания контактируют между собой, образуя комплементарные пары А-Т и Г-Ц, а сахарофосфатные остовы удалены друг от друга, располагаясь кнаружи от пар азотистых оснований.
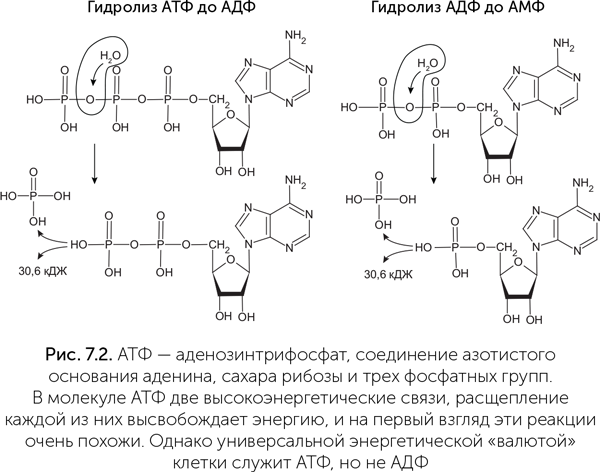
Когда в клетке строятся новые молекулы ДНК или РНК, сначала рибоза соединяется с одним из четырех азотистых оснований. Такая молекула называется нуклеозид. Дальше к ней присоединяются фосфатные группы общим числом до трех. Нуклеозид с фосфатными группами составляет нуклеотид. Далее из нуклеотидов строится цепочка РНК или ДНК. Новые нуклеотиды присоединяются к цепочке по одному, и каждый раз две фосфатные группы отделяются, а третья входит в состав цепочки. На построение фосфатного хвоста нуклеотидов затрачивается энергия, а при его распаде эту энергию можно использовать разными способами. Нуклеотид-трифосфаты и другие формы нуклеотидов, которые можно соединить в цепочку РНК без дополнительных затрат энергии, называют еще «активированными нуклеотидами». Один из активированных нуклеотидов, АТФ (аденозинтрифосфат), играет в клетках роль универсальной энергетической «валюты», подобно электрической энергии в человеческой цивилизации (рис. 7.2). АТФ может с равным успехом обеспечивать энергией сборку РНК, ДНК и белков, сокращение мышц, прохождение нервного импульса, фильтрацию и концентрирование солей в почках, а также множество других процессов.
Соответственно, чтобы получить РНК, не имея клеток и ферментов, надо как-то создать азотистые основания и рибозу из тех веществ, которые были доступны на древней Земле. Потом необходимо соединить их друг с другом и с фосфатом в нуклеотиды, а затем соединить нуклеотиды в цепочки.
Как мы помним, атмосфера древней Земли могла состоять в основном из углекислого газа и азота, и органические вещества в такой среде не образуются. Во время проведения опытов Миллера по получению аминокислот и другой органики в электрических разрядах ученые использовали смесь водорода, метана и аммиака, которая в условиях Земли быстро будет разрушена солнечным ультрафиолетом. В прошлой главе мы определили, что первые шаги земная жизнь делала в геотермальных водоемах, где есть несколько источников органических веществ. Это фотосинтез на кристаллах сульфида цинка, поставляющий муравьиную, уксусную и другие органические кислоты, и реакции на горячем сульфиде железа, в которых образуется карбонилсульфид (COS), меркаптаны, тиоуксусная кислота (CH3COSH) и ее эфиры. Для синтеза азотистых оснований это не очень подходящее сырье, потому что там нет необходимого азота, зато есть ненужная для РНК сера. Однако если на планете действует постоянный источник метана, то солнечный ультрафиолет может производить из него и атмосферного азота хорошее сырье для азотистых оснований и сахаров.
Круговорот метана на древней Земле
В 2000 году на дне Атлантического океана были обнаружены белые колонны неправильной формы и высотой до 50 м. Из колонн сочилась горячая вода. Это гидротермальное поле, получившее название Lost City («затерянный город»), отличается от «черных курильщиков», о которых мы говорили ранее. Температура воды в Lost City около 80 °С, и несет она не сульфиды металлов, а гидроксид магния, который выпадает в осадок и слагает белые колонны. В отличие от «черных курильщиков», Lost City находится примерно в 50 км от рифтовой долины, и его вода подогревается не горячей магмой, а химическими реакциями в толще твердых донных пород. Эти реакции в геологии называются «серпентинизация»: в них изверженные в рифтовой долине базальты превращаются в минералы зрелого океанского дна — серпентиниты. Серпентинизация происходит, когда базальт остывает до 200–300 °С, трескается и в трещины входит морская вода. Она реагирует с силикатами железа, окисляя железо до магнетита, при этом выделяется водород:
3Fe2SiO4 + 2H2O → 2Fe3O4 + 3SiO2 + 2H2.
Если в воде был растворен углекислый газ, то он в этих условиях восстанавливается до метана (CH4) и муравьиной кислоты (HCOOH). В горячей воде Lost City растворено до 30 мг/л метана и водорода, до 7 мг/л муравьиной и до 1 мг/л уксусной кислоты; изотопный состав углерода в них точно такой же, как в углекислом газе, т.е. метан и кислоты образуются абиогенно, без участия микробов (Lang et al., 2010).
Горячие источники, подобные Lost City, с тех пор были найдены во многих районах океанского дна. Их населяют богатые микробные сообщества, питающиеся метаном, муравьиной кислотой и водородом. На древней Земле геологические процессы были гораздо активнее, содержание углекислоты в океанской воде — выше, и серпентинизация производила большое количество водорода и метана. Выходящий в атмосферу метан вступал в химические реакции под действием солнечных лучей. Подобные процессы мы сейчас можем наблюдать в атмосфере Титана — крупнейшего спутника Сатурна, обладающего атмосферой из азота и 1–2% метана. Как показали наблюдения зонда «Кассини» и его спускаемого аппарата «Гюйгенс», в атмосфере Титана метан превращается в ацетилен (C2H2) и более сложные углеводороды (Raulin, Owen, 2002). Кроме того, под действием ультрафиолета метан реагирует и с прочными молекулами азота, при этом образуются цианид (HCN) и его производные — цианамид (NH2 CN) и цианоацетилен (HC3N). Эти вещества создают желтую дымку в атмосфере Титана, скрывающую его поверхность.
Земля отличается от Титана в нескольких отношениях. Во-первых, она в 10 раз ближе к Солнцу и получает в 100 раз больше ультрафиолетовых лучей на каждый квадратный метр атмосферы. Во-вторых, она гораздо теплее, чем промерзший до –170 °С Титан, и в ее атмосфере есть еще водяной пар и углекислый газ. Поэтому на древней Земле метан в атмосфере реагировал не только с азотом, но и с углекислым газом и водой, образуя формальдегид (CH2O). В-третьих, на Земле идут (и почти всегда шли) дожди из жидкой воды, поэтому продукты фотолиза метана не накапливаются в виде дымки, а растворяются в каплях воды и выпадают с дождем. И синильная кислота, и формальдегид хорошо растворимы в воде и быстро вымываются дождями из атмосферы (рис. 7.3). Поэтому на поверхность древней Земли регулярно поступали те органические вещества, из которых в принципе можно построить аминокислоты, сахара и нуклеотиды: формальдегид, цианид, цианамид и цианоацетилен. Хотя мы привыкли считать цианид сильнейшим ядом, на самом деле он блокирует только кислородное дыхание. Анаэробные (живущие без кислорода) бактерии могут им питаться, и, как мы вскоре увидим, цианид является отличным сырьем для производства азотистых оснований и РНК на заре жизни.
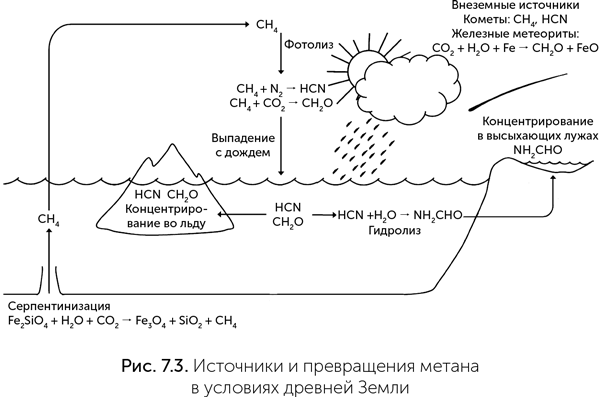
Кроме фотохимических реакций метана есть и другие источники цианида и формальдегида. Цианид обнаруживается в газах и испарениях геотермальных полей, например на склонах Мутновской сопки на Камчатке. Формальдегид образуется из углекислого газа и паров воды при разрядах молний и при контакте атмосферы с горячим металлическим железом (обломки упавших метеоритов и включения железа в вулканических лавах) (Cleaves, 2008).
Цианид постепенно реагирует с водой и превращается в формамид (NH2CHO). Как мы увидим, формамид тоже может быть хорошим предшественником нуклеотидов, кроме того, он отличается высокой температурой кипения (218 оС) и поэтому может накапливаться в высыхающих лужах после дождя.
Химия цианидно-формальдегидных дождей
Итак, для построения сложных органических молекул на поверхности древней Земли у нас есть формальдегид, цианид и его производные. Что и как можно сделать из этих составляющих?
Еще в 1865 году А. М. Бутлеровым была открыта так называемая формозная реакция: водный раствор формальдегида (СH2O) с добавлением гидроокиси кальция (известковая вода) при небольшом нагревании превращается в сложную смесь сахаров. (Об этом, а также о других проблемах биогенеза рассказывалось в статье Пармона В. Н. Новое в теории появления жизни // Химия и жизнь. 2005. № 5.) Изучению реакции много лет мешал ее капризный характер: колбу с раствором надо было греть несколько часов без всяких видимых изменений, и вдруг в течение пары минут раствор быстро желтел, затем коричневел и загустевал. А если исходные реагенты были очень чистыми, то реакция не шла вовсе. Причиной «капризов» оказался автокаталитический характер реакции: сначала формальдегид медленно превращается в двух- и трехуглеродные сахара (гликольальдегид, глицеральдегид и дигидроксиацетон), которые затем катализируют синтез самих себя и более сложных сахаров. Если к исходной смеси добавить чуть-чуть гликольальдегида или глицеральдегида, то реакция запускается почти сразу. Другой способ ускорить ее — осветить раствор ультрафиолетом, под действием которого некоторые молекулы формальдегида соединяются в гликольальдегид.
В классической реакции Бутлерова получаются сложные смеси сахаров, в которых сахара, характерные для живых клеток, перемешаны с огромным разнообразием семи-, восьми-, девятиуглеродных сахаров и даже более сложных. Если ее не останавливать вовремя, то в итоге получается коричневая карамелизованная смесь сложных сахаров и продуктов их распада. Подобная проблема часто встречается в предбиогенной химии: если к органическим веществам долго подводить энергию в виде тепла или ультрафиолета, то в итоге обычно получаются сложнейшие, неразделимые смеси веществ, похожие на смолу или деготь. Это знает на собственном опыте каждый, кому приходилось отмывать пригоревшую кастрюлю или сковородку.
Чтобы получить в реакции Бутлерова именно те сахара, которые встречаются в клетках — рибозу, глюкозу, — нужно ее как-то останавливать на полпути. В последние годы было обнаружено, что некоторые минералы избирательно связывают и выводят из реакции отдельные сахара, именно те, которые нужны для биохимии. Например, при добавлении растворимых силикатов, таких как Na2SiO3 (силикатный клей), силикат-анион образует комплексы с четырех- и шестиуглеродными сахарами, которые выпадают в осадок и далее не участвуют в реакции. Так накапливаются сахара, имеющие две соседние гидроксильные группы с одной стороны: эритроза, треоза, глюкоза, манноза (подробнее об этом можно прочитать в заметке Александра Маркова на сайте «Элементы», http://elementy.ru/news/431261). Если же в реакционную смесь добавить гидроксиапатит Ca3(PO4)2 × Ca(OH)2, то на его поверхности практически избирательно осаждается рибоза (см. уже упоминавшуюся статью В. Н. Пармона в майском номере «Химии и жизни» за 2005 год)! Еще более эффективно и избирательно осаждают рибозу из реакции Бутлерова соли борной кислоты (бораты). (Ricardo et al, 2013). Соли молибдена превращают ядовитые разветвленные сахара, которые тоже получаются в реакции Бутлерова, в нужные линейные и повышают выход рибозы. Обратите внимание, что все эти вещества — силикаты, бораты, фосфаты и соли молибдена — избирательно накапливаются в грязевых котлах, которые и по другим признакам хорошо подходят на роль колыбели жизни.
Получить азотистые основания оказывается проще, чем сахара. Самые разные воздействия на синильную кислоту или формамид приводят к тому, что их молекулы соединяются в кольца, такие же, как в азотистых основания. Аденин и гуанин образуются из синильной кислоты при замораживании ее водного раствора, ультрафиолетовом облучении или нагревании. Если добавить цианамид или мочевину, то получаются цитозин и урацил. Все четыре азотистых основания образуются с высоким выходом из формамида (NH2CНO) на поверхности частиц оксида титана TiO2 при ультрафиолетовом облучении; аденин, цитозин и урацил — на поверхности глины или оксидов железа при нагревании (см. обзор Constanzo et al., 2007).
Получение нуклеотидов
Чтобы азотистые основания приняли участие в синтезе РНК-подобных полимеров, они должны, естественно, сначала объединиться с сахаром и фосфатом. Этот этап оказался гораздо сложнее, чем получение отдельных сахаров и азотистых оснований. Во-первых, такая реакция идет с выделением воды, и поэтому в водном растворе равновесие сдвинуто в сторону отдельных сахаров и азотистых оснований. Во-вторых, стандартные способы обхода такой проблемы — нагревание сухой смеси веществ или крепкого рассола — здесь не подходят. В этих условиях азотистые основания соединяются с рибозой, но не той стороной — связь с сахаром образует боковая аминогруппа, а не атом азота из кольца. Аденин и гуанин можно соединить с рибозой правильным способом, облучая ультрафиолетом водный раствор азотистых оснований и рибозы, но выход нужного нуклеозида не превышает 1%, а с урацилом и цитозином этот способ вообще не работает. В клетках азотистые основания соединяются с рибозой правильно с помощью сложных ферментов, но нам надо как-то обойтись без них.
Чтобы решить эту проблему, ученые пошли другим путем. Если не удается правильно соединить готовые азотистые основания с рибозой, то можно попробовать создавать эту связь до того, как рибоза и азотистые основания будут достроены. Есть три возможных пути: строить азотистые основания на готовой рибозе, строить рибозу на готовом азотистом основании и строить и то и другое одновременно. Первый путь, кстати, используется в клетках для синтеза адениновых и гуаниновых нуклеотидов из простых предшественников. В экспериментах были достигнуты успехи на всех трех направлениях.
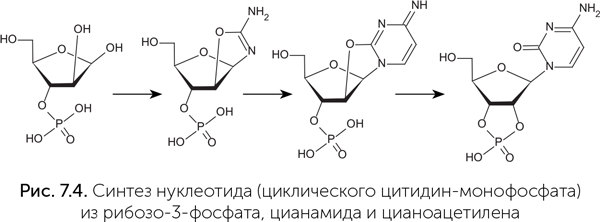
Так, если взять сухую смесь тех веществ, из которых в клетках образуется аденин (это три аминокислоты: глицин, глутамин, аспарагиновая кислота, а также соли муравьиной и фосфорной кислот и рибоза), и запекать ее при температуре 120–150 °C без доступа воздуха, то образуется нуклеотид аденозин-монофосфат с выходом 2–3% и нуклеозид (азотистое основание с рибозой без фосфора) с выходом до 5% (Kritsky et al., 2007). В водном растворе рибозо-3-фосфата при добавлении цианамида и цианоацетилена получается нуклеотид цитидин-монофосфат (рис. 7.4) (Ingar et al., 2003). В обоих этих случаях предшественники азотистого основания сначала реагируют с рибозой, а потом этот промежуточный продукт становится нуклеотидом.
Второй путь начинается с побочных продуктов синтеза азотистых оснований из формамида. Наряду с аденином, гуанином, цитозином и урацилом при этом получаются их формильные производные, имеющие альдегидную (CHO) группу на одном из атомов азота в кольце, чаще всего именно на том, который образует связь с сахаром в нуклеотидах. Эта группа может служить затравкой для построения сахара, если такое вещество (например, 9-формил-аденин) попадет в условия реакции Бутлерова — щелочную среду с формальдегидом. Все хитрости, которые позволяют получить в реакции Бутлерова именно рибозу, а не пригоревшую карамель, здесь тоже работают.
Наконец, возможность получения нуклеотидов по третьему пути, когда ни рибоза, ни азотистые основания не встречаются на промежуточных стадиях, была показана в 2009 году в работе Сазерленда с коллегами из Школы химии Манчестерского университета (см.: Клещенко Е. Реакция начала жизни // Химия и жизнь. 2009. № 7).
Они получили активированные пиримидиновые нуклеотиды (циклические 2',3'урацил- и цитидинмонофосфаты), смешивая в одной системе сразу и предшественники сахаров, и предшественники нуклеотидов, и фосфат. Казалось бы, это крайне расширяет круг возможных химических реакций, а значит, побочных продуктов должно быть больше. Но эксперимент опроверг это предположение.
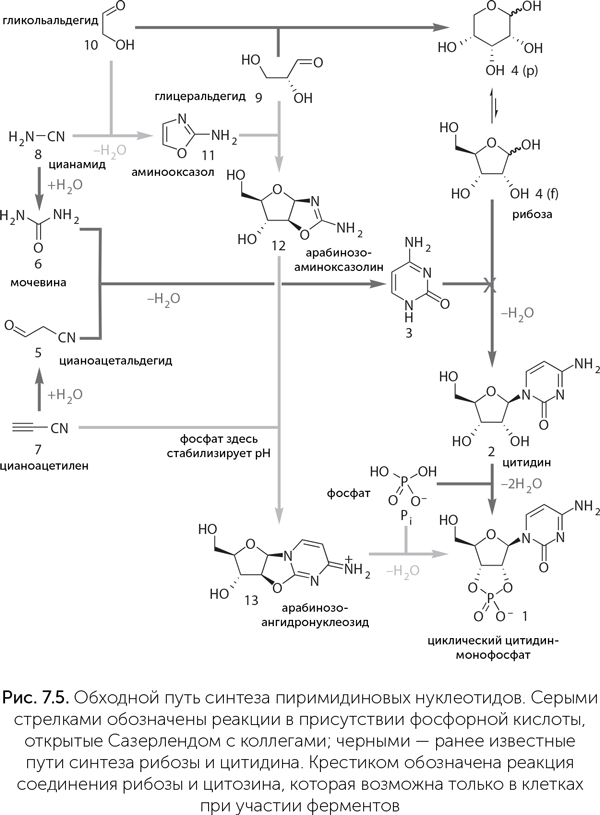
Авторы использовали цианоацетилен (на рис. 7.5 это № 7), цианамид (№ 8), глицеральдегид (№ 9) и гликольальдегид (№ 10). Фосфат облегчает реакции, приводящие в итоге к нуклеотидам, и подавляет другие, побочные. Так, он направляет реакцию цианамида с гликольальдегидом в сторону промежуточного продукта № 11 (2-аминооксазол), а затем реакцию его с глицеральдегидом с образованием продукта № 12 (арабинозо-аминооксазолин). Затем продукт № 12 реагирует с цианоацетиленом, давая вещество № 13 (арабинозо-ангидронуклеозид). В обычном водном растворе при этом повышается pH, и среда становится щелочной, что приводит к распаду промежуточных продуктов и побочным реакциям с цианоацетиленом, но фосфат и тут приходит на помощь, поддерживая среду кислой и направляя реакцию в сторону продукта № 13. Для его превращения в циклический цитидин-монофосфат достаточно подогреть реакционную смесь — все необходимое в ней уже имеется. Катализатором фосфорилирования становится мочевина, образующаяся из цианамида в ходе одной из побочных реакций. Наконец, чтобы избавиться от побочных продуктов этой реакции и превратить часть цитозина в урацил, достаточно осветить раствор ультрафиолетом.
Этот синтез поражает своим изяществом: побочные продукты одних реакций здесь становятся катализаторами последующих, фосфат направляет реакции в нужную сторону задолго до того, как войти в окончательный продукт, а ключевой промежуточный продукт (№ 11) способен к самоочищению и накоплению в высоких концентрациях благодаря своей высокой летучести — он хорошо испаряется из водных растворов при слегка повышенной температуре и конденсируется во время ночных заморозков.
Как написал редактор журнала Nature в предисловии к работе команды Сазерленда, «именно потому, что эта работа открывает так много новых направлений исследований, она на многие годы останется одним из великих достижений пребиотической химии».
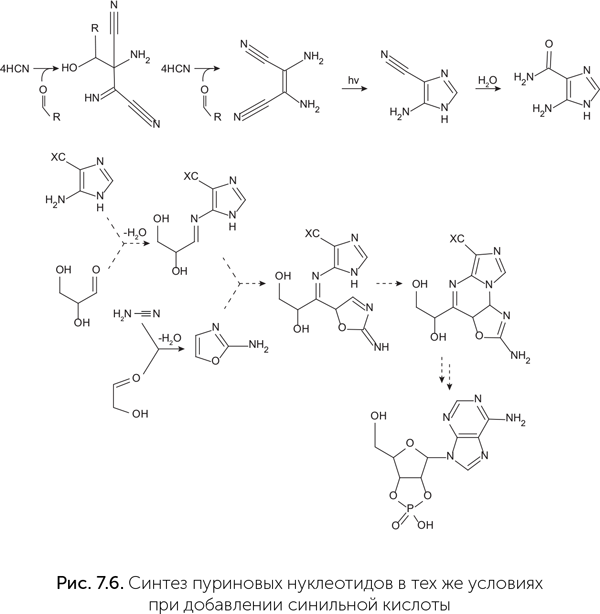
Вскоре в той же лаборатории аналогичным способом были получены и пуриновые нуклеотиды (циклические аденозин- и гуанозин-монофосфаты). Для этого оказалось достаточно добавить в систему синильную кислоту вместо цианоацетилена (рис. 7.6) (Powner et al., 2010).
Цианосульфидный протометаболизм
При всей важности результатов лаборатории Сазерленда и в этих путях синтеза есть к чему придраться. Во-первых, для них требуется последовательное добавление разных исходных веществ: сначала смешать гликольальдегид и цианамид, потом добавить глицеральдегид, а затем — цианоацетилен. Если смешать все сразу, то нуклеотиды практически не получаются. Во-вторых, не очень понятно, откуда взять простейшие сахара (гликольальдегид и глицеральдегид). В реакции Бутлерова они образуются из формальдегида, но тут же превращаются в более сложные сахара. Способов остановки реакции Бутлерова на глицеральдегиде пока неизвестно. В-третьих, для получения нуклеотидов нужны в больших количествах цианамид и цианоацетилен, а в атмосферных процессах они образуются в гораздо меньшем количестве, чем цианид.
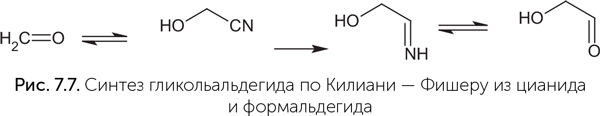
Сотрудники Сазерленда обратили внимание на другие пути получения сахаров. В химии давно известен синтез Килиани — Фишера, в котором цианид реагирует с формальдегидом, давая гликольнитрил (рис. 7.7). На второй стадии гликольнитрил восстанавливается, а на третьей реагирует с водой, выделяя аммиак, и превращается в гликольальдегид. Аналогично гликольальдегид может присоединить следующую молекулу цианида и превратиться в глицеральдегид и далее в более сложные сахара. Первая и третья реакции этого синтеза легко происходят в водном растворе без дополнительных условий, а вот на втором шаге нужны водород и определенный катализатор: палладий на сульфате бария (Pd/BaSO4). Просто палладий и другие металлы, катализирующие восстановление водородом (платина, никель), не подходят, так как вызывают побочные реакции восстановления, приводящие к образованию этиленгликоля и этаноламина. Понятно, что на древней Земле не было палладия на сульфате бария, поэтому синтез Килиани — Фишера долго не привлекал внимания специалистов по предбиологической химии. Однако недавно удалось найти подходящий восстановитель, который наверняка был на древней Земле: это сероводород (Ritson and Sutherland, 2013). В качестве катализатора при этом используются цианидные комплексы меди. Под действием ультрафиолета эти комплексы отнимают электроны от сероводорода (который превращается в серу) и передают их другим молекулам, в том числе гликольнитрилу. Механизм реакции получается сложнее, чем обычный синтез Килиани — Фишера, и кроме сахаров (гликольальдегида и глицеральдегида) получаются побочные продукты, прежде всего аминокислоты: глицин, аланин, серин и треонин.
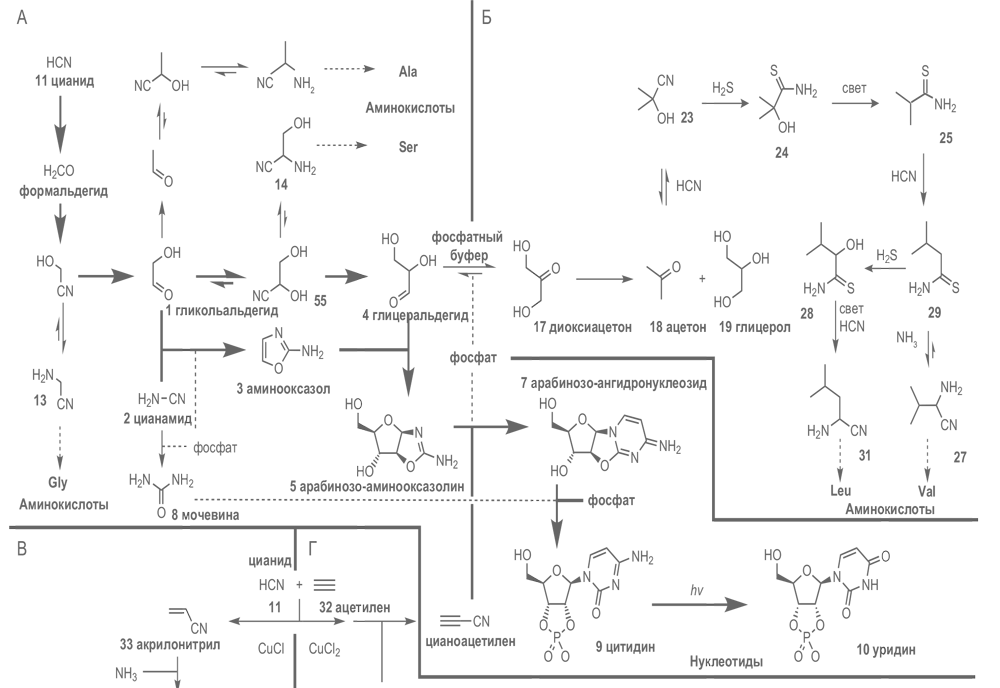
Оказалось, что по условиям эта реакция совместима с синтезом нуклеотидов из простых сахаров, цианамида и цианоацетилена. В присутствии фосфата удается получить нуклеотиды, начиная с цианида и формальдегида, а также возникает дополнительное направление побочных реакций: часть глицеральдегида превращается в диоксиацетон, который восстанавливается до ацетона. Ацетон, присоединяя дополнительные молекулы цианида, дает в итоге еще две аминокислоты, входящие в состав белков, — валин и лейцин (рис. 7.8).
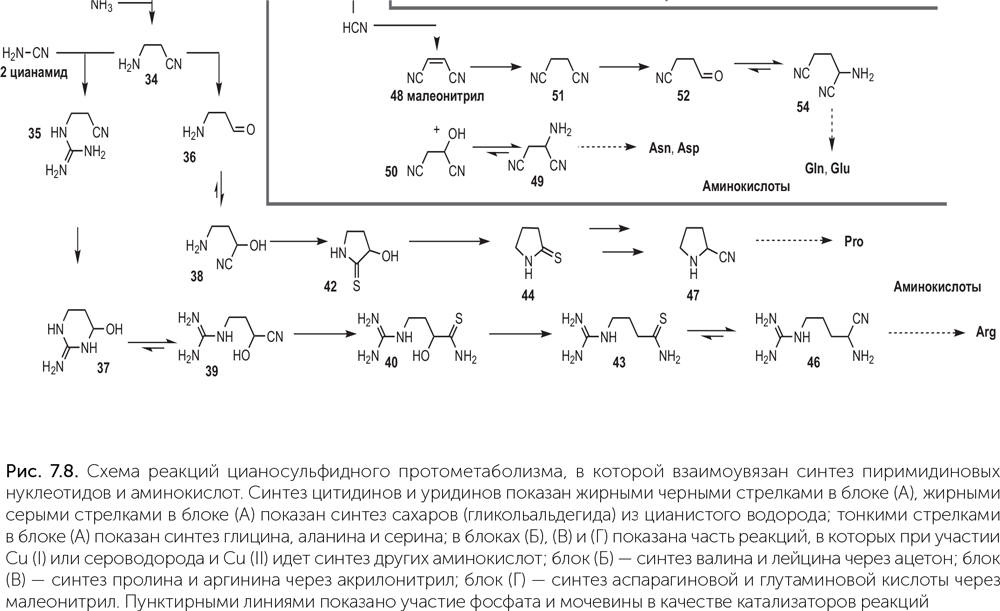
Для получения концентрированных растворов цианамида и цианоацетилена ученые обратили внимание на свойства цианидных комплексов железа. При добавлении синильной кислоты к воде, содержащей соли железа и других металлов, образуются гексацианоферраты, которые при упаривании раствора выпадают в осадок: K4Fe(CN)6 (желтая кровяная соль), Na4Fe(CN)6, Ca2Fe(CN)6 и Mg2Fe(CN)6. При нагревании до 500–800 °C гексацианоферраты разлагаются, давая различные продукты: карбид железа, азот, цианиды калия и натрия. Гексацианоферрат магния при таком разложении дает нитрид магния (Mg3N2), а гексацианоферрат кальция — карбид и цианамид кальция (CaC2 и CaNCN). Если эти продукты прокаливания залить водой, то KCN и NaCN растворяются, соединения кальция разлагаются, давая цианамид NH2CN и ацетилен C2H2, а нитрид магния разлагается с выделением аммиака. При добавлении солей меди ацетилен соединяется с цианидом, давая цианоацетилен (HC ≡ C – C ≡ N) и акрилонитрил (H2C = CH – C ≡ N). На древней Земле такие процессы могли происходить, например, в окрестностях вулкана: сначала синильная кислота из дождей и вулканических газов попадает в озеро с обогащенной железом геотермальной водой, и там накапливаются гексацианоферраты. Потом повышение активности вулкана выпаривает озеро, и разные соли откладываются на его дне кольцами: менее растворимые выпадают в осадок первыми и откладываются ближе к исходным берегам, а более растворимые остаются на самом глубоком месте озерной котловины. Потом вулканическое тепло прокаливает осадки гексацианоферратов, а когда вулкан успокоится и высохшее озеро вновь зальет геотермальной водой с сероводородом, по запекшейся корке солей потекут ручьи из концентрированных растворов цианида и цианамида, в которых пойдет синтез нуклеотидов.
На основе акрилонитрила и цианоацетилена в этих условиях получаются не только нуклеотиды, но и дополнительные аминокислоты. Акрилонитрил присоединяет аммиак и превращается в бета-аминопропионитрил, который через несколько стадий дает пролин и аргинин. Цианоацетилен с помощью меди может присоединить еще молекулу цианида и превратиться в малеонитрил (№ 48). Из малеонитрила образуются аспарагиновая кислота и глутаминовая кислота. Таким образом, из четырех простых веществ (синильная кислота, сероводород, цианамид и ацетилен) получаются не только все четыре нуклеотида, но и десять из двадцати белковых аминокислот. Что еще интереснее, в этой сложной сети реакций практически не образуется никаких веществ, которые не встречались бы в современных клетках, — в отличие от аппарата Миллера и реакции Бутлерова! Значит, цианосульфидные реакции могли определить исходный набор нуклеотидов и аминокислот, из которых строились первые живые системы.

