Противопаркинсонические средства
…Ты чего дрожишь, милейший?
Лорд Сей: Дрожу я от недуга, не от страха.
Шекспир, «Король Генрих VI»
Болезнь Паркинсона (БП) – распространенное нейродегенеративное заболевание, патофизиологической основой которого является гибель дофаминергических нейронов в области компактной части (pars compacta) черной субстанции. Это приводит к классическим двигательным симптомам паркинсонизма: брадикинезии, мышечной ригидности и тремору покоя. В головном мозге существует значительный резерв дофаминергических нейронов, потому симптомы заболевания часто не проявляются до тех пор, пока около 60–80 % дофаминергических нейронов не дегенерируют. Хотя точный механизм, ответственный за гибель клеток, неизвестен, возраст является единственным наиболее постоянным фактором риска. Как следствие, пациенты с БП, как правило, пожилые, и распространенность среди лиц старше 65 лет составляет примерно 1 %. БП вызывает нарушения функции не только экстрапирамидной нервной системы – это полисистемное неврологическое расстройство, вызывающее инвалидизирующие моторные, нейропсихиатрические и вегетативные дисфункции.
Болезнь Паркинсона развивается как дисбаланс между дофаминергическими и холинергическими функциями в ЦНС. Основными путями терапии БП является восстановление баланса между дофаминергическим и холинергическим влиянием.
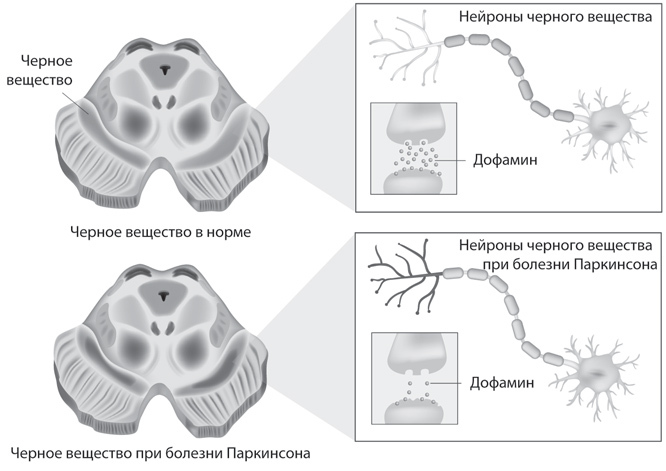
Рис. 17. Основой патогенеза болезни Паркинсона является деградация дофаминергических нейронов в черной субстанции головного мозга, что приводит к дисбалансу между дофаминергической и холинергической системами
Классификация противопаркинсонических средств
ЛС, стимулирующие дофаминергическую передачу в головном мозге:
• предшественники дофамина – леводопа (применяется в комбинации с ингибиторами периферической ДОФА-декарбоксилазы), карбидопа, бенсеразид;
• агонисты дофаминовых рецепторов – апоморфин, ропинерол, ротиготин.
ЛС, блокирующие разрушение эндогенного дофамина:
• ингибиторы моноаминоксидазы B – селегилин;
• ингибиторы катехол-О-метилтрансферазы – энтакапон, толкапон.
ЛС, ингибирующие холинергическую передачу в головном мозге
• тригексифенидил.
Поскольку преобладающая патофизиологическая причина БП – недостаток дофамина в черной субстанции, основным принципом терапии БП является увеличение содержания дофамина в ЦНС за счет введения его извне. Однако дофамин не проникает через гематоэнцефалический барьер (ГЭБ). Это связано с его полярностью и гидрофильностью (не может проникнуть путем пассивной диффузии), и он не имеет специфического транспортера для облегченной диффузии или активного транспорта. В связи с этим назначают предшественник дофамина леводопу, который путем активного транспорта всасывается из ЖКТ и проникает через ГЭБ в ЦНС, где превращается в дофамин под действием фермента дофа-декарбоксилазы. Вместе с тем этот фермент присутствует в стенке кишечника и плазме крови, что приводит к превращению леводопы в дофамин в периферических тканях. Образующийся таким путем дофамин вызывает на периферии побочные эффекты, а кроме того, при этом сокращается пул леводопы, который мог бы проникнуть в мозг для синтеза эндогенного дофамина. В этой связи леводопа всегда назначается с ингибитором дофа-декарбоксилазы периферического действия (DDI) карбидопой или бенсеразидом (не проникающими через ГЭБ) для защиты леводопы от ферментативного разрушения и предотвращения периферических дофаминергических побочных эффектов, таких как тахикардия, аритмии, тошнота и рвота.
Другая группа ЛС, стимулирующих дофаминенергическую передачу, – агонисты дофаминовых рецепторов – непосредственно возбуждает дофаминовые рецепторы в неостриатуме. Неселективные агонисты D1- и D2-рецепторов – перголид, бромокриптин, прамипексол. Препараты этой группы проявляют большую активность в отношении дофаминовых D2-рецепторов (прамипексол стимулирует D2- и D3-рецепторы).
Перголид и бромокриптин относят к производным алкалоидов спорыньи.
Бромокриптин и перголид в основном применяют в сочетании с леводопой, когда не удается получить удовлетворительные результаты, а также в случае возникновения синдрома «включения/ выключения», при котором происходит быстрое восстановление симптомов болезни, связанное с флуктуацией эффективности используемых ЛС.
Прамипексол по эффективности превосходит бромокриптин. Препарат назначают как в виде монотерапии, так и в сочетании с леводопой. По продолжительности действия агонисты дофаминовых рецепторов превосходят леводопу.
Для повышения эффективности леводопы, помимо ингибиторов ДОФА-декарбоксилазы, одновременно с леводопой назначают энтакапон, ингибитор катехол-о-метилтрансферазы (КОМТ), фермента, разрушающего леводопу. Энтакапон не проникает через ГЭБ и снижает скорость метаболизма леводопы в периферических тканях, особенно в условиях компенсаторного повышения активности периферической КОМТ. В итоге поступление леводопы в ЦНС повышается. Блокада КОМТ позволяет снизить дозу леводопы. Полагают, что применение ингибиторов КОМТ уменьшает выраженность синдрома «включения/выключения».
Толкапон, подобно энтакапону, блокирует КОМТ, однако он проникает в мозг, уменьшая метаболизм дофамина в ЦНС.
Селегилин – селективный необратимый ингибитор моноаминоксидазы типа B. Он используется у пациентов с недавно диагностированной болезнью Паркинсона для увеличения содержания дофамина в нейронах за счет предотвращения их ферментативного разрушения МАО В. Это может замедлить прогрессирование клинических проявлений заболевания и отсрочить потребность в терапии леводопой. Селегилин также можно комбинировать с леводопой при прогрессирующем заболевании.
Тригексифенидил – центральный холиноблокатор, блокирует М1-холинорецепторы неостриатума, уменьшая симптомы паркинсонизма. Препарат оказывает умеренное противопаркинсоническое действие – преимущественно уменьшает тремор и мышечную ригидность, мало влияя на брадикинезию.
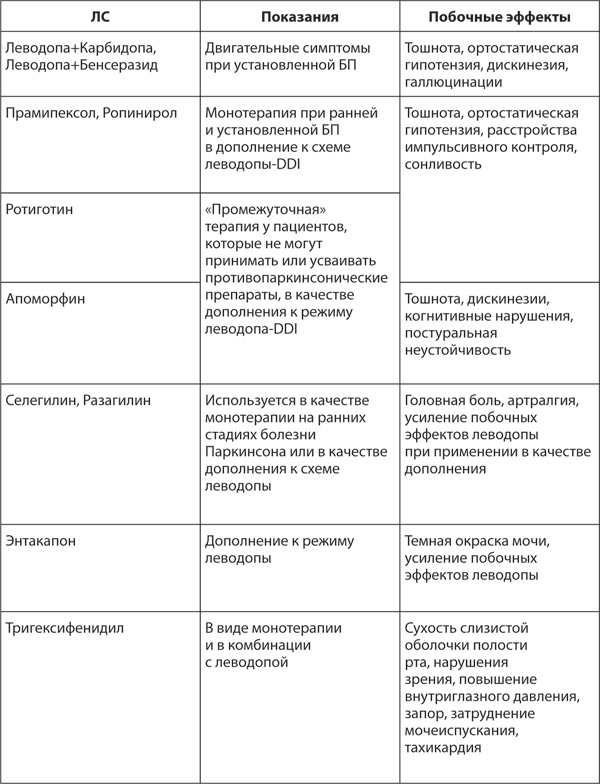
Таблица 15. ЛС против болезни Паркинсона
Вопрос
Мне непонятно: если в основе болезни Паркинсона лежит дефицит дофамина в мозге, почему его нельзя применять для лечения? Почему леводопу, из которой образуется дофамин, можно?
Дофамин является гидрофильным соединением, поэтому путем простой диффузии не всасывается из кишечника и не проникает через гематоэнцефалический барьер. Для леводопы в кишечнике и сосудах головного мозга есть специальный транспортер ароматических аминокислот, который переносит это ЛС соответственно из кишечника в кровь и из крови в мозг, где и образуется дофамин.

