Книга: Лаборатория химических историй. От электрона до молекулярных машин
Назад: Можно обойтись без денежного выражения
Дальше: Глава 12 Лабораторные будни
Глава 11
Всегда ли надо мыть посуду?
Приступая к новому синтезу, химик первым делом берет в руки необходимую стеклянную посуду, которая перед этим была тщательно вымыта и высушена. Помимо этого, исходные реагенты должны быть чистыми. Различные загрязнения могут затормозить реакцию или изменить процесс. Тем не менее, как говорится, жизнь любит иронизировать. Существуют примеры, когда именно загрязнения приводили к открытиям.
Фтор – один из самых активных элементов, он обладает исключительной реакционной способностью, и экспериментальные трудности, связанные с его получением, долгое время казались непреодолимыми. Большинство известных материалов реагируют с ним, многие элементы при соприкосновении с фтором воспламеняются, он может реагировать даже с инертными газами. Французский химик Ф. Муассан в 1886 г. сообщил Парижской академии наук, что ему удалось получить фтор в чистом виде электрохимическим разложением безводной плавиковой кислоты. Для проверки открытия в его лабораторию прибыла авторитетная комиссия – М. Бертло, А. Дебре, Э. Фреми, однако в решающий момент фтор проявил свой "характер" и не захотел выделяться. К чести комиссии следует сказать, что никто не объявил сообщение Муассана ошибочным. Все прекрасно понимали, сколь коварен фтор, и подбадривали Муассана, полагая, что не учтена какая-то экспериментальная мелочь. Вскоре Муассан понял, в чем дело: готовясь к приезду комиссии, он слишком тщательно очистил фтористый водород, и тот перестал проводить ток. Незначительных добавок фторида калия оказалось достаточным, чтобы обеспечить электропроводность. Именно это позволило воспроизвести получение фтора.
Вот другой пример, подтверждающий важность примесей. Полиэтилен – полимер, знакомый всем, – каждый, наверное, держал в руках полиэтиленовый пакет. Полиэтилен получают полимеризацией газообразного этилена:
CH2=CH2 → –(CH2-CH2)n–
(величина n, называемая степенью полимеризации, достигает нескольких сотен тысяч)
Долгое время полимеризацию проводили при давлении 1500–3000 атм и температуре 200–260 ℃. Это весьма жесткие условия. В 1950-х гг. немецкий химик К. Циглер решил найти катализатор, который позволил бы проводить реакцию в менее суровых условиях. Он начал изучать полимеризацию этилена в присутствии алкилов алюминия, но в результате удалось получить только короткоцепные молекулы (n – не более 100 элементарных звеньев).
Как иногда бывает, помог случай. Студент, помогавший Циглеру в работе, недостаточно тщательно вымыл перед опытом автоклав, в котором остались следы коллоидного никеля от предыдущего опыта по гидрированию. Результаты эксперимента, проведенного в "грязном" автоклаве, натолкнули Циглера на мысль, что, помимо алкилов алюминия, в реакционную систему следует добавлять соединения переходных металлов. В результате интенсивных исследований появилась эффективная каталитическая система TiCl4 + Al(C2H5)3, которая позволила проводить полимеризацию при 20 атм и температуре 120 оС. Возникло промышленное производство полиэтилена низкого давления. В 1963 г. за эти исследования К. Циглер (совместно с Дж. Натта) был удостоен Нобелевской премии.
На этом "вмешательство" случайностей не закончилось. В 1975 г. немецкий химик В. Каминский изучал механизм полимеризации этилена. Он проводил спектральное изучение смеси, используемой для полимеризации: [(С5Н5)2TiMe2 + Al(CH3)3] + CH2=CH2. В ней содержался катализатор, близкий по составу к циглеровскому. Вместо TiCl4 Каминский использовал комплексное соединение титана (С5Н5)2TiMe2; соединения такого типа называют металлоценами («родственниками» широко известного ферроцена).
Аспирант, готовивший смеси для измерений, не сумел полностью исключить попадание воздуха в образцы, и в итоге в спектрах при –40 оС были обнаружены сигналы группировки – СН2–, указывающие на присутствие молекул полиэтилена. Полимеризация, протекающая при столь низкой температуре, казалась невероятной. Детальное изучение позволило установить, что причиной исключительно высокой эффективности оказался не металлоцен, а наличие метилалюмоксана – [-Al(CH3) – O-]n-, который образовался в незначительном количестве при гидролизе Al(CH3)3 от действия влажного воздуха. В результате метилалюмоксан совместно с металлоценами стали применять очень широко: активность таких каталитических систем на несколько порядков превосходит активность систем с AlMe3.
В 1990-х гг. японский химик Хидэки Сиракава изучал электропроводность полиацетилена, содержащего чередующиеся одинарные и двойные связи:
– CH=CH – CH=CH – CH=CH – CH=CH–
В соответствии с теоретическими представлениями такой полимер должен был электропроводящим. Образец полимера был высокой чистоты и не содержал примесей, но, к сожалению, даже при сверхвысоком приложенном напряжении его электропроводность была крохотной. Желая немного модифицировать полимер, Сиракава понизил его чистоту и обработал бромом. В результате проводимость оказалась такой, что измерительный прибор перегорел! Электропроводность была в десять миллионов раз выше, чем перед добавлением брома. Конечно, было жаль, что перегорел дорогой измерительный прибор, зато в 2000 г. Сиракава получил Нобелевскую премию (совместно с А. Макдиармидом и А. Хигером) за открытие проводимости в полимерах. Сегодня это целое семейство электропроводящих полимеров, и у некоторых из них проводимость почти такая же, как у металлической меди.
Случалось, что свойства трудноуловимой примеси приписывали основному соединению. Наиболее яркое достижение немецкого химика А. Байера, заложившего основы химии красителей, состоит в том, что он выяснил строение природного красителя индиго, а затем сумел его синтезировать. Один из малоизвестных результатов работы Байера имел неожиданное продолжение. Изучая в 1879 г. строение индиго, ученый получил продукт его окисления – изатин, который, как оказалось, обладал интересным свойством. При смешивании с бензолом в присутствии серной кислоты изатин давал интенсивное синее окрашивание, и потому его стали использовать как очень удобный реагент для качественного обнаружения бензола. Это было заблуждением, но вскоре его развенчали. В 1883 г. другой немецкий химик В. Мейер во время чтения лекции решил показать студентам эффектный опыт, позволяющий обнаружить бензол с помощью цветной качественной реакции, однако у него под руками не оказалось бензола. Не растерявшись, Мейер решил на глазах у студентов вначале получить бензол, а затем подтвердить его наличие, подействовав изатином. Бензол он получил, нагревая бензойную кислоту:
C6H5COOH → C6H6 + CO2
Добавив к свежеполученному бензолу серную кислоту и изатин, он с изумлением обнаружил, что никакого окрашивания нет. Можно себе представить последовавшее за этим веселое оживление студентов, наблюдавших такой неудачный опыт? Тем не менее Мейер сумел сделать из эксперимента очень интересный и, как оказалось, абсолютно правильный вывод. Не вызывало сомнений то, что из бензойной кислоты он получил именно бензол. Более того, бензол, полученный таким образом, был абсолютно чистый, а бензол, который химики обычно использовали для работы, получали из каменноугольной смолы. Следовательно, как предположил Мейер, каменноугольный бензол содержит какую-то примесь, которая дает окрашивание с изатином.
Мейер сумел выделить из каменноугольного бензола соединение, которое он назвал тиофеном. Первая часть названия – "тио" – происходит от греч. θεῖον – "сера", а вторая часть названия – "фен" – указывала на родство с бензолом, спутником которого был тиофен. Группу, содержащую бензольное ядро, С6Н5-, называют фенильной (рис. 11.1).
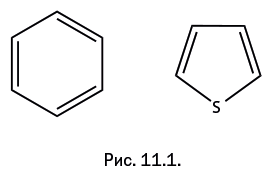
В наше время тиофен рассматривают как загрязнитель бензола, мешающий при проведении некоторых спектральных исследований и молекулярно-массовых измерений. На емкостях с бензолом, предназначенных для таких целей, указывают: «Не содержит тиофена». Вполне естественно, что упомянутый ранее изатин стали использовать для оценки чистоты бензола. Современная химия тиофена представляет собой самостоятельный раздел органической химии. И кстати, на основе тиофена создан электропроводящий полимер, подобный тому, о котором было рассказано немного ранее.
И все же во многих случаях чистота посуды и реагентов необходима. Существует эффектный химический опыт: экспериментатор показывает присутствующим колбу с прозрачной жидкостью, после нескольких легких встряхиваний жидкость полностью превращается в твердую застывшую массу. Для опыта готовят насыщенный раствор в горячей воде кристаллогидрата сульфата натрия Na2SO4•10H2O. После остывания раствор становится пересыщенным, и кристаллизация может начаться от легкого толчка, но не только от этого. Любая пылинка или частичка грязи на стенках колбы может вызвать кристаллизацию до того, как опыт будет продемонстрирован зрителям. В таком случае чистота посуды очень важна.
Существует другой вариант этого эффектного опыта, когда готовить заранее насыщенный раствор не требуется. Небольшое неудобство состоит в том, что показывать мгновенную кристаллизацию можно только на улице в прохладную погоду. В небольшую бутылочку наливают третичный бутанол (CH3)3C-OH. Это вещество совершенно безобидное и имеется во многих лабораториях, температура его кристаллизации +25,5 оС. При комнатной температуре третичный бутанол кристаллизуется неохотно, то есть легко переносит небольшое переохлаждение. Следует, зажав в кулаке бутылочку с третичным бутанолом (чтобы он не охладился преждевременно), вынести его на улицу и дать слегка охладиться в течение 3–4 минут. Если температура воздуха ниже 17 оС, то легкое встряхивание приведет к быстрой кристаллизации всей массы. И, разумеется, бутылочка заранее должна быть чисто вымыта, иначе кристаллизация может начаться самопроизвольно.
В заключение ответим на вопрос, стоящий в заголовке, поскольку у кого-то может создаться впечатление, что загрязнения иногда приводят к Нобелевской премии или к открытию. Нет, все немного не так. Использовать чистую химическую посуду в работе следует всегда, а в процессе интенсивной работы рано или поздно "счастливая" случайность найдет исследователя сама. Важно лишь не упустить момент и найти правильное объяснение.

