Книга: Лаборатория химических историй. От электрона до молекулярных машин
Назад: Глава 7 Тысячелетия спрессованы в минуты
Дальше: Торможение и ускорение процесса
Заметить, не пройти мимо
Далее расскажем о похожей ситуации, возникшей при изучении уже описанного выше класса элементоорганических соединений – металлорганосилоксанов. Напомним, что эти соединения построены из фрагментов RSi-O-M, где R – органическая группа, а М – поливалентный металл. Получение этих соединений проводят в органических растворителях.
Синтезы металлорганосилоксанов, проводимые в разное время независимыми исследователями, приводили к весьма похожим результатам. В процессе синтеза полученные металлорганосилоксаны перегруппировывались – частично, а иногда и полностью. В результате получались продукты структурной перестройки – во-первых, органосилоксан, не содержащий металла совсем, а во-вторых, продукт с повышенным содержанием металла в сравнении с исходным соединением. Это легко обнаружить, если обратить внимание на величину атомного отношения M/Si в исходном и конечном соединении. Примеры показаны на рис. 7.1.
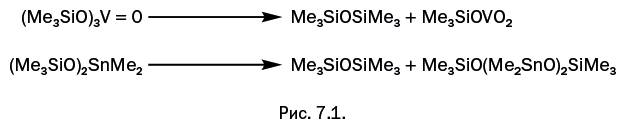
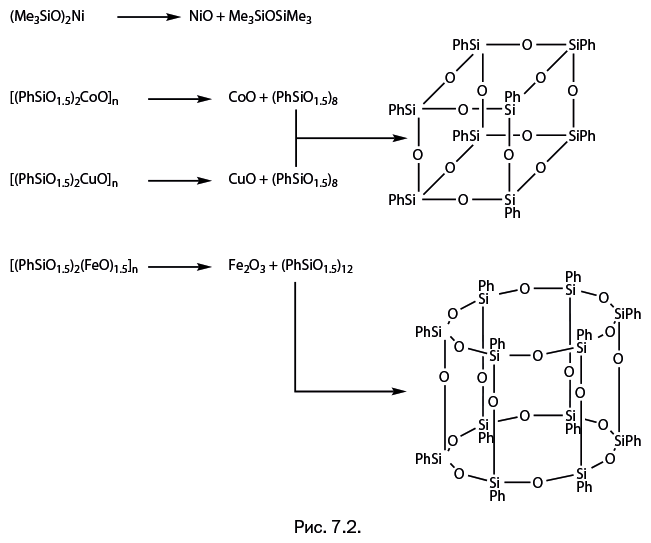
В некоторых случаях, помимо органосилоксанового соединения, не содержащего металл, образовывался оксид металла, вообще не содержащий кремния (рис. 7.2). Процесс затрагивает широкий круг металлосилоксанов, содержащих различное число органических групп R у кремния. Перегруппировка протекает наиболее полно, вплоть до образования оксидов металлов, когда в структуре присутствуют ионы переходных металлов Ni, Co, Cu, Fe. Силоксановый продукт реакции в некоторых случаях представляет собой каркасную структуру (рис. 7.2).
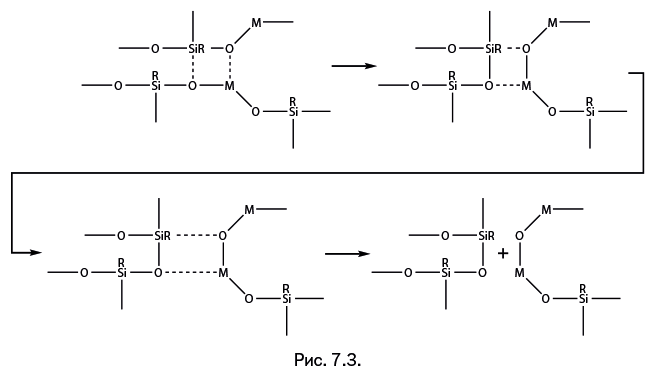
Таких примеров было найдено довольно много. Исследователи обычно описывали их как побочные реакции, которые вызывали скорее досаду, нежели интерес, поскольку мешали получить нужное соединение в достаточном количестве. Но после того, как все результаты свели воедино, постепенно выявились и закономерности. Выяснилось, что в широко известных свойствах ионов металлов заложена движущая сила перегруппировки. Каждый ион металла, находясь в структуре молекулы, старается окружить себя атомами, содержащими неподеленные пары электронов O:, N:, P: и другие (неподеленные электронные пары обозначены точками). Именно эти пары образуют с ионом металла координационную связь: обычно говорят, что металл таким способом заполняет свою координационную сферу. Делает это он весьма настойчиво, но выбирает в соседство атом, который наиболее охотно отдает пару для образования координационной связи электронов. В металлорганосилоксанах присутствует два типа атомов кислорода – во фрагментах Si-O-Si и Si-O-M. Атомы кислорода во фрагментах Si-O-Si крайне неохотно отдают свои электроны соседнему иону металла, а во фрагментах Si-O-M это происходит намного легче. Но существует еще третий фрагмент – М-О-М, и его атом кислорода наиболее охотно отдает свою электронную пару для образования координационной связи. Обратите внимание: он будет отдавать пару не тому иону металла, который рядом (между ними уже есть связь), а тому, который в соседнем фрагменте. Таким образом, в результате перегруппировки в системе возникает больше фрагментов M-O-M, поскольку ионы металлов предпочитают именно их для заполнения координационной сферы. В схеме перегруппировки на первой стадии происходит временное объединение двух звеньев Si-O-M. Образуется переходный комплекс (показано пунктирными линиями), координационные и обычные связи меняются местами, затем переходный комплекс распадается, образуется дополнительное звено Si-O-Si и совершенно новое звено М-О-М (рис. 7.3).