Глава 2
Золотой век
Флемингу и его коллегам приписывают создание первого общедоступного антибиотика, но это не совсем так. Да, их метод работы привел к массовому производству и распространению пенициллина в 1945 году, но, оказывается, люди потребляли антибиотики тысячелетиями, сами того не подозревая. Значимые уровни тетрациклина – антибиотика широкого спектра действия, который используется до сих пор, – были обнаружены в останках мумий Судана, датируемых 350–550 годами нашей эры. (По всей видимости, источником послужило пиво, которое варили в то время.) В пробах, взятых из бедренной кости скелетов позднего римского периода на оазисе Дахла в Египте, также были обнаружены следы тетрациклина (неясно, подавали там выпивку или нет). Неудивительно, что, судя по сохранившимся источникам, уровень инфекционных заболеваний у этих народов был чрезвычайно низким. Наши предки понимали, что антибиотики работают, пусть и не знали, как именно.
Использование антибиотиков в доисторические времена не ограничивается только лишь Африкой. Традиционная китайская медицина снабдила нас множеством антибиотиков, включая артемизинин – лекарство от малярии, которое получают из полыни. На протяжении тысячелетий оно использовалось китайскими травниками для лечения различных заболеваний. Антибиотики окружают нас; бактерии из красных почв Иордании до сих пор применяются для лечения инфекций. Вызов заключается не только в том, чтобы найти их, но и в том, чтобы доказать их безопасность и эффективность для использования в организме человека. И вот с этим уже сложнее.
Поскольку антибиотики вездесущи, не так-то просто определить, что делает антибиотик антибиотиком. Может, все дело в форме молекулы? Или в размере? Может ли препарат, используемый для лечения другого заболевания, например рака или подагры, также служить в качестве антибиотика? Огромное количество химических веществ способно убивать бактерии – кислоты и отбеливатель легко уничтожают любой живой организм, но не все они считаются антибиотиками. Речь идет о веществах, которые избавляют от инфекций, не убивая нас.
Если углубиться в вопрос, большинство экспертов используют термин «антибиотик» для обозначения любой молекулы, производимой микробом или человеком в лабораторных условиях, которая может быть использована в лечении или профилактике бактериальной инфекции. Чтобы заслужить звание антибиотика, молекула должна убивать или подавлять рост по крайней мере одного типа бактерий. Те, что убивают, называются бактерицидными, те, что подавляют рост, – бактериостатическими, и ученые часто спорят о разнице, так как бактерицидные препараты, как правило, более эффективны. Некоторые антибиотики также могут убивать паразитов и грибы, но они не эффективны против вирусов. Вот почему ваш врач не хочет выписывать антибиотики при простуде, ведь ее симптомы обычно вызваны вирусом. (До 1930 года ученые не знали, что бактерии и вирусы – это разные вещи; вирусы размножаются внутри других организмов – растений, животных, человека, бактерий, и в подавляющем большинстве случаев они невосприимчивы к антибиотикам.)
Триумф пенициллина открыл путь для производства десятка новых антибиотиков – колистина, тетрациклинов, аминогликозидов, цефалоспоринов, – фармацевтические компании наперегонки штампуют волшебные лекарства. Пятидесятые годы двадцатого века стали известными как золотой век развития антибиотиков, время, когда прогресс в молекулярной биологии привел к огромному количеству новых лекарств, которые заметно увеличили продолжительность жизни. Половина лекарств, используемых сегодня, была обнаружена именно в то время.
В 1950-м в компании Pfizer работало всего восемь сотрудников по продажам. Всего через год их стало уже сто.
К 1952 году американцы тратили более 100 млн долларов в год на антибиотики широкого спектра действия. Экономика здравоохранения активно развивалась, и впервые ведущие медицинские журналы отказались от политики против коммерческих объявлений. В 1955 году в журнале Journal of the American Medical Association было больше рекламы, чем в журнале Life, американские доктора поняли, что они могут заработать больше денег с помощью фармацевтических компаний, чем занимаясь своими прямыми обязанностями. Год спустя, в 1956 году, венский микробиолог Эрнест Явец подвел итоги прогресса.
«Большинство бактериальных инфекций можно вылечить просто, эффективно и дешево, – отметил он. – Смертность и заболеваемость бактериальными заболеваниями упали так низко, что их уже нет среди важнейших нерешенных проблем медицины».
В 1960-е инфекции стали второстепенным вопросом. Пришло время переходить к более насущным проблемам, таким как рак и болезни сердца.
Однако некоторые умы придерживались менее оптимистичных взглядов на развитие медицины. В 1953 году два ведущих врача того времени – Максвелл Финланд и Луис Вайнштейн – отметили несколько проблем, связанных с новыми лекарствами. Антибиотики могут спасти жизнь, это верно, но они также могут нанести вред практически любому органу в теле человека, причем трудно предсказать точно, когда это случится. Они могут привести к летальному исходу. Финланд и Вайнштейн призвали к осторожности, утверждая, что врачи должны «сомневаться, использовать ли антибиотики в тех случаях, когда показания к их применению либо полностью отсутствуют, либо не строго необходимы, а не то простое или легкое заболевание превратится в серьезное и потенциально смертельное». В частности, хлорамфеникол, антибиотик, который используется для борьбы со вспышками тифа, ассоциирован с апластической анемией, или синдромом серого ребенка.
К концу 1950-х годов побочные эффекты антибиотиков уже были хорошо известны, и ученые сообщали о резком увеличении устойчивых к антибиотикам инфекций. Бактерии незаметно изменились, и теперь чудо-препараты не могли их убить, кроме того, они синтезировали новые ферменты, способные переварить любую молекулу, которая может представлять угрозу для бактерии. Медицина и промышленность эволюционировали в золотую эпоху антибиотиков; однако и бактерии не стояли на месте.
Научные исследования по разработке антибиотиков немного замедлились в 1960-х, так как фармацевтическая промышленность переключилась на более прибыльные заболевания, включая сердечные заболевания и рак, – как раз тогда, когда бактерии начали становиться хитрее. Это стратегическое решение, так же как и более строгий регламент утверждения лекарств, привело к стабильному снижению количества открытий новых антибиотиков. Семидесятые и восьмидесятые годы двадцатого века были временем огромных научных достижений, но в фармацевтической промышленности наступило затишье. В течение этих десятилетий не было открыто ни одного нового класса антибиотиков.
Затем произошел прорыв. Летом 1995 года в журнале Science группа из сорока ученых опубликовала последовательность генома Haemophilus influenzae – бактерии, которая вызывает инфекции легких. Это ключевое исследование впервые предоставило ученым полную информацию о геноме бактерии – той самой, которую изучал Флеминг в экспериментах с пенициллином. Главным автором статьи о бактерии Haemophilus был Крейг Вентер – ученый, предприниматель и популяризатор науки. Исследование, проведенное его группой, привело к смене концепции разработки лекарств. После десятилетий неудач наконец-то наступила эра геномной медицины. Ученые могли использовать результаты исследований Вентера в качестве шаблона для разработки всевозможных препаратов, которые когда-то невозможно было представить.
Научная группа Вентера обнаружили сотни генов, которые могли быть потенциальными мишенями для новых антибиотиков, поэтому исследование вызвало большой интерес со стороны крупных фармацевтических компаний. Лондонская компания Glaxo SmithKline поначалу отошла от разработки антибиотиков, однако затем зацепилась за идею использования генома для разработки лекарств и потратила семь лет (а также около ста миллионов долларов) на исследования с использованием высокопроизводительного генетического скрининга, робототехники, биоинформатики и автоматических детекторов с целью открыть новые антибиотики. В период с 1995 по 2001 год почти полмиллиона соединений были исследованы учеными из Glaxo SmithKline, однако всего лишь пять обладали подходящими для лекарств свойствами, при этом ни одно из них не было полезно для медицины.
Программа провалилась. Использование результатов Вентера для скрининга антибиотиков оказалось тратой времени и вызвало радикальное изменение в стратегии компании. GSK стала гораздо избирательнее в своих инвестициях, финансируя группы химиков, синтезирующих лекарственные соединения, а не гоняющихся за генетическими мишенями. Теперь стратегия заключалась в нахождении меньшего количества активных молекул, но при этом таких, которые наверняка оправдывали непомерные расходы на их получение.
В этом они были не одиноки. Геномный подход оказался потерей времени и средств для ряда компаний, которые потратили миллионы на попытки создания лекарств, исходя из последовательности генома. Геном Haemophilus вызвал всплеск непомерного энтузиазма, который, как мы теперь знаем, не принес никакой пользы. Через десять лет после секвенирования первого бактериального генома не было разработано ни одного лекарства, основанного на полученной из сиквенса информации. Это фиаско отбросило разработку лекарств далеко назад, что хорошо ощущается до сих пор. В результате фармацевтические компании стали гораздо более консервативными. Многие просто отказались от поиска антибиотиков, что и привело к той тревожной ситуации, в которой мы сейчас находимся. Бактерии, вызывающие у людей смертельные инфекции, научились искусно подавлять действие используемых препаратов, и скоро у нас могут закончиться варианты.
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США в настоящее время утверждает в год несколько десятков новых лекарств, называемых также новыми молекулярными субстанциями (NMEs), но среди них очень мало антибиотиков. Число патентных заявок на новые антибактериальные препараты снизилось на треть (34,8 %) с 2007 по 2012 год, а опрос, проведенный в 2016 году, показал, что только 37 молекул – кандидатов в антибиотики находится в разработке, при этом в онкологии таких кандидатов было более 500. Похоже, что разработка новых антибиотиков застопорилась именно тогда, когда они особенно нужны.
Энтони Фаучи – директор Национального института аллергии и инфекционных заболеваний при Национальном институте здоровья США – это человек, благодаря которому исследованиям микробной устойчивости к антибиотикам был присвоен приоритет федерального финансирования. Фаучи сказал мне, что разработка новых препаратов – одна из наиболее важных задач. Но ситуация сложная.
– Правительство не должно играть роль фармацевтической компании, – сказал он, – иначе потребуется построить целую индустрию, и это отвлечет внимание правительства от приоритетных задач, с которыми оно хорошо справляется: от научных открытий и проверки концепций. Нужен другой партнер.
И этот партнер – существующие фармацевтические гиганты.
– Если бы власти попытались создать новый Merck, это стоило бы миллиарды долларов. Контроль качества продукта, производство, фасовка и упаковка готовых лекарств, нумерация партии – люди принимают это как должное, но на самом деле это тонкое искусство, которым в совершенстве владеют фармацевтические компании, а не государство.
Проблема в том, что создание новых антибиотиков не так уж и выгодно. После зарождения идеи нового лекарства необходим длительный процесс разработки, который иногда обходится в миллиард долларов, – только после этого лекарство поступает в продажу. Если результат разработок – Виагра, – то затраты вполне оправданны, потому что доход от продажи такого лекарства составит миллиарды долларов. С антибиотиком прибыль ограничена тремя факторами: их прописывают короткими курсами, назначают только в случае болезни и рано или поздно даже к самому потрясающему новому антибиотику разовьется устойчивость.
А устойчивость точно разовьется.
– Фармацевтические компании не заинтересованы в том, чтобы всерьез вкладываться в разработку антибиотиков, – как-то поделился со мной Фаучи. – Что можно с этим поделать?
Есть несколько вариантов. Большинство из них предполагает ограничение финансового риска и финансовые поощрения.
– Например, можно сказать фармацевтической компании: если вы разработаете антибиотик, то у вас будут налоговые льготы, – говорит Фаучи. – Или будет расширен патент по продаже самого выгодного из ваших лекарств, которое приносит не менее пяти миллиардов долларов. Мы продлим ваш патент на два года, при условии, что компания вложит часть дохода с него в разработку новых антибиотиков.
Но не всегда этого достаточно. Когда фармацевтическая компания оценивает соотношение риска и прибыли, а также рентабельность разработки препарата, они используют показатель чистой приведенной стоимости (ЧПС). Это сумма всех инвестиционных затрат на исследования и разработки, а также ожидаемых в будущем доходов. Для антибактериальных препаратов ЧПС составляет около 42 млн долларов; для большинства других лекарств, в том числе мышечных и неврологических препаратов, она приближается к миллиарду долларов. В последние несколько десятилетий все меньше и меньше компаний готовы идти на риск ради относительно небольшой прибыли.
Фармацевтические исследования и разработки имеют самый высокий показатель неудач для новых продуктов среди всех отраслей, это поднимает важные вопросы: как далеко мы должны зайти в стимуляции производства новых препаратов? Что следует сделать – изменить налоговую политику или патентное право для поощрения фармацевтических компаний к разработке антибиотиков? Должны ли мы создать более короткий путь утверждения новых антибиотиков, который позволит проводить менее длительные клинические исследования для препаратов, которыми лечат инфекции, угрожающие жизни? Пока я размышлял над этими непростыми вопросами, мы с доктором Уолшем начали работу над нашим собственным исследованием, которое, как мы надеялись, поможет решить нарастающую проблему супербактерий.
Allergan была одной из немногих компаний, по-прежнему делающих ставки на антибиотики. Большинство из ее конкурентов, включая Pfizer, Johnson & Johnson и Merck, постепенно сократили финансирование исследований и разработок либо просто сдались. Как отметил Фаучи, «это рискованный процесс, а компании подотчетны акционерам, а не пациентам».
В этом отношении Allergan поистине необычная компания. Они не только обеспечивают стабильное финансирование ученых вроде меня, которые занимаются разработкой антибиотиков, но и наращивают инвестиции и активно пытаются найти выброшенные лекарства – молекулы, которыми владеют другие компании, однако не используют их. Такие, как далба.
В отличие от истории Александра Флеминга, прозорливость которого стала ключом к разработке антибиотика, группа ученых, работавших с далбой, ее создали, а не нашли. Это был продукт гениальной программы для создания более эффективных лекарств, направленной на совершенствование существующих молекул с помощью молекулярного моделирования. Если коротко охарактеризовать данный подход: химики используют компьютерное моделирование для определения того, как существующие химические вещества могут взаимодействовать с опасными патогенами. Добавить атом углерода здесь, убрать атом азота там, посмотреть, что произойдет. Эту область, в которой работают программисты-новаторы и ученые, еще называют синтетической органической химией, и она – дико дорогое «развлечение».
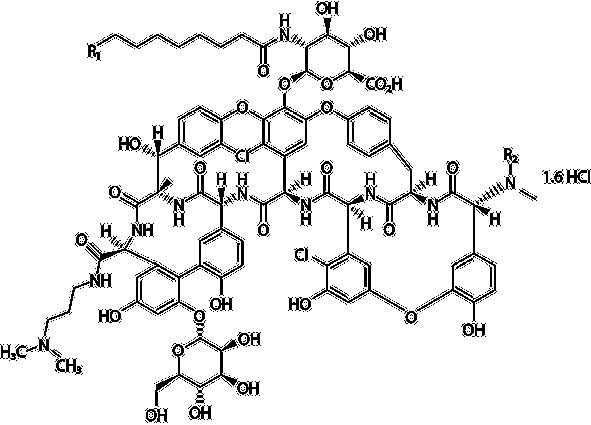
Химическая структура далбаванцина
Антибиотики, которые известны уже много лет, могут быть перестроены для повышения их эффективности. Молекулы раскрывают, разрывают и затем повторно ферментируют, ионизируют, собирают и чистят. Это напоминает работу шеф-повара, который мечтает получить еще одну мишленовскую звезду; химики возятся с микроскопическими ингредиентами, пока не найдут идеальный рецепт. Мне нравится думать о пробирке как о крошечном сотейнике.
Далба была создана путем экстракции крупной молекулы, известной как загадочное соединение A40926, из бактерии под названием Nonomuria, которая была найдена в индийской почве в 1980-е – во времена охоты на антибиотики. Химики удалили из A40926 неуклюже торчащие сахара, аминокислоты и атомы углерода, но делали это очень аккуратно, чтобы не разрушить небольшую щель в молекуле, которая является связывающим карманом. Этот карман позволит их новому препарату искать и разрушать клеточные стенки бактерий, избегая человеческих клеток. Благодаря этому свойству A40926 превратился в бьющий точно в цель мощный антибиотик под названием далба. Разработчики попросили Тома Уолша и меня испытать их детище.
Я часто задавался вопросом, почему Allergan сделал ставку на антибиотики. Было бы наивно полагать, что подобные инвестиции были сделаны исключительно из альтруистических соображений. Компания успешно вывела ряд препаратов на рынок, в том числе мощный антибиотик цефтаролин, но из-за высокой цены его использование довольно ограниченно, да к тому же более дешевый дженерик работает просто отлично. Больница, в которой я работаю, отказывается закупать некоторые лекарства их производства из-за высоких цен. При этом Allergan все же получают хорошую прибыль, будучи владельцами торговой марки «Ботокс», для которого нет альтернативы; в 2018 году препарат принес компании около трех миллиардов долларов.
Но важно понимать, что появление супербактерий полностью меняет расстановку сил. Пациенты и врачи в ужасе, и если Allergan сможет разработать новый эффективный метод лечения, который будет спасать людей от смертельно опасных инфекций, – компания прекрасно понимает, что в таком случае мы вынуждены будем его использовать. Как общество, мы будем готовы заплатить почти любую цену.
Я открыл толстую папку, которую протянул мне Том Уолш. Первые несколько страниц были стандартными внутренними документами Allergan, а вот седьмая страница привлекла мое внимание. Это была краткая история далбы. В декабре 2001 года Lehman Brothers предсказала запуск лекарства в 2005 году с объемом продаж 7,7 млн долларов. Ожидалось, что препарат быстро станет суперпопулярным и в 2006 году принесет компании 65,8 млн долларов, а в 2008-м уже 225 млн. Но, как и в случае со многими другими предсказаниями Lehman Brothers, это было очень далеко от истины. Pfizer провела годы, пытаясь показать, что далба безопасна для лечения инфекций, вызванных супербактериями, но в 2007 году FDA заявило о том, что не считают эти доказательства достаточно убедительными. Необходимо было собрать больше данных, прежде чем антибиотик мог быть утвержден. В 2008 году Pfizer сдалась и объявила о снятии всех торговых заявок на их некогда перспективное лекарство. Спустя пятнадцать месяцев права на него приобрела Durata Therapeutics, а затем сама компания вместе с исключительными правами на далбу была куплена Allergan. В мае 2014 года после продолжительных исследований FDA наконец утвердили далбу для лечения кожных инфекций, но врачи не спешили назначать ее.
Антибиотик, который спасал жизни в 2011 году, может уже не сработать всего несколько лет спустя, и обеспокоенные врачи не хотят рисковать, когда речь идет о жизни и смерти. Супербактерии развиваются, создавая тысячи ферментов, расщепляющих и уничтожающих антибиотики, и мы никак не можем предсказать этот процесс. Они также развивали молекулярные механизмы, известные как эффлюкс, позволяющие выводить из клетки антибиотики и делая лекарства бесполезными. Бактерии могут испортить все старания химиков всего одной мутацией, и столь тщательно разработанный антибиотик теряет силу. Тогда умирающий пациент получает бесполезное лекарство, а многомиллиардные инвестиции испаряются.
Подобные генетические мутации трудно обнаружить, врачи и пациенты, как правило, не подозревают о них до тех пор, пока инфекция не приживается и не начинает распространяться. Иногда мутация обнаруживается только при вскрытии. Я посетил десятки лекций и семинаров по вопросам разработки антибиотиков, но никто не говорит о том, что бактерии мутируют так быстро, что даже самые многообещающие новые продукты не могут идти в ногу со временем. Это – самый охраняемый секрет в медицине.
Чтобы понять, как мы попали на это перепутье и почему Джексон, автомеханик из Квинса, мог умереть от полученной инфекции, полезно будет узнать о самом первом осознанном применении антибиотиков и, главное, о том, какие ошибки были совершены. История экспериментов над людьми содержит много неприятных шокирующих моментов, но помогает понять, почему клинические исследования сегодня проводят именно так, а не иначе и почему будет не так-то просто исследовать далбу.

