Критерий 6. Хронический стресс
Стрессом называется неспецифическая реакция организма на любое воздействие, вызывающее нарушение постоянства внутренней среды. Факторы, способствующие возникновению в организме стресса, довольно многочисленны. Они могут быть внешними (экзогенными): повышенная или пониженная температура окружающей среды, колебания концентрации кислорода в воздухе, травмы, гиподинамия, инфекции, избыток или недостаток питательных веществ, токсины и химические мутагены, ионизирующие излучения и жесткий ультрафиолет. Они также могут быть внутренними (эндогенными): психологический, нейрогормональный, оксидативный стресс, митохондриальный стресс и стресс эндоплазматической сети.
Старение с полным основанием можно назвать хроническим стрессом. С возрастом все большее количество физиологических констант нашего тела выходит за допустимые пределы.
Наиболее явно нарушение постоянства видно по отклонениям от нормы показателей крови – ее pH, уровня глюкозы и других питательных веществ, количества липопротеинов разных классов, концентрации витаминов, макро- и микроэлементов. Возникающие отклонения вызывают активизацию компенсаторных процессов, которые зачастую приводят к большему повреждению, чем сами отклонения.
Стресс-гормоны и старение
Говоря о причинах хронического физиологического стресса у пожилых людей, нельзя не упомянуть постоянное повышение, особенно в утренние часы, уровня стресс-гормона кортизола. Воспалительные процессы в гипоталамусе, возникающие при старении, провоцируют выработку избыточного адренокортикотропного гормона, который ускоряет образование кортизола корой надпочечников. Этот жизненно важный стероидный гормон необходим, чтобы при остром стрессе быстро мобилизовать поступление в кровь запасов глюкозы, аминокислот, липидов, подавить воспалительные процессы. Его роль также важна в процессе пробуждения – с первыми лучами солнца уровень кортизола повышается, затем он увеличивает уровень глюкозы, и наш мозг просыпается. В то же время, понижая выработку инсулина, высокая концентрация кортизола длительное время поддерживает повышенный уровень глюкозы в крови. Вызывая сужение сосудов, он может нарушать питание тканей и вызывать артериальную гипертензию. Кортизол подавляет функцию гиппокампа (отдела головного мозга, отвечающего за память) и способствует уменьшению его размеров. В результате нарушений в гиппокампе у пожилых людей снижена память, способность к обучению, повышена раздражительность и склонность к депрессиям.
Давно известно, что у пациентов, регулярно проходящих лечение кортизолом (обычно они получают в десятки раз бо́льшие дозы кортизола, чем физиологическая норма), появляются признаки ускоренного старения кожи и преждевременно развиваются возрастзависимые патологии – остеопороз, ожирение, ослабление иммунной системы. Кстати, тихоокеанский лосось, приходя на нерест, активизирует программу самоубийства, очень похожую на ускоренное старение, в основе которой – выработка высоких доз все того же кортизола. Погибшие животные служат субстратом для размножения бактерий и простейших. Последние приводят к вспышке численности зоопланктона, который является источником пищи для молоди в холодных, обедненных питательными веществами северных ручьях. Очевидно, что в человеческом обществе такое «самопожертвование», заложенное природой, совсем не нужно.
Хотите похудеть? Снижайте уровень кортизола
Доказано, что хронически высокие показатели кортизола провоцируют набор веса, особенно в области живота и поясницы. А это означает, что не важно, как много вы упражняетесь и насколько правильно питаетесь – вы не потеряете вес, если уровень кортизола у вас в крови будет оставаться высоким, так как это делает организм нечувствительным к инсулину.
В ходе одного исследования была проанализирована взаимосвязь между уровнем кортизола, чувствительностью к инсулину и количеством висцерального жира у мужчин. Мужчины с большим количеством висцерального жира имели повышенную выработку кортизола на протяжении всего дня, а также пониженную чувствительность к инсулину по сравнению с теми, у кого количество висцерального жира было меньше. Напротив, подкожный жир не обнаружил никакой связи с уровнем кортизола или инсулина.
Чтобы понизить уровень кортизола, нужно соблюдать следующие простые правила: уменьшить потребление кофеина (его много в крепком чае или кофе), высыпаться, регулярно выполнять физические упражнения, заниматься медитацией и слушать релаксирующую музыку, не допускать резкого повышения уровня сахара в крови, сбалансировать диету по антистрессовым микронутриентам (витамины группы В, магний, цинк, хром III, альфа-липоевая кислота). В некоторых случаях полезно принимать противострессовые препараты из таких растений, как женьшень, лимонник, астрагал, родиола розовая.
Окислительныйстресс
Окислительным стрессом можно назвать устойчивое превышение уровня окислителей в клетке над уровнем восстановителей. Под окислителями прежде всего понимаются активные формы кислорода и азота – так называемые свободные радикалы (рис. 27). Окислительный стресс могут вызывать как внешние стресс-факторы (радиация, тяжелые металлы, гипоксия, гипероксия), так и внутренние процессы, связанные со старением, – дефекты митохондрий, хроническое воспаление, снижение количества антиоксидантных ферментов и веществ – перехватчиков свободных радикалов.
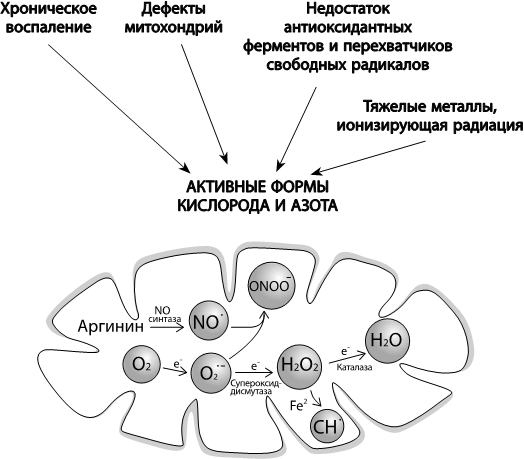
Рис. 27. Причины окислительного стресса
УЗНАЙ БОЛЬШЕ
В основном свободные радикалы в клетке образуются в процессе клеточного дыхания в митохондриях, однако некоторое их количество может возникнуть в цитоплазме, на поверхности клеток или в особых структурах клетки, таких как пероксисомы и микросомы.
Свободные радикалы в определенном количестве необходимы – они помогают клеткам печени и почек окислить и нейтрализовать токсины, клеткам иммунной системы – атаковать инфекционные агенты, синтезировать стероидные гормоны и другие гормоноподобные вещества, стимулируют защитные реакции клетки – остановку клеточного цикла, необходимую для починки повреждений, образование ферментов репарации ДНК, белков теплового шока и антиоксидантных ферментов.
Однако в случае хронического повышения уровня свободных радикалов, особенно в условиях избытка ионов железа и меди, повышающих их токсичность, возникает окислительный стресс, приводящий к повреждению клеточной ДНК, белков и мембран (рис. 28).
Окислительный стресс приводит к накоплению повреждений и мутаций в митохондриальной и ядерной ДНК, к нарушению регуляции активности генов, укорочению концов хромосом, сшиванию между собой молекул белков, липидов и ДНК с образованием токсичных агрегатов – амилоида и липофусцина.
На тканевом и системном уровне окислительный стресс вызывает гибель клеток (апоптоз и некроз), клеточное старение и хроническое воспаление.
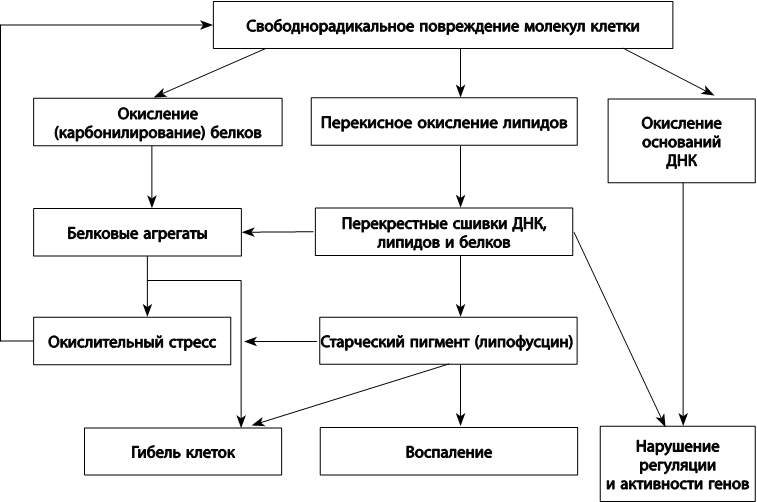
Рис. 28. Последствия окислительного стресса
Протеотоксический стресс
Любой белок в клетке и межклеточном матриксе имеет риск подвергнуться различным патологическим модификациям, нарушающим его структуру и функцию. Это может быть:
1) необратимое окисление (так называемое карбонилирование);
2) неферментативная реакция с глюкозой и продуктами ее окисления – гликирование и гликоксидация с образованием конечных продуктов гликирования;
3) сшивание белков с продуктами окисления жиров – липидными пероксидами, а также белков между собой и с ДНК.
Поврежденные таким образом белки в норме подвергаются утилизации при помощи специальной структуры клетки – протеасомы, которая нарезает ненужные белки на кусочки либо особыми цитоплазматическими и митохондриальными ферментами. Активность этих ферментов и структур клетки с возрастом падает. Еще один способ избавления от агрегатов поврежденных белков или целых клеточных органелл – аутофагия. В результате нарушения регуляции определенных генов с возрастом снижается активность процессов утилизации белковых агрегатов (микроаутофагия) и поврежденных митохондрий (митофагия). Как следствие происходит накопление старческого пигмента липофусцина, запускающего каскад неблагоприятных для нашего долголетия изменений и способствующих окислительному стрессу избежавших утилизации поврежденных митохондрий.
Кроме уничтожения нарушенного белка, отдельные повреждения белков подлежат восстановлению предназначенными для этого ферментами. При клеточном старении отмечается снижение уровней как утилизирующих, так и восстанавливающих ферментов. Особенно выраженные снижения активности отмечаются в митохондриях. Искусственная активация генов этих ферментов в экспериментах на модельных организмах приводит к увеличению продолжительности жизни и повышению устойчивости к окислительному стрессу. Таких же результатов удается достичь, работая со старыми клетками человека в лабораторных условиях.
Стоит отметить, что восполнение запасов цинка в организме пожилых людей приводит к снижению накопления окисленных белков и к активации ферментов, восстанавливающих функцию поврежденных белков.
Белок с естественной пространственной укладкой, как правило, растворим в воде, поскольку он несет на своей поверхности заряженные аминокислотные группы, тогда как окисленные белки утрачивают заряд, становятся водоотталкивающими и слипаются в агрегаты. Накопление агрегатов, в зависимости от места их образования, вызывает:
1) стресс в эндоплазматической сети (особой структуре, имеющейся в каждой клетке и служащей для сортировки и транспортировки вновь образованных белков), который выливается в нечувствительность клетки к инсулину, системное воспаление, клеточное старение или гибель клетки;
2) митохондриальный стресс, приводящий к порочному кругу, в результате чего поврежденная митохондрия выделяет еще большее количество свободных радикалов.
При хроническом физиологическом стрессе тоже наличествуют все характеристики, присущие критерию старения.

