Энтропия и вероятность
Людвиг Больцман (1844–1906) родился в Вене и учился в Венском университете, где в 1867 году он и получил докторскую степень. Больцман был импульсивным человеком, менявшим (по выбору) одну академическую специальность за другой – за почти сорокалетнюю карьеру в общей сложности семь раз.
С начала 1870 года Больцман был научной суперзвездой и пользовался огромным спросом. В 1894 году министру культуры Австрии пришлось предложить Больцману зарплату, которая была больше, чем у любого другого профессора в Австрии, чтобы тот согласился преподавать теоретическую физику. Прежде Больцман уже дважды был преподавателем в Венском университете, с 1867 по 1869 год как доцент и с 1873 по 1876 год как преподаватель математики. Тем не менее в 1900 году он в третий раз покидает университет.
В 1902 году он последний раз вернулся в Вену, вновь став преподавателем теоретической физики; все два года его отсутствия должность была вакантна. Хорошо зная его характер, австрийские власти позволили Больцману вернуться взамен на его обещание никогда не устраиваться на любую другую работу за пределами Австрии. Больцман сдержал это обещание. Личность Больцмана была такова, что он всегда переходил из одной крайности в другую: сам он шутил про свой характер, говоря, что родился между Масленицей и Пепельной средой – между празднованием и епитимией, так сказать. Сегодня врачи, скорее всего, поставили бы Больцману диагноз «биполярное расстройство» (впрочем, у него были и другие проблемы со здоровьем: астма, мигрень, плохое зрение и стенокардия).
Больцман был исключительным теоретиком (что любопытно, ведь при этом он был профессором экспериментальной физики в университете города Грац, Австрия, с 1876 по 1890 год – его самое долгое пребывание на одной должности). Вот как он сам описывал себя: «Я теоретик с головы до пят. Мои мысли и дела всецело направлены на развитие теории. Ни одна жертва в ее славу не была бы слишком велика, ведь теория – смысл всей моей жизни».
Несомненно, Больцман был только вторым по значимости теоретиком после Максвелла. Но Больцман был известен не только благодаря своей смелости в исследовании теории, но и исключительным педагогическим талантом, чем никогда не мог похвастаться Максвелл. Более того, он внимательно относился к своим студентам и обращался с ними как с равными, ведя дискуссии и позволяя даже критиковать себя.
В 1866 году, в возрасте 22 лет, Больцман нап исал первую значимую научную работу, которая называлась «О механическом значении второго начала». В ней он противопоставлял неоднозначной природе второго начала надежную фигуру принципа сохранения энергии, описанного в первом начале. Он попытался дать общее доказательство второго начала и связал его с классической механикой, описанной Ньютоном.
Хотя Максвелл сам не формулировал второе начало, он рассматривал этот подход как в корне неверный, поскольку для него второе начало было чистой воды вероятностным, статистичным по своей природе и поэтому не имело основы в виде чисто классического описания с точки зрения механики. Больцман в своем заблуждении был не одинок. Клаузиус также пытался вписать второе начало в принципы механики. Очень скоро Больцман понял, что этот подход в корне неверен, в то время как Клаузиус даже после несколько попыток не был разубежден.
Первую такую попытку Клаузиус предпринял в 1862 году, представив «дезинтеграцию», которая должна была стать мерой значительности разделения между атомами и молекулами в объекте. В 1870 и в 1871 годах он публикует работы, которые должны были описать второе начало с точки зрения механики. На его последнюю работу быстро откликнулся Больцман, заявив в своей работе, что Клаузиус по сути повторил его опыт 1866 года. В следующей работе в 1872 году Клаузиус любезно ответил, что «чрезвычайный спрос» на его работы затрудняет ознакомление с текущей научной литературой. Тем не менее все эти подходы были ошибочны, и хотя Клаузиус не достиг успеха со статистической природой второго начала, это смог сделать Больцман, продолжив тем самым работу, начатую Максвеллом.
В 1868 году Больцман не упоминал работу Максвелла, скорее всего, потому, что он все еще учил английский (в частности, чтобы иметь возможность прочитать оригинал работы Максвелла по электромагнитной теории), чем из-за недосмотра с его стороны. Однако спустя два года после этой неудавшейся попытки, и уже будучи знакомым с работой Максвелла по распределению скоростей атомов газа, Больцман нашел то, что искал – объяснение энтропии и второго начала с точки зрения вероятности и статистики.
Вспомните, что закон Максвелла описывает возможный диапазон, или распределение скоростей атомов в идеальном газе в равновесии при определенной температуре. Мы уже выяснили, что «энергия движения» является кинетической и объект, обладающий скоростью, должен находиться в движении и, следовательно, обладать кинетической энергией. Следовательно, распределение Максвелла также описывает распределение атомов идеального газа по кинетической энергии в состоянии равновесия. Другими словами, Максвелл описывает распределение кинетической энергии идеального газа в равновесии – вот что понял Больцман. В 1868 году Больцман смог показать, что идея распределения может быть расширена на полную энергию системы в равновесии – и кинетическую, и потенциальную. Фактически, применяя более общий подход к проблеме, Больцман также смог вывести распределение Максвелла для находящейся в равновесии системы атомов идеального газа.
Итак, пока атомы газа данной системы движутся, сталкиваясь друг с другом и со стенками контейнера, внутри которого они находятся, когда система пребывает в равновесии, система в целом принимает значения энергии из диапазона, задаваемого распределением Больцмана. Каждая из этих энергий описывает систему как пребывающую в некотором микросостоянии. Каждое микросостояние описывается всеми положениями атомов газа и соответственно их скоростями в данный момент времени. С течением времени система переходит из одного микросостоянии в другое и, если дать ей достаточно времени, испытает все доступные микросостояния. Однако она не будет переживать каждое микросостояние с одной и той же частотой; более вероятные состояния будут возникать чаще. Согласно распределению Больцмана, микросостояния с более низким уровнем энергии – более вероятные, а вероятность их возникновения определяется вероятностью Больцмана.
Распределение Больцмана, вероятность Больцмана и микросостояния – основополагающие идеи статистической механики, которая позволяет нам правильно рассчитать определенные параметры системы, причем не только системы атомов газа, но и всех классических систем (в отличие от квантовых). Такие величины, как давление и температура, можно рассчитать, иногда с помощью компьютерного моделирования. Итак, несмотря на то что мы не можем видеть атомы, их хаотичное движение и возникающие в результате микросостояния, с помощью методов Больцмана и аналогичных им мы можем правильно описать многие вещи, которые мы наблюдаем в повседневной жизни.
Когда вы смотрите на какой-либо объект, вы наблюдаете его физическое состояние, или макросостояние. Опять-таки, давайте снова вспомним о шарике, наполненном воздухом. Вы не можете видеть воздух, в котором молекулы движутся, сталкиваясь друг с другом и со стенками шарика. Вы видите форму (объем) шарика и можете измерить его температуру. В этом случае макросостояние вашей системы прекрасно описывается свойствами, которые вы можете наблюдать и измерить: температурой и объемом. Тем не менее микросостояния, возникающие в результате столкновения молекул, скрыты от глаз.
Таким образом, множество микросостояний являются скрытыми состояниями системы, в то время как макросостояние – это состояние системы в целом, с физическими свойствами, которые мы можем увидеть и измерить. В некотором смысле макросостояние – это грубый, нечеткий вариант системы.
Вот как это примерно выглядит: когда я был ребенком, я любил трясти коробки с моими новогодними подарками. Когда я тряс коробку, содержимое болталось из стороны в сторону (часть его разбивалась) и по сути переходило из одного микросостояния в другое. Я никогда не мог видеть все эти встряски (и все эти «микросостояния»), зато я мог видеть среди всех этих трясок то, что никогда не менялось – коробку в красивой обертке с бантиком наверху: ее «макросостояние» всегда было одинаковым, хотя «микросостояния» внутри коробки изменялись с каждым потряхиванием.
Различия между макросостоянием и микросостояниями, составляющими его, позволяют нам прийти к более фундаментальному пониманию энтропии, большему, чем «отношение тепла к температуре». Больцман продемонстрировал, что чем больше микросостояний доступно системе, тем выше ее энтропия. Вспомним, что спонтанный процесс возникает без помощи извне или приложения работы; он просто происходит. Согласно Клаузиусу, спонтанный процесс возникает, поскольку он предпочтителен с точки зрения энтропии; это то направление, которое приводит к увеличению энтропии и поэтому является предпочтительным.
Используя концепцию микросостояний Больцмана, мы также можем утверждать следующее: спонтанный процесс возникает, потому что он приводит к появлению большего количества микросостояний. Ярчайший тому пример – смешивание жидкостей. Представьте, что происходит, когда в чашку с кофе наливают сливки. Мы можем вообразить, как сливки собираются наверху чашки, никогда полностью не смешиваясь с кофе. Однако второе начало уверяет нас, что в природе кофе и сливки будут стремиться увеличить их общую энтропию.
Таким образом, вместо того чтобы держаться вместе наверху чашки, сливки движутся через кофе. Этот процесс диффузии дает сливкам доступ к гораздо большему пространству в чашке, чем если бы они оставались наверху. Более того, то место наверху чашки, где раньше находились сливки, теперь также доступно для кофе. Получается, что диффузия открыла и сливкам, и кофе доступ к большему пространству в чашке. Это означает, что у обоих возникло больше микросостояний, и в результате энтропия системы максимизировалась.
Итак, означает ли это, что вы никогда не увидите, как сливки спонтанно отделяются от кофе? Если коротко, то да. Причина этого в том, что существует только одно микросостояние, в котором сливки и кофе абсолютно разделены, и множество микросостояний, где они смешиваются (в той или иной мере). В конце концов, это связано с вероятностью: чем больше способов ведет к возникновению явления (смешивания) по сравнению с другим (отделением), тем более оно вероятно. В нашем примере вариантов смешивания гораздо больше, поэтому оно более вероятно (точно так же в лотерее гораздо больше комбинаций, которые ведут к проигрышу, чем к выигрышу).
Однако Больцман никогда не говорил, что шансов нет. По сути, существует ненулевая вероятность того, что однажды кофе и сливки не смешаются. Но этот шанс настолько мал, насколько много способов смешения. Таким образом, когда встречаются частицы кофе и сливок, сталкиваясь друг с другом, они проводят больше времени в микросостояниях, результатом чего является смешанное макросостояние (физическое состояние), которое мы видим.
Давайте рассмотрим последний пример – нечто более понятное, чем сталкивающиеся частицы, которые создают невидимые микросостояния. Рассмотрим колоду карт.
Первое, что вы заметите в новой колоде карт – все карты расположены по порядку: карты каждой масти следуют одна за другой, от туза до короля. В терминах, о которых мы говорили, это будет «упорядоченное» микросостояние колоды. Теперь представим, что мы поместили нашу колоду в устройство для тасования карт. Когда карты тасуются, колода изменяет начальное микросостояние на другое, потом на третье и так далее. Мы можем представить нечто подобное в случае с газом, где постоянное движение атома вынуждает систему «перетасовывать» микросостояния.
Итак, остановим тасовщик и посмотрим на карты. Как мы видим, текущее микросостояние – «беспорядочное». Все масти перемешаны друг с другом, последовательность нарушена – ничего общего с тем, какой была колода до перемешивания. Положим карты в тасовщик опять и продолжим перемешивать, периодически проверяя новые микросостояния. Конечно, мы предполагаем, опираясь на опыт, что каждый раз, когда мы наблюдаем новое микросостояние, карты находятся в беспорядке. Сколько бы мы ни перемешивали карты, скорее всего, они не вернутся в исходное микросостояние. Нельзя сказать, что это невозможно – скорее, существует гораздо больше способов перейти колоде в новые микросостояния, а не в первоначальное. Понятно, что у колоды карт куда больше беспорядочных микросостояний, чем упорядоченных. Поэтому неупорядоченное макросостояние, или фаза, обладает большей энтропией, чем упорядоченное, и поэтому его возникновение более предпочтительно.
В целом так себя ведет и природа, не только колода карт. Представьте, как вода в виде льда (твердое состояние) тает и превращается в жидкость благодаря теплу, получаемому из окружающей среды, а затем – в пар (газ) благодаря дальнейшему сообщению тепла. В каждой из последовательных фаз добавление тепла приводит к росту скорости молекул воды. В твердом веществе молекулы воды фактически не двигаются. Как только лед начинает таять, молекулы воды приходят в движение, по мере перехода в жидкое состояние их скорость возрастает. Наконец, с добавлением еще большего тепла молекулы воды переходят от покачивающихся движений к прямым столкновениям друг с другом, и вещество переходит в состояние газа. Увеличение активности движения от твердого, жидкого и до газообразного состояния приводит к увеличению количества микросостояний для каждой из последовательных фаз. Следовательно, как и для колоды карт, – большее количество микросостояний означает бо2льшую энтропию.
Часто рост скорости молекул соотносят с увеличением неупорядоченности системы. Твердое агрегатное состояние является наиболее упорядоченным, а состояние газа – наиболее неупорядоченным. Такое понимание тем удобнее, что также хорошо согласуется с нашей аналогией с колодой карт. Однако оно не учитывает физическое явление, происходящее с далеко идущими последствиями: добавление энергии в форме тепла (q) позволило системе увеличить количество микросостояний (тем самым сменяя фазы в нашем примере выше). Фактически, если мы обозначим изменение (в нашем случае рост) энтропии как ΔS, мы можем записать формулу
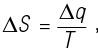
отражающую термодинамические процессы, которые мы наблюдали ранее.
Во времена Больцмана идея, что вещество состоит из малых невидимых частиц, которые сегодня мы называем атомами, еще не была главенствующей. Нетрудно представить, что теории Больцмана, предполагавшие их существование, могли встретиться с некоторым сопротивлением. Больцмана жестко критиковали, но он отказывался отступать. В 1898 году Больцман опубликовал второй том «Лекций по теории газа». Так что мы можем получить представление, насколько стойко он был убежден в существовании атомов:
«По-моему, это была бы большая трагедия для науки, если бы [кинетическая] теория газов была предана забвению из-за сиюминутного враждебного отношения… Я понимаю, что я всего лишь отдельный человек, бессильно сражающийся с духом времени. И все равно в моих силах сделать такой вклад, что, когда [кинетическую] теорию газов возродят к жизни, заново придется открывать не так уж много».
Среди самых ярых противников Больцмана был Фридрих Вильгельм Оствальд (1853–1932). Он был противником всех теорий химии и физики, которые подразумевали существование атомов, особенно кинетической теории газов. Для Оствальда объединяющей научной концепцией была энергия. Он считал энтропию распадом энергии (что было близко к концепции Томсона), не имевшим ничего общего с движением атомов и микросостоянием систем. Оствальд считал атомы артефактами математической теории, а не проявлениями физической реальности.
Другой противник атомной теории Эрнст Мах (1838–1916) не подписался бы и под объединяющим концептом энергии, который защищал Оствальд. Мах просто не мог принять идею существования атомов, потому что не видел доказательств в пользу их существования. С оглядкой на микроскопическую интерпретацию энтропии у Больцмана Мах писал: «По моему мнению, корни этой теоремы [об энтропии] лежат гораздо глубже, и если привести в соответствие молекулярную [атомную] гипотезу и теорему об энтропии, это было бы удачей для гипотезы, но не для теоремы об энтропии».
Летом 1905 года Больцман читал серию лекций в Калифорнийском университете в Беркли. Он был на пике славы. Студенты стремились попасть на его лекции, а коллеги искали его научного совета. По возвращении в Вену (не имея понятия о работе Эйнштейна 1905 года) Больцман описал свое путешествие в книге «Путешествие одного немецкого профессора в Эльдорадо».
В начале 1906 года Больцман был в отпуске со своей женой и дочерью недалеко от побережья итальянского города Триест. В очередной раз борясь с депрессией, Больцман повесился на оконной раме, пока женщины были на пляже. Вернувшись, его дочь обнаружила его мертвым. Людвиг Больцман похоронен на Центральном кладбище его родного города Вены. На его могильной плите написано выражение для энтропии через число микросостояний системы:
S = k ln W,
где S – это полная энергия системы, k – постоянная Больцмана, а W – общее число микросостояний, соответствующих данному макросостоянию системы.

