АТФ-синтаза: соединение ЭТЦ и окислительного фосфорилирования
АТФ-синтаза (аденозинтрифосфатаза, или комплекс V) – важный фермент, являющийся финальной ступенью в длинной цепи событий, кульминацией которых становится синтез АТФ.
Именно этот фермент соединяет протонный градиент (возникающий в результате функционирования ЭТЦ и восстановления кислорода до воды) с фосфорилированием – процессом добавления фосфатов к аденозиндифосфату (АДФ), который превращается в аденозинтрифосфат (АТФ). Все это называется окислительным фосфорилированием.
АТФ-синтаза, будучи крупным ферментом, представляет собой мельчайшую из известных нам машин. В интернете можно найти несколько удачных анимированных иллюстраций ее работы, и я советую вам не пожалеть времени и посмотреть их. Фактически АТФ-синтаза – это роторный двигатель, состоящий из множества крошечных белковых деталей. АТФ-синтаза состоит из двух основных компонентов – главного вала, который пронизывает мембрану насквозь, и прикрепленной к нему вращающейся головки, которая в электронный микроскоп напоминает шляпку гриба. Давление протонов, скопившихся снаружи от мембраны, проталкивает их через вал и вращает головку; три протона, проходящие через вал, проворачивают головку примерно на 120 градусов, так что она совершает полный оборот за три щелчка. На головке находятся три участка связывания, и именно на них происходит сборка АТФ. С каждым поворотом головки образующееся напряжение создает или разрывает химические связи. Первый участок связывает АДФ; при следующем повороте головки к АДФ присоединяется фосфат и образуется АТФ; третий поворот высвобождает АТФ. У людей для каждого полного оборота головки нужны девять протонов, при этом образуются три молекулы АТФ.
Использование протонных насосов для хранения потенциальной энергии в форме электрохимического градиента, а затем укрощение этой энергии по мере того, как она проходит сквозь мембрану, чтобы создать химическую энергию, может выглядеть довольно странным механизмом. Однако он присущ всем формам земной жизни.
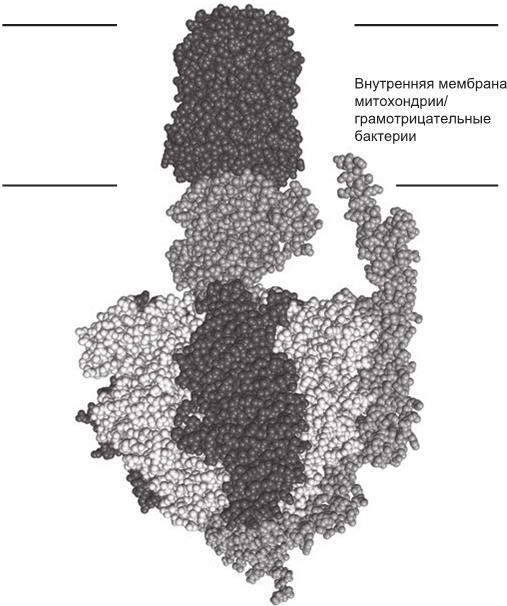
Рис. 1.8. Молекулярное изображение АТФ-синтазы, демонстрирующее ее направленность и сложность
Аналогично происходит и фотосинтез растений, хотя в этом случае солнечная энергия используется для выкачивания протонов через мембрану хлоропласта, который представляет собой результат растительной эволюции митохондрий. Бактерии, являясь прародительницами митохондрий, функционируют в этом же ключе. Они создают протонный градиент за счет разницы в концентрациях растворенного вещества по обе стороны мембраны и разницы зарядов и свободно удерживаются с помощью их клеточной стенки. Но, в отличие от людей и млекопитающих, в растительном мире конечным «приемником» электронов, движущихся по ЭТЦ, могут быть самые разные молекулы, а не только кислород. Как бы то ни было, извлекаемая с помощью ЭТЦ энергия используется для выкачивания протонов через мембрану. Этот механизм является столь универсальным, что может считаться отличительным признаком жизни на Земле.
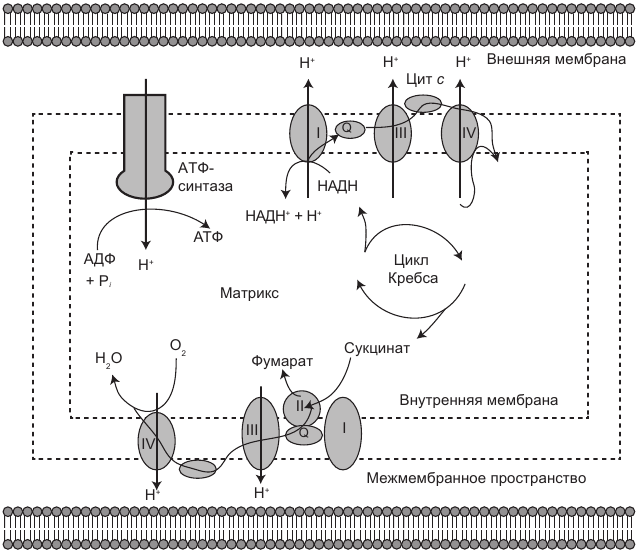
Рис. 1.9. Иллюстрация механизма генерации энергии с помощью окислительного фосфорилирования посредством комплекса I (верхняя половина рисунка) и комплекса II (нижняя половина рисунка)
Митохондриальная ДНК: любопытный реликт древности
После поглощения бактерии, впоследствии ставшей митохондрией, бактерией-хозяином она некоторое время жила на правах паразита. Организм хозяина давал ей практически все, что нужно для выживания, и поэтому она обленилась. Ей не было нужды содержать громоздкую и бесполезную ДНК. В самом деле, зачем кодировать белки, если это с успехом делает хозяйская ДНК? Природа также задалась этим вопросом и со свойственной ей безжалостной эффективностью сделала так, что паразитическая бактерия начала терять лишние гены.
И все бы ничего, только при утрате наиболее важных генов клетка неизбежно умирает. Лэйн в своей книге приводит следующий пример: наши предки-приматы однажды (миллионы лет назад) лишились гена, синтезирующего витамин С. К счастью, их диета была богата фруктами с повышенным содержанием этого витамина. Поэтому потеря данного гена не вызвала катастрофических последствий: древние человекообразные выживали и даже процветали. Но откуда мы знаем, что они в свое время обладали геном витамина С, если его нет у современных людей? Бо́льшая часть его находится в мусорной ДНК, и этот рудимент идентичен функционирующему гену рецептора витамина С у других видов.
Утрата бесполезных генов – весьма распространенное явление. Бактерии могут потерять их в течение нескольких часов или дней. Как это помогает выживанию? Деление клеток, обеспечивающее репродукцию бактерий, требует очень большого количества энергии, тогда как бактерии в сравнении с эукариотами производят очень мало энергии. Чем меньше размер бактериальной ДНК, тем меньше энергии требуется для ее копирования для дочерних клеток. Эффективность сброса генетического балласта проявляется в малом количестве мусорного ДНК на главной хромосоме бактерий.
Вы можете возразить, что утрата генов – это неэффективный механизм, потому что сброшенные гены могут быть вновь востребованы. Тем не менее отказ от генов бактериями не является столь безрассудным, как это может показаться. Дело в том, что бактерии могут вновь приобрести нужные им (равно как и другие) гены в рамках процесса, называемого горизонтальным переносом генов. Бактерии способны подбирать ДНК в окружающей их среде (забирая генетический материал у мертвых клеток или других бактерий) с помощью бактериальной конъюгации, которая не сильно отличается от акта совокупления между людьми в плане передачи ДНК. (Ну ладно, возможно, различия здесь существенны, но главное здесь то, что бактерии могут приобретать новые гены и успешно пользуются этой способностью.) Феномен горизонтального переноса генов, позволяющего бактериям получать новый генетический материал, говорит о том, что введение в пищевую цепь генетически модифицированных растений и животных может привести к непредсказуемым последствиям и требует гораздо более углубленных исследований, нежели проведены до сих пор. Бактерии в наших кишечниках или в кишечниках наших домашних животных способны вобрать в себя модифицированные гены. Если это произойдет, то в царствах животных и растений может начаться необратимый хаос (а ведь существует бесконечное число иных возможностей утечки модифицированных генов в мир живой природы).
Процесс потери и приобретения генов сохраняет общую генетическую базу бактерий в состоянии постоянного изменения, что является благоприятным для выживания, так как предупреждает потерю той или иной колонией всех «избыточных» генов в конкретный момент времени. Какая-то часть входящих в данное сообщество бактерий, как правило, сохраняет эти гены в полностью функциональном состоянии, и, если в них вновь возникает нужда, передает реабилитированный генетический материал остальным членам сообщества посредством механизма горизонтального переноса. Развитая способность бактерий делиться друг с другом генами объясняет такие явления, как очень быстрое распространение резистентности к антибиотикам в рамках больших бактериальных сообществ. Именно поэтому регулирующие организации требуют от компаний-изготовителей пищевых добавок с содержанием пробиотиков доказательств того, что соответствующие пробиотические штаммы не обладают сопротивляемостью к антибиотикам (в противном случае генетическая защита от лекарств может быть передана потенциально патогенным бактериям в кишечнике).
Процесс переноса хромосомных генов при конъюгации гораздо быстрее протекает при участии содержащихся в хромосоме крошечных колец – плазмид (я упоминал о них выше), однако бактерии могут передавать гены, являющиеся частью ее основных хромосом, просто это происходит медленнее. Любой ген, который не используется регулярно или в котором сейчас отсутствует потребность, будет отвергнут во имя более быстрой и эффективной репликации.
Будучи потомками бактерий, митохондрии потеряли бо́льшую часть своих генов. Но если бы они были всего лишь паразитами, живущими на всем готовом, то почему у них сохранились какие-то гены? Это хороший вопрос, особенно если учесть, что каждая клетка включает в себя от нескольких сотен до нескольких тысяч митохондрий, а каждая из митохондрий скрывает от пяти до десяти копий ДНК. Лэйн глубоко погружается в проблему. Содержащийся в клетке объем митохондриальной ДНК является серьезной проблемой при клеточном делении или при делении самих митохондрий (митохондриальном биогенезисе), так как все эти гены должны быть скопированы. Кроме того, каждая митохондрия должна поддерживать свой собственный аппарат генетической трансляции и синтезирующих белки рибосом. Для наследников бактерий (мы помним, что кредо первых микроорганизмов – максимальная экономия энергии) такой набор функций является, на первый взгляд, чрезмерным.
Помимо этого, наличие в одной клетке митохондрий с разными геномами потенциально влечет за собой катастрофические последствия (это происходит, если, например, митохондрии из отцовского сперматозоида умудряются выжить и сосуществуют с митохондриями из материнской яйцеклетки, что, как правило, приводит к прерыванию энергии). Этого можно было бы избежать, если бы все митохондриальные гены были переданы в ядро и удерживались там.
Другая проблема заключается в том, что открытый и беззащитный генетический материал митохондрий находится в непосредственной близости к ЭТЦ, в которой формируются и из которой исходят разрушительные свободные радикалы. Они могут повредить мДНК и вызвать мутации, потенциально способные привести к гибели митохондрии (что, в свою очередь, означает повышенную опасность возникновения разных заболеваний, включая рак, о чем мы поговорим позже).
Почему же все митохондриальные гены не переместились в ядро? Факт, что они до сих пор находятся в митохондриях (несмотря на два миллиарда лет эволюции и множество разумных причин, по которым им следовало бы туда перейти), говорит о том, что на это обязательно должна быть причина, причем она должна быть фантастически убедительной.
Суть в необходимости контроля процесса окислительного фосфорилирования. Его скорость в значительной степени обусловлена энергетическими потребностями клетки, зачастую меняющимися каждую минуту (в зависимости от того, бодрствуем мы или спим, занимаемся физическими упражнениями или сидим за столом, боремся с болезнью или пышем здоровьем и т. д.). Эти быстро изменяющиеся сценарии требуют от митохондрий адаптировать производство энергии к потребностям клетки, а каждая клетка требует к себе особого подхода (у клеток головного мозга, мышц, кишечника, печени и т. д. – разные уровни потребления энергии).
Для того чтобы эффективно реагировать на эти быстрые изменения, митохондриям приходится поддерживать определенный уровень постоянного контроля ситуации, а значит, сохранять в мДНК соответствующие гены. Реакции, которые происходят в рамках ЭТЦ во внутренней митохондриальной мембране, должны жестко регулироваться на уровне каждой митохондрии. Но это было бы невозможно, равно как и клетка не смогла бы быстро реагировать на резкие изменения во внешней среде, если бы весь процесс не контролировался бы дистанционно генами, расположенными в удалении от клеточного ядра.
Вроде бы пока наши рассуждения осмыслены, не так ли? Давайте теперь обсудим тему спроса и предложения перед тем, как я предложу вам глубже погрузиться в вопрос о том, почему митохондрии сохранили некоторые гены. Не забывайте, что целостный процесс выработки энергии от работы индивидуальных комплексов до производства АТФ АТФ-синтазой похож на последовательность переключения передач в автомобиле, при которой каждая предыдущая передача контролирует скорость движения при следующей. Если потребность клетки в энергии является сильной, то электроны быстро переносятся по ЭТЦ, протоны оперативно выкачиваются через мембрану, протонный градиент резко повышается (резервуар наполняется). Чем выше он, тем сильнее давление, приводящее к производству АТФ АТФ-синтазой.
Однако, если потребность в АТФ практически равна нулю, окислительное фосфорилирование все равно будет продолжаться до того, как в АТФ будут превращены все АДФ и все фосфаты. Так как клетка больше не использует АТФ (которая при сжигании обратно расщепляется на АДФ и фосфаты), АТФ-синтаза прекращает работу из-за дефицита сырья. Если это происходит, то протоны уже не могут пройти сквозь нее, и протонный резервуар наполняется чрезмерно высоко. Когда протонный градиент является слишком высоким, небольшое количество энергии, выделяемое при переносе электронов по ЭТЦ, оказывается недостаточным для выкачивания протонов из матрикса в межмембранное пространство. Недостаточная работа протонного насоса приводит сначала к замедлению, а потом и к остановке переноса электронов по ЭТЦ. Однако не беспокойтесь, механизм вновь начинает работать, когда потребность клетки в энергии повышается и клетка начинает использовать АТФ (в результате чего АТФ-синтаза получает больше АДФ и фосфатов). Все это указывает на важность физических упражнений, при которых клетка активно использует АТФ (мы еще поговорим об этом).
Клетка может испытывать дефицит в кислороде, например при остром нарушении мозгового кровообращения. В этом случае на завершающем этапе ЭТЦ отсутствует «приемник» электронов, и в результате они попадают, так сказать, в «пробку», после чего окислительное фосфорилирование останавливается. В каждой из такого рода ситуаций формирование «пробки» из электронов означает, что они могут ускользнуть и стать причиной появления свободных радикалов.
Рассмотрев тему «спроса и предложения», мы должны вновь обратиться к компонентам ЭТЦ. Каждый из них может быть либо восстановлен (приобрести один электрон или несколько электронов), либо окислен (потерять один или несколько электронов), но не может одновременно и восстанавливаться, и окисляться. В митохондриях эукариот процесс переноса электронов начинается с окисления НАДН и восстановления убихинона (кофермента Q) комплексом I. Далее комплекс II окисляет сукцинат до фумарата и восстанавливает убихинон Q. Комплекс III переносит электроны от восстановленного убихинона к цитохрому с. В конце ЭТЦ комплекс IV, как мы помним, катализирует перенос электронов с цитохрома с на кислород. ЭТЦ остановится, если соответствующий комплекс не передаст электрон следующему «звену». Точно так же процесс переноса электронов остановится, если, например, комплекс I не получит электрон от НАДН для его последующей передачи, и т. д.
Окислительно-восстановительные реакции (ОВР) сегодня все более активно изучаются с медицинской точки зрения. В каждой митохондрии находятся тысячи ЭТЦ (примерно десять тысяч на одну митохондрию!), а окислительное фосфорилирование может быть наиболее эффективным в том случае, когда соотношение между восстановленными и окисленными переносчиками электронов составляет примерно 50: 50.
Утрата этого баланса не только замедляет окислительное фосфорилирование и производство энергии, но также может привнести хаос в жизнедеятельность митохондрий. Эта опасность связана с тем, что переносчики электронов в ЭТЦ характеризуются реактивностью. Если поток электронов в ЭТЦ течет в нормальном режиме, то каждый опорный пункт в большинстве случаев успешно передает электроны другому такому пункту, который желает их чуть сильнее, чем предыдущий обладатель. Однако, так как переносчики электронов не могут одновременно восстанавливаться и окисляться, если следующий по цепи переносчик уже имеет лишний электрон и еще не успел от него освободиться, то в ЭТЦ возникает затор. Создание затора и выпадение электрона из общего движения подобно ситуации, когда один поезд еще не покинул станцию вовремя, и следующий за ним состав не может попасть туда. Наиболее вероятный вариант в таком случае – транспортная пробка. В результате возникает вероятность преждевременного перехода блокированного электрона на кислород. Когда кислород получает электрон от любого носителя, кроме комплекса IV (последний комплекс в ЭТЦ), то формируется известный нам токсичный свободный радикал – супероксид. Это необязательно ведет к отрицательным последствиям (как я покажу ниже), но сейчас давайте условимся, что супероксид, как правило, приносит вред всем видам биологических молекул. Продолжая аналогию с пробкой из поездов, представим, что приближающийся локомотив не получил сигнал о том, что другой состав застрял на станции, а машинист не успел ударить по тормозам. В этом случае поезда сталкиваются и их вагоны сходят с рельсов, причиняя окружающей среде всевозможный ущерб.
Поддержание динамического равновесия восстановительно-окислительных реакций не только обеспечивает быстрое и эффективное движение электронов по ЭТЦ, но и снижает риск формирования свободных радикалов в форме супероксидов. Сохранение этого баланса также зависит от количественного соотношения между собой разных категорий транспортеров электронов (включая промежуточные переносчики). Например, если в митохондрии присутствует переизбыток комплексов I, принимающих электроны от НАДН, но нет соответствующего им количества коферментов Q, многие из несчастных обладателей электронов, не имея возможности их передать, просто потеряют своих подопечных, после чего бедняг захватит хищный кислород. Конечно, как и во всех других случаях, связанных с живыми организмами, соотношение переносчиков ЭТЦ постоянно изменяется (какое-то их количество изнашивается, заменяется и т. д.).

