Глава 1
В поисках исцеления
Недавно я услышала необыкновенную историю, которая хорошо показывает мощь и возможности технологии редактирования генома.
В 2013 году ученые из Национальных институтов здравоохранения США столкнулись с медицинской загадкой. Изучая редкое наследственное заболевание, известное как синдром WHIM, они встретили пациентку, чье состояние казалось необъяснимым. В раннем возрасте у женщины (я буду называть ее Ким) была диагностирована эта болезнь, однако через много лет, когда специалисты НИЗ обследовали Ким, заболевание будто бы чудесным образом исчезло.
Синдром WHIM выявлен лишь у нескольких десятков человек в мире, и этот потенциально смертельный иммунодефицит приносит большие страдания тем, кому не повезло услышать такой диагноз. Причиной болезни является крошечная мутация – всего одна неправильная “буква” из 6 миллиардов “букв” ДНК: иными словами, заменены лишь около дюжины атомов. Но это крохотное изменение делает носителя синдрома WHIM чрезвычайно восприимчивым к заражению вирусом папилломы человека (ВПЧ), который вызывает образование неконтролируемо распространяющихся по всему телу бородавок. А они, в свою очередь, могут перерастать в рак.
О редкости заболевания наглядно говорит тот факт, что первой пациенткой, у которой сотрудники НИЗ диагностировали этот синдром еще в 1960-х годах, была Ким, ее же они и обследовали годы спустя (в научной литературе она известна как пациент WHIM-09). Ким страдала от болезни с рождения, и в течение жизни ее несколько раз госпитализировали из-за инфекций, связанных с синдромом.
В 2013 году Ким, которой к тому времени было уже 58 лет, пришла на обследование в НИЗ с двумя своими дочерьми, каждой из которых было по 20 с небольшим. У более молодой из двух женщин были классические симптомы заболевания, однако ученые очень удивились, когда обнаружили, что сама Ким казалась совершенно здоровой. Собственно, она это и подтвердила, заявив, что у нее нет никаких симптомов уже больше 20 лет. Поразительным образом Ким излечилась сама, без всякого медицинского вмешательства.
Ученые провели ряд экспериментов, чтобы понять, как произошло это спонтанное исцеление от потенциально смертельной болезни, и обнаружили некоторые важные зацепки. В клетках, взятых из щеки и с кожи Ким, все еще присутствовал мутантный ген, однако он необъяснимым образом исчез из клеток ее крови. Подвергнув ДНК кровяных клеток женщины более обстоятельному анализу, ученые обнаружили нечто еще более удивительное: у одной копии 2-й хромосомы отсутствовали целых 35 миллионов “букв” ДНК – и этот фрагмент целиком включал мутировавший ген под названием CXCR4. (Названия генов пишутся курсивом, а названия белков, которые кодируют эти гены, – прямым шрифтом. К примеру, ген HTT кодирует белок гентингтин; болезнь Гентингтона вызвана мутацией в гене HTT.) Остальные двести миллионов “букв” ДНК 2-й хромосомы были перемешаны – словно сквозь хромосому пронеслось торнадо и оставило ее составляющие в полном беспорядке.
Эти первоначальные открытия породили ряд новых вопросов. Как ДНК в клетках крови Ким стала такой “неорганизованной”, в то время как в других клетках организма она была в норме (не считая мутации в гене CXCR4)? Более того, почему, несмотря на то что хромосома, содержащая ген CXCR4, так сильно повреждена – на ней не хватает 164 генов! – клетки крови не просто выжили, но и нормально функционируют? Геном человека – полный набор всей генетической информации в наших клетках – содержит тысячи генов, необходимых для поддержания жизненно важных функций, таких как репликация ДНК и деление клеток, и казалось практически невероятным, что такое количество генов могут просто исчезнуть без вредных последствий для организма.
Проведя ряд опытов, ученые НИЗ понемногу приблизились к объяснению чудесного исцеления Ким. Они заключили, что в одной из клеток ее организма, должно быть, произошло редкое событие, обычно приводящее к катастрофическим последствиям, – хромотрипсис. Это явление было открыто недавно; в результате хромотрипсиса хромосома внезапно разрушается, а затем восстанавливается, и это приводит к массовой перестановке генов в ней. Последствия такой трансформации для организма обычно либо незначительны (если поврежденная клетка немедленно умирает), либо очень серьезные (если перестановка в ДНК случайно активирует гены, вызывающие рак).
Однако в теле Ким хромотрипсис вызвал другие изменения. Мутировавшая клетка не просто нормально развивалась, но избавилась от гена, вызывающего синдром WHIM, так как в ней больше не было копии гена CXCR4, несущего болезнь.
Однако Ким повезло не только в этом. Ученые НИЗ определили, что “счастливая” клетка была, должно быть, гемопоэтической (кроветворной) стволовой клеткой. Из такой стволовой клетки происходят все виды кровяных клеток в теле, у нее есть практически неограниченный потенциал размножения и самообновления. Эта клетка передала свою измененную хромосому каждой дочерней клетке, что в итоге привело к обновлению всей иммунной системы Ким. Теперь в ней были только новые здоровые лейкоциты (белые кровяные тельца), в которых отсутствовала мутация гена CXCR4. Эта цепочка событий – настолько маловероятная, что я с трудом могла допустить мысль о реальности произошедшего, пока слушала доклад ученых, – фактически вывела из тела Ким неизлечимую болезнь, от которой она страдала с рождения.
Ученые, исследовавшие здоровье Ким, пришли к выводу, что природа будто бы провела над удачливой женщиной “беспрецедентный эксперимент”, в ходе которого всего одна стволовая клетка прошла через ряд спонтанных изменений, которые избавили как ее саму, так и все дочерние клетки от гена, несущего болезнь. Это была случайность – и, если бы события развивались немного иначе, эта случайность, попросту говоря, могла бы убить Ким, а не спасти ей жизнь.
Чтобы понять, насколько неожиданно благоприятным был такой исход, представьте, что геном человека – это большая компьютерная программа. В случае Ким в программе среди шести миллиардов “букв” содержалась всего одна “буква” некорректного кода. Чтобы найти эту неверную “букву”, вы вряд ли бы стали случайным образом, наугад удалять большие куски кода и перемешивать другие его части: это не только не исправило бы изначальную ошибку, но и привело бы к другим, гораздо более опасным. Только в случае чрезвычайного везения – вероятность такого везения была бы один к миллиону или даже к миллиарду – вы бы умудрились не только удалить именно тот кусок кода, что содержал ошибку, но и не нарушить при этом ключевые функции программы. Коротко говоря, это и случилось в геноме Ким – только работавшим наугад программистом была сама природа.
Однако как бы удивителен ни был случай Ким, еще больше поражает то, что он не уникален. Хотя это и единственный описанный случай исцеления пациента в результате спонтанного разрушения и последующего восстановления хромосомы, в научной литературе есть и другие примеры пациентов, которые частично или полностью излечились после случайных, спонтанных исправлений мутаций. Например, в 1990-х у двух пациентов из Нью-Йорка выявили тяжелый комбинированный иммунодефицит (ТКИД) – наследственное заболевание, которое также называют синдромом “мальчика в пузыре” (из-за стерильных условий, в которых приходилось держать некоторых детей, чтобы минимизировать возможный контакт с болезнетворными микроорганизмами). Без строжайшей изоляции или интенсивных форм терапии маленькие пациенты с диагнозом ТКИД обычно умирают, не дожив и до двух лет. Однако двое пациентов из Нью-Йорка оказались исключением из этого ужасного правила: они на удивление хорошо себя чувствовали и в подростковом, и во взрослом возрасте. В обоих случаях, как определили ученые, клетки пациентов спонтанно скорректировали мутацию в гене ADA, несущую болезнь, причем эта коррекция не потревожила остальные гены хромосомы.
Известны и другие похожие случаи, когда сама природа редактировала геном, избавляя людей от наследственных заболеваний, таких как синдром Вискотта – Олдрича (от этого недуга целых 10–20 % процентов больных спасает именно спонтанная коррекция генома) или болезнь печени под названием тирозинемия. В случае некоторых кожных заболеваний присутствие клеток с отредактированным геномом можно увидеть невооруженным взглядом: при одном из видов ихтиоза, имеющем выразительное название “ихтиоз с конфетти”, у больных на коже появляются участки красной, шелушащейся кожи. Клетки в этих местах несут генетическую мутацию, однако клетки окружающих, здоровых участков кожи смогли ее исправить.
Однако в общем и целом шансы на спонтанное излечение от наследственного заболевания минимальны. С большинством пациентов никогда не произойдет такого чуда природы – чтобы гены сами изменились абсолютно правильным образом, именно в нужных клетках и в нужных тканях. Редактирование генома самой природой – это аномалия, интересный медицинский курьез, затронувший небольшое количество пациентов, выигравших в “генетическую лотерею”.
Но что, если бы редактирование генома было не только спонтанным явлением? Что, если бы врачам был доступен какой-нибудь способ корректировать вредоносные мутации, которые вызывают синдромы WHIM, ТКИД, тирозинемию – и, если уж на то пошло, любое наследственное заболевание?
У многих ученых, включая и меня, случаи, подобные истории болезни Ким, вызвали повышенный интерес – не только потому, что они обнаруживали целительную мощь природы, редактирующей геном, но также потому, что они наталкивали на мысль о возможности нового вида медицинского вмешательства: рационального и точно рассчитанного исправления ошибок в геноме. Исправления, которое могло бы устранить неприятные симптомы наследственных заболеваний. Истории этих везучих людей продемонстрировали, что намеренное редактирование генома стало бы возможно, если бы у ученых были нужные генетические данные и необходимые биотехнологические инструменты.
В течение десятилетий, задолго до того, как я посвятила себя этой области знаний, специалисты по медико-биологическим наукам бились над тем, чтобы получить эти данные и разработать такие инструменты. Более того, ученые мечтали о терапевтическом редактировании генома еще до того, как было обнаружено, что сама природа подсказывает, как это можно сделать. Но чтобы сделать такую технологию реальной, исследователям необходимо было понять сам геном: из чего он сделан, как он строится и – что наиболее важно – каким образом можно вносить в него изменения и “настраивать” его. Только обладая подобной базовой информацией, первопроходцы этой научной области и их последователи могли предпринять первые неуверенные шаги по направлению к лечению людей – людей не настолько везучих, как Ким, которой посчастливилось исцелиться самой.
Термин “геном”, предложенный в 1920 году немецким ботаником Гансом Винклером и, возможно, образованный слиянием слов “ген” и “хромосома”, описывает всю совокупность наследственного материала в клетке организма. В большинстве случаев он идентичен в каждой клетке любого организма (за исключением отдельных клеток с мутациями). В геноме содержится информация – инструкции, согласно которым организм любого живого существа растет, поддерживает себя и передает гены потомкам. У одного организма геном вызывает развитие плавников и жабр для движения и дыхания под водой; у другого – рост листьев и выработку хлорофилла для получения энергии из солнечного света. Присущие нам физические черты: зрение, рост, цвет кожи, предрасположенность к недугам и т. д. – соответствуют информации, закодированной в наших геномах.
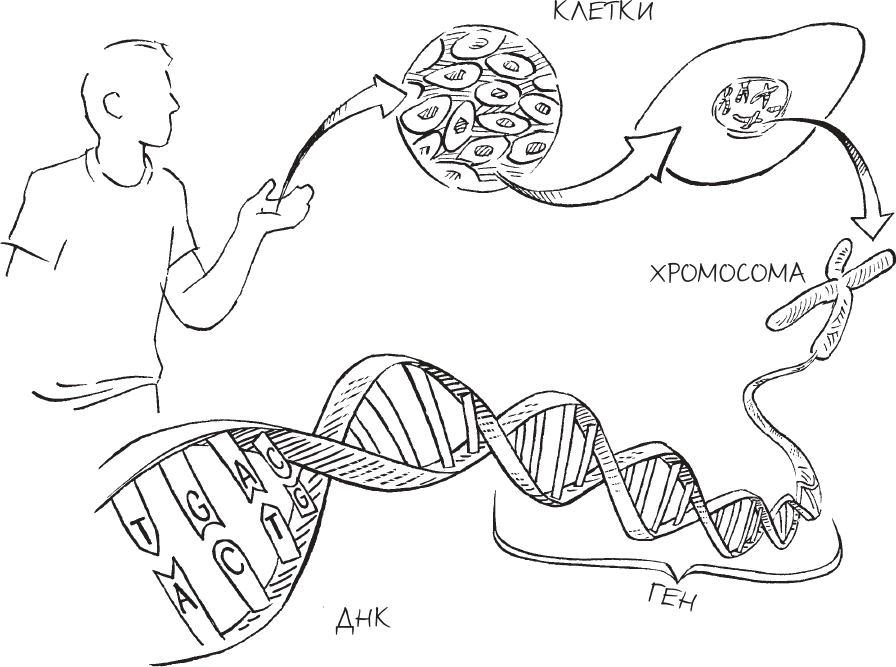
Геном образуют молекулы, которые называются дезоксирибонуклеиновой кислотой (ДНК) и состоят всего лишь из четырех различных видов структурных элементов – нуклеотидов, тех самых “букв” ДНК: А, Г, Ц и Т. Эти буквы – сокращения названий химических групп, азотистых оснований, которыми нуклеотиды отличаются друг от друга: аденин, гуанин, цитозин и тимин. “Буквы” молекул связаны в длинные одинарные цепочки. Две такие цепочки образуют знакомую нам всем спиральную структуру.
Эта структура чем-то напоминает лесенку, скрученную в длинную двойную спираль. Две цепочки ДНК оборачиваются друг вокруг друга вдоль центральной оси, а сахарофосфатный остов каждой цепи остается на внешней стороне спирали; если продолжить сравнение, можно сказать, что эти элементы как бы образуют перила лестницы. При таком расположении элементов азотистые основания четырех типов оказываются в центре спирали и находятся ближе всего к оси, встречаясь в середине молекулы; это “ступеньки” лестницы. Элегантная черта этой структуры – набор химических взаимодействий, благодаря которым цепочки связаны в каждой ступеньке. Это своего рода “молекулярный клей”: “буква” А с одной цепочки всегда образует пару с “буквой” Т на другой цепочке, а Г – с Ц. Эти пары “букв” называют парами оснований.
Двойная спираль прекрасно демонстрирует молекулярные основы наследственности; именно с помощью этой структуры относительно простое химическое соединение ДНК может при делении клетки передавать генетическую информацию двум дочерним клеткам; таким же образом информация может в дальнейшем распространяться в каждую клетку целого растения или животного. Благодаря тому, что молекула состоит из двух цепочек, и тому, что существуют правила, согласно которым эти цепочки соединяются (А – только с Т, Г – только с Ц), каждая из них представляет собой точный шаблон для соответствующей пары.
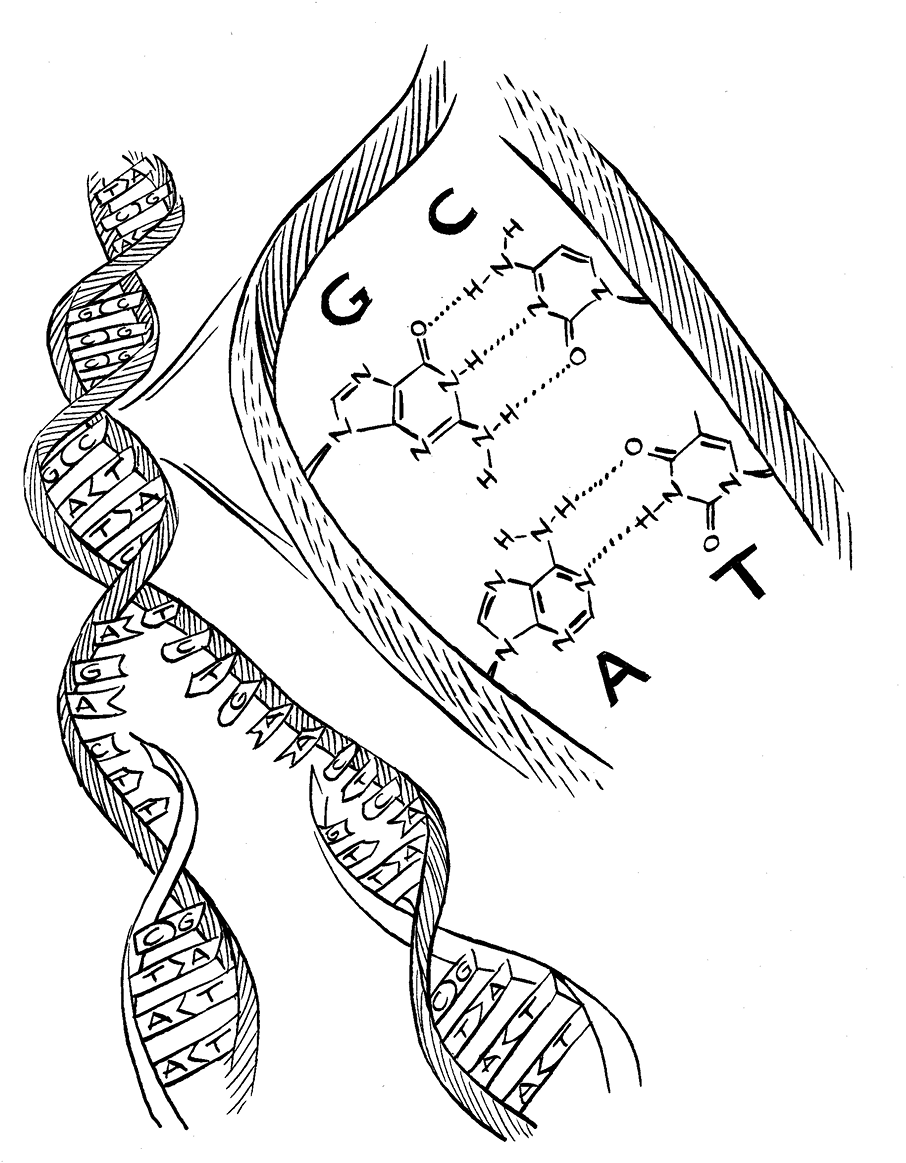
Структура двойной спирали ДНК
Незадолго до деления клетки две цепочки разделяются ферментом, который “расстегивает” двойную спираль прямо по центру, будто застежку-“молнию”. После этого другие ферменты подбирают новую пару для каждой цепочки, используя те же самые правила для формирования пар оснований, в результате чего образуются две точные копии оригинальной двойной спирали.
Мое собственное знакомство с двойной спиралью ДНК совпало с другим моим открытием: оказывается, ученые способны изучать молекулы, слишком маленькие для того, чтобы их можно было разглядеть даже в самый мощный оптический микроскоп. Мне было около двенадцати, когда я, вернувшись однажды домой из школы, обнаружила на своей постели потрепанную книгу Джеймса Уотсона “Двойная спираль” (мой отец иногда выбирал для меня ту или другую подержанную книгу в букинистическом магазине, чтобы посмотреть, не заинтересует ли она меня). Я подумала, что это какой-то детектив (и так ведь оно и было!), и отложила книгу на несколько недель, прежде чем погрузиться в чтение одним дождливым субботним днем.
Уотсон рассказывал о том, как научное сотрудничество с Фрэнсисом Криком позволило им обоим – используя критически важную информацию, собранную их коллегой Розалинд Франклин, – расшифровать эту простую и красивую молекулярную структуру. Именно тогда я ощутила первую искру интереса, который в конце концов и заставил меня выбрать похожий путь в жизни. (Много лет спустя я смогла резко ускорить собственную научную карьеру, расшифровав некоторые из первых трехмерных структур РНК – куда более сложных!)
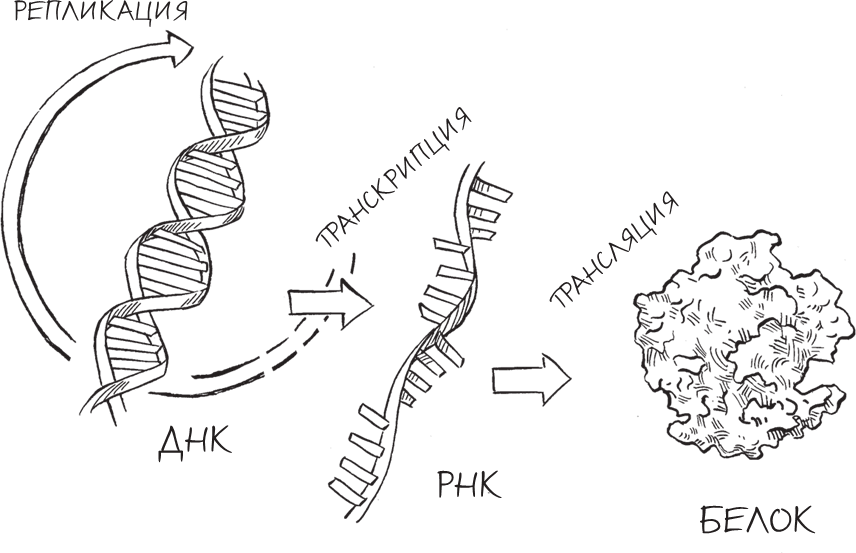
В годы, которые последовали за открытием Уотсона и Крика, другие ученые пытались понять, каким образом структура этой молекулы и ее достаточно простые химические составляющие могут кодировать информацию и объяснять многочисленные биологические явления. ДНК похожа на какой-то тайный, зашифрованный язык: каждая последовательность “букв” предоставляет собой инструкцию для образования определенного белка внутри клетки. Затем эти белки выполняют большинство жизненно важных функций в организме, например расщепляют пищу, распознают и уничтожают болезнетворные микроорганизмы, чувствуют свет.
Чтобы превратить инструкции, содержащиеся в ДНК, в белки, клетки используют важнейшую (и близкородственную ДНК) молекулу рибонуклеиновой кислоты (РНК), которая образуется по шаблону ДНК в ходе процесса, который называется транскрипцией. Три “буквы” в РНК совпадают с “буквами” ДНК, однако “буква” Т (тимин) заменена на У (урацил). Кроме того, сахар, образующий остов РНК, содержит на один атом кислорода больше, чем атом сахара в ДНК (потому-то последнюю и называют дезоксирибонуклеиновой кислотой). РНК выступает в качестве передатчика информации от клеточного ядра, в котором находится ДНК, во внешнюю часть клетки, где образуются белки. В этом процессе (он называется трансляцией) клетки используют для создания отдельных молекул белков длинные цепочки РНК, которые образуются с использованием информации с определенных фрагментов ДНК – участков кода, называемых генами. Каждые три “буквы” РНК, поставленные рядом, соответствуют одной аминокислоте (аминокислоты – это “строительные блоки” белков). Гены и соответствующие им белковые продукты отличаются друг от друга последовательностью нуклеотидов (в генах) и аминокислот (в белках). Этот общий поток генетической информации – от ДНК к РНК к белку – известен как центральная догма молекулярной биологии, и именно на этом языке “общается” и выражает себя жизнь.
Размер генома и число генов, содержащихся в нем, сильно различаются у представителей различных царств живого мира. У большинства вирусов, например, всего несколько тысяч “букв” ДНК (или РНК, так как в некоторых вирусных геномах нет ДНК) и небольшое количество генов. Геномы бактерий, с другой стороны, содержат миллионы “букв” и около 4000 генов. В геноме мух около 14 000 генов, распределенных среди сотен миллионов пар оснований ДНК. В человеческом геноме около 3,2 миллиарда “букв” ДНК и около 21 000 генов, кодирующих белки. Любопытно, что размер генома не всегда соответствует сложности организма; геном человека приблизительно такой же длины, как геном мыши или лягушки, где-то в десять раз короче, чем геном саламандры, и более чем в сто раз меньше, чем геномы некоторых растений.
Центральная догма молекулярной биологии
Геномы различных видов живых существ могут иметь совершенно различную структуру. В то время как большинство бактериальных геномов существуют внутри клетки в виде одной непрерывной последовательности ДНК, человеческий геном состоит из 23 отдельных частей, которые называются хромосомами и имеют длину от 50 до 250 миллионов “букв”. Как и клетки большинства млекопитающих, клетки человека обычно содержат две копии каждой хромосомы, одну от отца, другую от матери. Каждый родитель передает ребенку 23 хромосомы, так что всего их получается 46. (Существуют исключения из этого правила; например, у людей с синдромом Дауна есть третья копия 21-й хромосомы.) Полный набор ядерных хромосом может быть найден практически в любой клетке тела (важное исключение – красные кровяные тельца, так как у них нет ядра), однако ДНК хранится не только в ядре. В геном человека также входит отдельная мини-хромосома – она содержит всего 16 000 “букв” ДНК и расположена в митохондриях, “батарейках” клетки, производящих энергию. В отличие от генетического кода других хромосом, митохондриальная ДНК наследуется исключительно по материнской линии.
Мутации в любой из 23 пар хромосом или в митохондриальной хромосоме могут вызывать наследственные заболевания. Простейшая мутация называется точечной заменой – в этом случае один нуклеотид заменен на другой, и в результате соответствующий ген будет кодировать дефектный белок. К примеру, серповидноклеточная анемия, наследственное заболевание крови, случается при замене семнадцатой “буквы” гена под названием бета-глобин (с А на Т). При переходе от нуклеотидов к аминокислотам, то есть в ходе трансляции, эта мутация приводит к тому, что глутамат заменяется на валин, причем происходит это в критической области белка гемоглобина – компонента эритроцитов (красных кровяных телец), транспортирующего кислород. Последствия этого крошечного изменения в белке – меняются лишь десять атомов из более чем восьми тысяч – очень серьезны. Мутировавшие молекулы гемоглобина слипаются и образуют аномальные волокна, меняющие форму эритроцитов, что ведет к анемии, повышенному риску инсульта и инфекций, а также к сильной боли в костях.
Серповидноклеточная анемия – пример генетического заболевания, наследуемого по рецессивному типу. Это означает, что болезнь возникает тогда, когда обе копии гена HBB в организме несут мутацию; если изменения есть только в одной копии, то немутировавший ген может произвести достаточно нормального гемоглобина, чтобы нивелировать негативное воздействие мутантного гемоглобина. Люди, у которых лишь одна копия гена HBB мутантная, все равно являются носителями серповидноклеточной анемии, и хотя обычно это не влияет на их здоровье, они все же могут передать дефектный ген потомству.
Другие генетические заболевания наследуются по доминантному типу, что означает, что всего одной мутантной копии гена достаточно, чтобы вызвать болезнь. Один из примеров этого – синдром WHIM, при котором тысячная “буква” гена CXCR4 меняется с Ц на Т; мутировавший ген кодирует гиперактивный белок, который нивелирует работу здорового гена.
И серповидноклеточная анемия, и синдром WHIM – примеры генетических заболеваний, вызываемых простыми точечными заменами (ошибочной подменой одной “буквы” ДНК на другую). Однако генетические заболевания могут быть и результатом вставки (инсерции) или утраты (делеции) фрагментов ДНК. К примеру, нейродегенеративное расстройство, известное как хорея Гентингтона, происходит из-за мутации в гене HTT, в котором одни и те же три “буквы” ДНК повторяются слишком много раз. Это заставляет клетки мозга производить аномальные белки, постепенно разрушающие эти клетки. А вот муковисцидоз (опасное для жизни наследственное заболевание, которое поражает главным образом легкие), напротив, возникает из-за удаления трех “букв” генетического кода в гене CFTR, что приводит к тому, что белок лишается важной аминокислоты и его функционирование нарушается. Другие заболевания возникают, когда участки гена инвертированы (расположены в обратном порядке) или когда фрагменты хромосом или даже целые хромосомы по ошибке удвоены или отсутствуют.
О генетических причинах многих болезней стало известно благодаря относительно недавнему изобретению секвенирования ДНК – процесса, который позволяет ученым прочитывать и записывать содержимое генома человека “буква за буквой”. После того как в 1970-х годах появились первые методы секвенирования, ученые начали кропотливо искать и идентифицировать генетические причины наиболее известных на тот момент наследственных заболеваний. “Квантовый скачок” в этой области произошел, когда был осуществлен проект “Геном человека”, начавшийся в 1990-х годах, когда ученые со всего мира объединились, чтобы отсеквенировать весь геном человека. При выполнении этой амбициозной задачи была использована новая технология, которая позволяла клонировать большие фрагменты ДНК человека в дрожжах. Реализации проекта также способствовали значительный прогресс в автоматизации лабораторных процессов и разработка сложных вычислительных алгоритмов для облегчения анализа данных, полученных при секвенировании. Проект стоил огромных усилий и средств (около 3 миллиардов долларов), и в 2001 году был опубликован первый “черновой вариант” генома.
С момента завершения проекта “Геном человека” процесс секвенирования ДНК и секвенирования целых геномов стал удивительно быстрым, дешевым и эффективным. Ученые точно идентифицировали более четырех тысяч различных мутаций, способных вызывать генетические заболевания. Секвенирование ДНК помогает выявить повышенный риск развития некоторых видов рака, подбирать индивидуальные методики лечения для пациентов с различной наследственностью. Сегодня коммерческий анализ ДНК стал общедоступным: он стоит лишь несколько сотен долларов за каждый тест, и миллионы людей решили сделать анализ собственных геномов, для чего им нужно было лишь предоставить образец слюны. Последовало значительное увеличение объема данных о человеческом геноме, что помогло исследователям выявить важные связи между тысячами вариантов генов и рядом физических и поведенческих черт.
И все же, несмотря на то что секвенирование генома отражает огромный прогресс в изучении наследственных недугов, это в конечном счете лишь диагностический инструмент, но не средство для их лечения. Оно помогло нам увидеть, как наследственные заболевания записываются на языке ДНК, однако секвенирование не дает нам никаких возможностей для изменения этого языка. В конце концов, научиться читать – далеко не то же самое, что научиться писать. Для этого ученым нужен совершенно другой набор инструментов.
Исследователи мечтали о связанных с ДНК методах лечения с тех пор, как было открыто существование генетических заболеваний. Когда некоторые ученые только начинали определять основополагающие причины наследственных заболеваний, другие уже находились в напряженном поиске новых методов лечения этих недугов – методов, которые позволили бы не только давать пациентам препараты, временно смягчающие нежелательные эффекты генной мутации, но и исправлять сам мутировавший ген, чтобы навсегда остановить болезнь. Приведу пример: серповидноклеточная анемия лечится сегодня при помощи частых переливаний крови, использования препарата гидроксикарбамида и пересадки костного мозга. Разве не лучше было бы атаковать саму мутацию ДНК, вызвавшую заболевание?
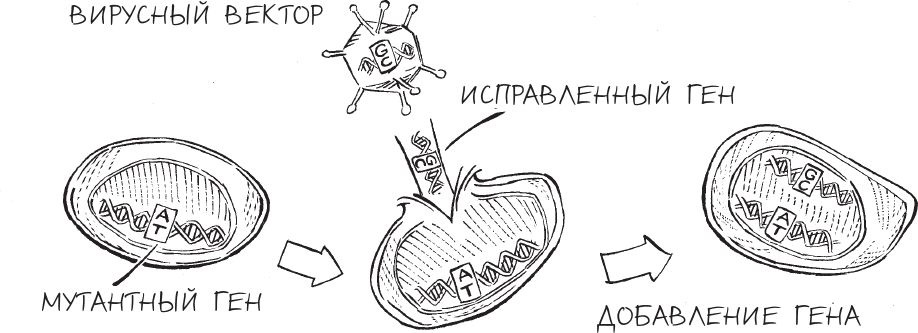
Пионеры исследований в этой области знали, что лучшим решением для лечения наследственных заболеваний было бы исправление дефектного гена – то есть целенаправленно проделать то же самое, что природа сделала случайно, исцелив Ким и других везучих пациентов вроде нее. Однако идея лечения наследственных недугов посредством переписывания мутантного генетического кода казалась фантастической – нечто поиска иголки в стоге сена, а потом вытаскивания ее из этого стога, причем нельзя было задеть при этом ни одной соломинки. Но вместе с тем ученые подозревали, что похожих изменений можно было бы добиться, добавляя целые замещающие гены в поврежденные клетки. Вопрос состоял в том, каким образом доставить этот ценный груз в нездоровый геном.
Зная о том, что вирусы обладают необычной способностью “вклеивать” новую генетическую информацию в ДНК бактериальных клеток, пионеры исследований генной терапии поняли, что вирусы можно использовать для доставки “лечебных генов” людям. Первые опыты подобного рода были проведены в конце 1960-х годов американским врачом Стэнфилдом Роджерсом – он изучал папилломавирус Шоупа, вызывающий вырастания на коже у кроликов. Роджерса особенно заинтересовала одна особенность этого вируса: в телах зараженных кроликов вырабатывалось слишком много аргиназы – фермента, нейтрализующего вредную аминокислоту аргинин. В организмах больных кроликов было гораздо больше аргиназы и меньше аргинина, чем у здоровых животных. Кроме того, Роджерс обнаружил, что у исследователей, работавших с вирусом, уровень аргинина в крови также был ниже нормы. Видимо, эти ученые подхватили вирус от кроликов, и эта инфекция вызвала долгосрочные изменения также и в их телах.
Роджерс начал подозревать, что вирус Шоупа доставлял в клетки ген, ответственный за повышенную выработку аргиназы. Он удивился, что вирус способен переносить генетическую информацию столь эффективно, и задался вопросом: а смогла бы специально сконструированная версия вируса доставлять в клетки другие, полезные гены? Много лет спустя Роджерс вспоминал: “Было ясно, что в поисках болезни мы открыли средство лечения!”
Ему не пришлось долго ждать случая, чтобы протестировать свою теорию на реальных пациентах. Спустя всего несколько лет у двух девочек из Германии было диагностировано наследственное расстройство под названием гипераргининемия. Как и у кроликов, инфицированных папилломавирусом Шоупа, у пациенток были аномальные уровни аргинина в крови – однако на этот раз не пониженные, а слишком высокие. Ген, ответственный за производство аргиназы (как подозревал Роджерс, именно этот ген переносился вирусом Шоупа), в организмах девочек либо отсутствовал, либо мутировал.
Симптомы гипераргининемии ужасны: в их числе постепенно усиливающиеся спазмы, эпилепсия и серьезная умственная отсталость. Однако был шанс, что вмешательство на ранней стадии, особенно в случае младшей пациентки, могло предотвратить наиболее тяжелые последствия заболевания. Роджерс и его немецкие коллеги ввели девочкам вирус Шоупа в терапевтических целях, сделав инъекцию больших доз очищенного вируса кроликов прямо в кровоток.
К сожалению, экспериментальная генная терапия Роджерса обернулась разочарованием – и не только для него, но и, что более печально, для его пациентов и их семьи. Инъекции не оказали почти никакого воздействия ни на одну из девочек, а Роджерса массово порицали за процедуру, которую многие его коллеги сочли безрассудной и непродуманной. Дальнейшее исследование показало, что вопреки предположениям Роджерса в вирусе Шоупа даже не содержалось гена аргиназы, поэтому он не мог никак быть полезен для лечения гипераргининемии.
Хотя Роджерс больше никогда не предпринимал попыток провести генную терапию, его идея об использовании вирусов в качестве средства доставки генов в клетки – ученые называют такие средства векторами – произвела революцию в биологии. Эксперимент не удался, однако общий принцип Роджерса оказался верным, и перенос генов при помощи вирусов до сих пор является одним из наиболее эффективных известных способов вставки генов в геном клетки – и, следовательно, изменения генетического кода живых организмов.
Вирусы эффективны в качестве векторов благодаря нескольким своим характерным особенностям. Начать с того, что в результате своей эволюции вирусы научились невероятно эффективно проникать в клетки любого типа. С тех пор как на Земле существует жизнь, организмам всех царств – бактериям, растениям, животным и т. д. – приходилось бороться с паразитическими вирусами, единственной целью которых является “взлом” клетки и вставка в нее собственной ДНК, чтобы эта клетка вырабатывала множество новых копий вирусных частиц. На протяжении тысячелетий эволюции вирусы выработали способность использовать практически любое слабое место в клеточной защитной системе и усовершенствовали стратегии “доставки” своего генетического груза внутрь клетки. Вирусные векторы поразительно надежны в качестве инструмента; работающие с ними исследователи могут доставить гены в необходимые клетки с практически стопроцентной эффективностью. Для ученых, которые первыми использовали этот вид терапии, вирусные векторы были чем-то вроде троянского коня.
Вирусы способны не только переносить свою ДНК внутрь клетки, но и обеспечивать ее сохранение там. В 1920–1930-е годы, на заре генетических экспериментов на бактериях, ученые недоумевали по поводу способности бактериальных вирусов возникать словно из ниоткуда и вызывать инфекции. Дальнейшие исследования показали, что эти вирусы могут вносить свой геном в бактериальную хромосому и таиться там до тех пор, пока условия не станут подходящими для интенсивного инфицирования. Ретровирусы – большой класс вирусов, к которым относится, например, вирус иммунодефицита человека (ВИЧ), – проделывают то же самое в организме человека, внося свой генетический материал в геном инфицированных клеток. Из-за этого вредоносного свойства уничтожить ретровирусы чрезвычайно сложно, и они сумели оставить огромный след в наследственности нашего вида. Целых 8 % генома человека – около 250 миллионов “букв” ДНК – это наследие древних ретровирусов, которые поражали наших предков много тысячелетий назад.
Генная терапия с использованием вирусных векторов
За первыми попытками генной терапии в 1960-х последовало быстрое развитие этой научной области, которое происходило благодаря революционной разработке, известной как рекомбинантная ДНК, – это собирательный термин для генетического кода, искусственно созданного в лаборатории. Используя новые биотехнологические инструменты и новые биохимические методы, ученые в 1970-х и 1980-х годах научились вырезать и вставлять фрагменты ДНК в геномы и выделять заданные последовательности генов. Это позволило им вставлять “лечебные” гены в вирусы и удалять опасные гены таким образом, что вирусы больше не вредили инфицированным клеткам. Ученые фактически превратили эти вирусы в нечто вроде тихих снарядов, предназначенных для того, чтобы доставить свой генетический заряд точно в нужную цель – и никуда более.
К концу 1980-х были проведены эксперименты на мышах, и в ходе этих экспериментов перенастроенные ретровирусы успешно вставляли произведенные в лаборатории гены в ДНК животных; теперь предстояло испытать генную терапию в клинических условиях. В это время я работала в Гарварде, проводила там исследования для своей докторской диссертации по биохимии; я помню, как мы с коллегами по лаборатории обсуждали новость о том, что Френч Андерсон и его коллеги из Национальных институтов здравоохранения первыми смогли провести клинические испытания. Они разработали многообещающий вектор, снабженный здоровой копией гена ADA (аденозиндезаминазы). Из-за мутации этого гена возникает недостаточность аденозиндезаминазы – формы ТКИД (тяжелого комбинированного иммунодефицита). Команда Андерсона хотела использовать генную терапию для того, чтобы навсегда включить здоровый ген ADA в состав кровяных телец пациентов, страдающих от ТКИД, – таким образом, чтобы эти клетки смогли вырабатывать недостающий белок. Андерсон и его коллеги надеялись, что это приведет к излечению от болезни.
К сожалению, результаты этого первого клинического испытания оказались не вполне ясными; перестроенный вирус вроде бы не причинил вреда ни одному из двух пациентов, которые его получили, однако и эффективность метода было трудно определить. К примеру, после проведения этой процедуры у обоих пациентов увеличилось количество жизнеспособных иммунных клеток – однако это улучшение могло быть вызвано и другими средствами, которые больные принимали параллельно с проведением генной терапии. Более того, в реальности лишь очень небольшое число клеток получило здоровый ген ADA, а это означало, что вирус, вероятно, не настолько эффективен в качестве средства доставки генов, как надеялись ученые.
Однако за три десятилетия, прошедших со времени этого первого и не слишком убедительного опыта, в области генной терапии происходил феноменальный прогресс. Усовершенствования в конструировании вирусных векторов и методов их доставки в клетки привело к чрезвычайно воодушевляющим результатам генной терапии ADA у десятков больных ТКИД, и коммерческий препарат под названием стримвелис, скорее всего, скоро будет одобрен экспертами.
По состоянию на 2016 год было проведено около 2000 испытаний различных видов генной терапии, и список недугов, поддающихся лечению этим методом, значительно расширился: теперь он включает такие моногенные наследственные заболевания, как муковисцидоз, миодистрофия Дюшенна, гемофилия, некоторые виды слепоты, а также все большее число различных сердечно-сосудистых и неврологических недугов. А перспективный метод иммунотерапии рака – при котором клетки, сражающиеся с опухолью, “заряжаются” генами, нацеленными на специфичные для опухолей молекулы, – был назван одним из самых многообещающих прорывов в онкологии и подтверждением того, что генная терапия еще много чего может предложить медицине.
Но, несмотря на шумиху, генная терапия пока не стала панацеей, как надеялись ученые и медики; напротив, в некоторых случаях она, кажется, принесла больше вреда, чем пользы. Тяжелый удар по этой области нанес 1999 год, когда один пациент умер после мощного иммунного ответа его организма на большую дозу вирусного вектора. В то время я преподавала в Йельском университете и была полностью погружена в исследования способа, которым вирусные молекулы РНК “взламывают” белоксинтезирующие системы в клетках. Хотя область моих исследований не слишком пересекалась с генной терапией, новости об этом катастрофическом исходе расстроили меня и одновременно заставили более целеустремленно работать над тем, чтобы лучше понимать устройство вирусов и клеток.
Позже, уже в начале 2000-х, у пяти пациентов, которым проводили генную терапию сцепленного с X-хромосомой ТКИД, развилась лейкемия – рак красного костного мозга. Это произошло из-за того, что ретровирус ошибочно активировал некий онкоген (один из генов, вызывающих рак), и это привело к неконтролируемому размножению клеток. Этот инцидент подчеркнул неотъемлемый риск, присущий методу, при котором пациентам вводятся большие количества чужеродного агента, а в их геномы случайно встраиваются несколько тысяч “букв” ДНК. Я помню, как тогда подумала, что эта область клинических исследований, в принципе столь многообещающая, может оказаться неприемлемо рискованной.
Кроме того, генная терапия по своей сути неэффективна для широкого ряда генетических заболеваний, которые не вызваны отсутствием или мутацией генов. Такие заболевания не могут быть исправлены простым добавлением новых генов в клетки. Возьмем, к примеру, хорею Гентингтона, при которой измененный ген вырабатывает белок аномального строения и действие этого гена полностью нивелирует действие другого, здорового. Так как мутантный ген доминирует над нормальным, простая генная терапия – то есть добавление еще одной нормальной копии гена с помощью специально видоизмененного вируса – никак не поможет в случае хореи Гентингтона или других заболеваний, наследуемых по доминантному типу.
В таких (и подобных) случаях врачам придется найти способ “починить” проблемные гены, а не просто заменить их. И если бы они научились восстанавливать дефектный код, вызывающий расстройства, то научились бы лечить как рецессивные, так и доминантные наследственные заболевания, не боясь при этом добавить ген не туда, куда следует.
Эта возможность интриговала меня с самого начала карьеры. В начале 1990-х, уже получив степень доктора философии в Гарвардском университете, я в течение многих вечеров обсуждала эту идею с коллегами по лаборатории в Колорадском университете в Боулдере, где я была постдоком. В те дни мы с моим другом и коллегой Брюсом Салленджером спорили обо всем подряд – от президентских выборов 1992 года (мне нравился Пол Цонгас, а Брюсу – Билл Клинтон) до различных стратегий генной терапии. Один из вопросов, который мы обсуждали, был таким: возможно ли отредактировать молекулы РНК – то самое связующее звено между ДНК и белком в клетке – таким образом, чтобы исправить мутации, которые эти молекулы “наследовали” от ДНК? Помимо всего прочего, это была тема исследовательского проекта Брюса. Иногда мы также обсуждали другую возможность: редактирование “исходного кода” таких дефектных РНК – то есть самой ДНК генома. Мы оба считали, что этот метод изменил бы все. Вопрос состоял лишь в том, удастся ли когда-нибудь воплотить эту идею в действительность.
На протяжении 1980-х, в то время как некоторые исследователи оттачивали методы переноса генов с использованием вирусов, другие искали более простые пути трансформации клеток млекопитающих, используя ДНК, изготовленную в лаборатории. Эти базовые методы предназначались прежде всего для фундаментальной науки, но со временем ученые начали также исследовать их потенциал для лечения клеток человека.
У этих подходов было несколько ключевых преимуществ перед более сложными техниками переноса генов. Прежде всего они были гораздо более быстрыми; вместо того чтобы “упаковывать” гены в перенастроенные вирусы, ученые могли вводить созданную в лаборатории ДНК напрямую в клетки или делать так, чтобы клетки сами поглотили ее: для этого последние погружались в специально приготовленную смесь ДНК и фосфата кальция. Во-вторых, хотя в этих более простых методах и не применялось встраивание новых генов в геномы клеток при помощи вируса, клетки могли объединять чужеродную ДНК со своей собственной – пусть и не слишком эффективно.
Мыши часто становились первыми подопытными животными, на которых тестировались эти техники, и ученые поражались тому, насколько эффективными оказывались такие методы применительно к маленьким созданиям. Вводя новую ДНК в оплодотворенные яйцеклетки мышей и затем имплантируя эти яйцеклетки в женские особи, исследователи обнаружили, что они могли перманентно встроить чужеродную ДНК в геномы представителей следующего поколения и вызвать наблюдаемые изменения в развивающихся животных. Эти достижения означали, что любой ген, который ученые были способны изолировать и клонировать в лаборатории, можно было попробовать ввести в клетку и изучить его поведение там; добавляя этот ген в клетки, ученые могли наблюдать его воздействие на организм и лучше понять его функции. Хотя моя научная работа в то время была в основном посвящена формам и функциям молекул РНК, я осознавала, что потенциальные последствия этих открытий были огромны.
Вопрос состоял в следующем: каким именно образом ДНК находит путь к геному? Марио Капекки, профессор университета Юты, пытался ответить на этот вопрос в начале 1980-х, сделав одно необъяснимое наблюдение: когда в один геном “подселяли” сразу много копий какого-нибудь гена, эти копии интегрировались в геном вовсе не беспорядочно, как этого можно было бы ожидать, а прямо наоборот. Капекки обнаружил, что копии гена, вместо того чтобы распределяться хаотическим образом по разным хромосомам генома, всегда собирались вместе в одной или немногих областях, при этом многие копии накладывались друг на друга, как будто их так собрали таким образом умышленно. Впоследствии ученый установил, что именно так оно и было.
Капекки наблюдал результаты процесса, называемого гомологичной рекомбинацией, – в тот момент это был уже хорошо известный феномен, однако ученый не ожидал наткнуться на него в этом эксперименте. Наиболее известный пример гомологичной рекомбинации – происходящая во время формирования яйцеклеток и сперматозоидов редукция каждого двойного набора хромосом (половину которого мы получили от матери, а половину от отца) до одинарного, который затем объединится со вторым таким же набором (у другого партнера) в ходе полового размножения. В этом процессе избавления от “лишнего” клетки выбирают смесь отцовских и материнских хромосом; каждая пара хромосом вступает в своего рода половой акт, обмениваясь крупными фрагментами ДНК таким образом, что генетическое разнообразие в пределах одной хромосомы увеличивается. Несмотря на головоломную сложность смешивания, сопоставления и пересборки цепей из миллионов “букв” ДНК, клетки могут выполнять эти задачи безупречно именно благодаря процессу гомологичной рекомбинации. Тот же процесс происходит во всех царствах живых существ: к примеру, бактерии с его помощью обмениваются генетической информацией, а биологи пользуются преимуществами гомологичной рекомбинации для проведения генетических экспериментов на дрожжах в течение многих лет.
Тем не менее открытие того факта, что клеткам лабораторных млекопитающих также свойственно явление гомологичной рекомбинации, имело огромное значение. Марио Капекки писал в конце своей статьи 1982 года:
Будет интересно определить, сможем ли мы использовать [вовлеченные в процесс ферменты], чтобы путем гомологичной рекомбинации направленно воздействовать на гены, расположенные в определенных участках хромосом.
Другими словами, гомологичная рекомбинация позволяет ученым с безупречной точностью вставлять гены в подходящие места генома – а это поразительное усовершенствование по сравнению со случайной вставкой генов с помощью вирусов. И, что еще важнее, гомологичная рекомбинация может дать ученым возможность “переписывать” дефектные гены, помещая здоровые гены прямо в то место, где произошла мутация.
Спустя всего три года после экспериментов Капекки эта возможность воплотилась в реальность в примечательной научной работе, статью о которой опубликовал Оливер Смитис с коллегами. Работая с человеческими клетками, взятыми из опухолей мочевого пузыря, ученые поставили перед собой задачу заменить “доморощенные” копии гена бета-глобина в клетках на искусственные рекомбинантные версии, сконструированные в лаборатории. Невероятно, но это сработало. Ученым не пришлось использовать никаких необычных трюков – они просто смешали ДНК с фосфатом кальция и опрыскали клетки полученной смесью – некоторые из клеток поглотили чужеродную ДНК, создали пары из разработанных в лаборатории цепочек ДНК и собственных подходящих последовательностей в геноме, а затем посредством некоторой “молекулярной гимнастики” заменили старые на новые.
Казалось, клетки могут проделывать большую часть сложной работы по модификации собственных геномов без посторонней помощи. Это означало, что ученые могли доставлять гены более мягким способом, не используя вирусы для “запихивания” новой ДНК в геном. Заставляя клетки “думать”, что рекомбинантная ДНК была лишь дополнительной хромосомой, которой нужно найти пару с подходящим геном, уже имеющимся в геноме, ученые могли гарантировать, что новая ДНК соединялась с изначально находящейся в клетке посредством гомологичной рекомбинации.
Ученые назвали этот новый подход к манипуляции с генами направленным воздействием на гены. Сегодня этот метод известен под другим именем: редактирование генома.
Потенциал этой технологии для генетических исследований был невероятно заманчив. Однако Смитис знал, что гомологичная рекомбинация может быть также использована и в качестве терапии. Если бы ученые смогли провести аналогичное направленное воздействие на гены в стволовых клетках пациентов, страдающих от серповидноклеточной анемии, то мутировавший ген бета-глобина можно было бы заменить на нормальную, здоровую последовательность. Открытие Смитиса было сделано в рамках экспериментального подхода, однако в один прекрасный день оно потенциально могло быть использовано для лечения заболеваний.
Другие лаборатории также вступили в конкуренцию за усовершенствование этой техники направленного воздействия на гены. Одной из них была лаборатория Капекки. В 1986-м, когда я была на втором курсе магистратуры, он показал, что гомологичная рекомбинация достаточно точна для того, чтобы исправлять даже точечные мутации в геноме и корректировать недостаточность ферментов в клетках. Два года спустя Капекки предложил общую стратегию направленного воздействия на любой ген с известной последовательностью нуклеотидов в любом геноме. Он также предположил, что гомологичную рекомбинацию можно использовать не только для исправления и “ремонта” генов, но и для их инактивации в исследовательских целях; “выключая” гены и наблюдая, что получится в результате, ученые могли определять функции этих генов.
Редактирование генома посредством гомологичной рекомбинации
К тому времени как я завершила работу над своей диссертацией на соискание степени доктора философии в конце 1980-х, направленное воздействие на гены широко применялось для редактирования ДНК в культурах клеток мышей и человека и даже в живых мышах. Важная работа, проведенная в лаборатории Мартина Эванса, продемонстрировала, что, направленно воздействуя на гены в эмбриональных стволовых клетках мышей и затем вводя эти измененные стволовые клетки обратно в мышиные эмбрионы, ученые могут создавать живых мышей с “дизайнерскими” изменениями. Важнейшие открытия, совершенные Капекки, Смитисом и Эвансом, впоследствии, в 2007 году, были удостоены Нобелевской премии по физиологии или медицине.
Впрочем, несмотря на свой колоссальный потенциал, редактирование генома поначалу больше подходило для фундаментальных исследований, чем для применения в лечении заболеваний у человека. Для ученых, исследующих генетику млекопитающих и пытающихся найти способы, которыми можно было бы выявить функции различных генов, метод направленного воздействия на гены в корне менял все. Однако исследователи-медики с настороженностью относились к использованию этого метода на людях, поскольку, несмотря на весь свой потенциал, гомологичная рекомбинация совсем не оправдывала ожиданий в том, что касалось лечения.
Возможно, самым важным сдерживающим фактором была проблема негомологичной (или незаконной) рекомбинации, при которой новая ДНК интегрируется в геном случайным образом, вместо того чтобы оказаться точно у подходящей последовательности. Фактически незаконная рекомбинация, похоже, происходила почти в сто раз чаще гомологичной, и, естественно, терапевтические перспективы технологии, которая могла исправить мутировавший ген лишь в 1 % измененных клеток, а в геном остальных 99 % “вклеивала” ДНК как попало, не выглядели слишком многообещающими. Ученые разрабатывали различные изящные пути обхода этой проблемы в клеточных культурах и не теряли надежду на то, что в будущем метод удастся применить в медицине. Как заявил Капекки в начале 1990-х, “в конце концов, гомологичная рекомбинация – единственный потенциально возможный метод генной терапии человека”. Однако в то время казалось, что редактирование генома – просто недостаточно совершенная технология для того, чтобы применять ее на людях.
В начале 1980-х, пока другие ученые были поглощены мыслями о направленном воздействии на гены в клетках человека, Джек Шостак пытался разобраться в процессе клеточного деления у дрожжей. Шостак был профессором Гарвардской медицинской школы (и затем моим научным руководителем в работе над докторской диссертацией), и его занимал фундаментальный вопрос: как вообще возможны направленное воздействие на гены и гомологичная рекомбинация? В частности, Шостак хотел понять, каким образом две цепочки ДНК из одной хромосомы могут объединяться с двумя соответствующими цепочками ДНК из второй хромосомы, обмениваться информацией, слившись на время некой промежуточной стадии, и затем разделяться вновь, заново образуя отдельные хромосомы после деления клетки.
В 1983 году, когда я все еще была студенткой Помона-колледжа в Калифорнии, Шостак на другом конце страны решил, что нашел ответ. Основываясь на результатах экспериментов по генетике дрожжей, он и его магистрантка Терри Орр-Вивер вместе с профессорами Родни Ротштайном и Фрэнком Сталем обнародовали смелую модель, согласно которой провоцирующим фактором – сигналом, запускающим процесс гомологичной рекомбинации, – было разрезание одной из двух хромосом, что приводило к двуцепочечному разрыву ДНК. Согласно этой модели, двуцепочечный разрыв и освободившиеся концы ДНК на месте разрыва были особенно подвержены слиянию, а располагающиеся по бокам их последовательности с гораздо большей вероятностью могли быть вовлечены в обмен генетической информацией с соответствующей хромосомой (или, в случае редактирования генома, – с соответствующей ДНК, которую предоставлял исследователь).
К тому времени как я пришла в лабораторию Шостака в 1986 году, он уже сменил центральную повестку своих исследований на изучение роли молекул РНК на начальных этапах эволюции жизни на Земле. Однако в лаборатории мы с коллегами обсуждали модель двуцепочечных разрывов, ее изящество и тот неприкрытый скепсис, с которым она была встречена в научном сообществе. Но с течением времени становилось все яснее, что эта модель согласуется с большим количеством экспериментальных данных. Механизм репарации двуцепочечных разрывов казался логичным не только в случае процесса гомологичной рекомбинации при формировании яйцеклеток и сперматозоидов, но и при рекомбинации, происходящей каждый раз, когда была повреждена ДНК. Все клетки подвержены разрушительным для ДНК воздействиям, будь то рентгеновское излучение или канцерогены, и надо отметить, что клетки весьма эффективно справляются с репарацией таких разрывов, не теряя при этом генетической информации. Согласно модели Шостака, этот процесс репарации зависел от возможности хромосом обмениваться фрагментами посредством гомологичной рекомбинации, и именно поэтому наличие двух копий хромосом является выгодной эволюционной стратегией. Любое повреждение одной из хромосом можно репарировать, просто скопировав соответствующую последовательность со второй хромосомы.
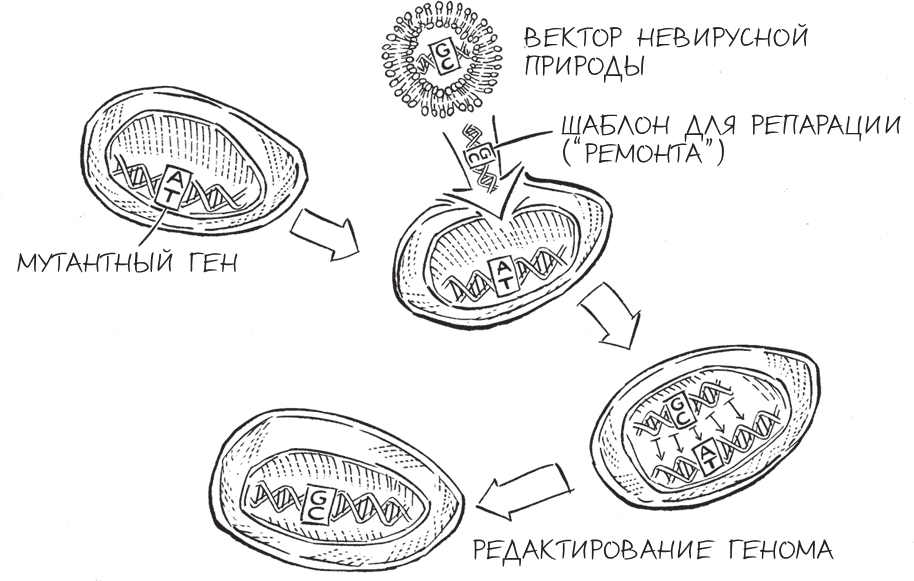
Если модель двуцепочечных разрывов верна и выводы, полученные на дрожжах, справедливы и для млекопитающих, возникает очевидная возможность улучшить эффективность редактирования генома: сделать надрез в ДНК в точности в том месте, где необходимо провести редактирование. Если предстоит заменить дефектный ген в геноме на исправленную копию, созданную в лаборатории, то сначала нужно понять, как разрезать дефектный ген, вызвав локальный двуцепочечный разрыв в ДНК, – а затем добавить исправленную копию гена. Клетка, “почувствовав” разрыв, попыталась бы восстановить повреждение, начав поиск соответствующей хромосомы для копирования, – тут-то ученые и “подсунули” бы ей синтезированный ген. По сути дела, можно было заставить клетку “подумать”, что повреждение ее ДНК произошло по естественным причинам, и предоставить ей новый фрагмент ДНК под видом второй хромосомы, которую клетка могла бы использовать для репарации поврежденного участка.
В 1994 году исследователи из лаборатории Марии Джесин в Мемориальном онкологическом центре имени Слоуна – Кеттеринга (Нью-Йорк) стали первыми, кому удалось “обмануть” таким образом клетки млекопитающих, – об этом прорыве я читала с большим интересом, находясь неподалеку, в Нью-Хейвене, куда я только что приехала после завершения работы постдоком в Боулдере. Мне было чрезвычайно интересно узнать об этой важной работе, которая была основана на предложенной моим научным руководителем модели двуцепочечных разрывов и выполнена исследовательницей, которая, как и я, была увлечена молекулами жизни.
Эксперименты по редактированию генома, проведенные Джесин, были оригинальными и новаторскими. Ее стратегия заключалась в введении в мышиные клетки ферментов, разрезающих геном и создающих двуцепочечные разрывы; одновременно с этим она добавляла в клетки фрагменты синтезированной ДНК (шаблоны для репарации), соответствующие разрезанной последовательности ДНК. Затем исследовательница проверяла, получилось ли у мышиных клеток восстановить поврежденную ДНК с помощью вставки шаблона для репарации. Проводя этот же самый эксперимент с добавлением фермента и без него, Джесин смогла проверить свою гипотезу, что искусственно созданный двуцепочечный разрыв повышал эффективность гомологичной рекомбинации.
Сложность заключалась в том, чтобы подобрать подходящий фермент, разрезающий геном только в одном определенном месте из миллиардов возможных вариантов. Чтобы решить эту проблему, Джесин остроумно позаимствовала часть молекулярного механизма из дрожжей: эндонуклеазу I-SceI.
Нуклеазы – это ферменты, разрезающие нуклеиновые кислоты; одни режут РНК, другие – ДНК. Эндонуклеаза делает “надрез” где-то внутри цепочек, в отличие от экзонуклеаз, которые работают исключительно с концами цепочек. Некоторые эндонуклеазы чрезвычайно губительны для клеток, поскольку они “режут” практически любой фрагмент ДНК, который встречается им на пути, вне зависимости от последовательности нуклеотидов в нем. Другие эндонуклеазы действуют очень специфично и разрезают только строго определенные последовательности; а большинство ведет себя как нечто среднее между первыми и вторыми.
Эндонуклеаза I-SceI, которую выбрала Джесин, была одной из наиболее специфических эндонуклеаз, известных к тому времени: фрагмент ДНК должен был содержать определенную последовательность из восемнадцати нуклеотидов, чтобы фермент сделал в нем разрез. Использование высокоспецифичной эндонуклеазы было критически важно: если бы Джесин выбрала слишком “неразборчивый” фермент, он бы “порезал” геном как попало, и это не только сделало бы результаты более сложными для интерпретации, но и, вероятно, повредило бы клетку. Однако, обладая специфичностью к восемнадцатибуквенной последовательности ДНК, I-SceI разрезает только один фрагмент ДНК из более чем пятидесяти миллиардов возможных комбинаций. (По иронии судьбы, в мышином геноме нет подходящей последовательности из восемнадцати “букв”, поэтому, прежде чем приступить к своему эксперименту, Джесин пришлось добавить копию этой последовательности в ДНК мышей – чтобы ферменту было что резать.)
Результаты эксперимента Джесин были потрясающими. Она добилась того, что точная репарация мутировавшего гена посредством гомологичной рекомбинации прошла в целых 10 % клеток; сейчас эта эффективность может показаться не слишком высокой, однако это было в сотни раз лучше, чем у лучших из достигнутых к тому времени результатов. На тот момент это было наиболее многообещающее свидетельство того, что гомологичная рекомбинация может рано или поздно позволить ученым переписывать генетический код без риска незаконной рекомбинации или риска случайного встраивания в геном различных последовательностей при использовании ретровирусных векторов. Стоит лишь инициировать двуцепочечный разрыв в нужном месте – и фактически все остальное клетки сделают сами.
Имелась только одна проблема: чтобы этот подход можно было практически использовать, нужно было научиться разрезать геном в строго заданных местах. В эксперименте Джесин для проверки правильности идеи последовательность, которую распознавала эндонуклеаза I-SceI, была искусственно добавлена в геном перед введением нуклеазы, однако последовательности многих болезнетворных генов, скажем так, незыблемы: их невозможно изменить таким образом, чтобы они “пришлись по вкусу” тому или иному придирчивому ферменту. После разрыва геном легко восстанавливался и включал в себя новую генетическую информацию – хитрость была в том, чтобы понять, как сделать разрыв в нужном месте.
Начиная с середины 1990-х, пока я разбиралась со структурами молекул РНК с их уникальным биохимическим поведением, другие ученые спешили разработать новые системы, которые, подобно I-SceI, могли бы направленно действовать на конкретные последовательности ДНК. Тот, кому удалось бы решить эту проблему, смог бы раскрыть весь потенциал редактирования генома.
К этим технологиям нового поколения предъявлялось три критически важных требования: они должны были распознавать определенную выбранную последовательность ДНК; уметь разрезать эту последовательность и легко подвергаться перепрограммированию, для того чтобы атаковать различные последовательности ДНК и инициировать их разрыв. Первые два условия были необходимы для создания двуцепочечных разрывов, а третье – для того, чтобы этот инструмент был максимально универсален. I-SceI превосходно отвечала двум первым критериям, однако совершенно не соответствовала третьему. Биоинженеры поняли: чтобы создать программируемую систему разрезания ДНК, нужно либо перестроить I-SceI таким образом, чтобы она могла атаковать разные последовательности, либо найти совершенно новую нуклеазу, которая уже “научилась” разрезать самые различные последовательности ДНК.
Попытки ученых видоизменить I-SceI не достигли цели (что и неудивительно, учитывая крайне сложное молекулярное устройство белков-ферментов), и вскоре стало ясно, что поиск других природных нуклеаз – гораздо более перспективный подход. Фактически, к тому моменту, когда Джесин вела свои эксперименты с I-SceI, ученые уже выделили десятки нуклеаз из целого ряда организмов и установили конкретные последовательности ДНК, служившие мишенями для этих ферментов. Однако существовала фундаментальная проблема: подавляющее большинство ферментов распознавали последовательности длиной лишь в 6 или 8 “букв” – то есть слишком короткие для того, чтобы с таким ферментом можно было работать. В геноме человека подобные последовательности встречаются десятки или даже сотни тысяч раз, и это означает, что, даже если нуклеаза способна стимулировать гомологичную рекомбинацию в одном гене, она в процессе может “порубить” почти весь геном. Клетка была бы разрушена еще до того, как у нее появится какой-либо шанс начать репарацию ДНК.
Исследователи не могли положиться ни на одну из ранее открытых нуклеаз, а поиск нового фермента, подобного I-SceI, для каждой новой попытки редактирования генома – задача совершенно неосуществимая. Если вы хотите превратить терапевтическое редактирование генома в эффективную технологию исправления болезнетворных мутаций, то медики не могут в каждом случае ждать, пока вы обнаружите нуклеазу, которая бы избирательно действовала именно на тот участок заданного гена, в котором у конкретного пациента вредоносная мутация. Вам необходима возможность “взять с полки” подходящую нуклеазу из уже открытых – или по крайней мере технология, позволяющая создавать нужные нуклеазы по мере необходимости.
Революционное исследование, предложившее решение этой проблемы, было проведено в 1996 году, хотя я тогда о нем не знала. Шринивасан Чандрасекаран, профессор из Университета Джонса Хопкинса, понял, что вместо создания нуклеаз “с нуля”, поиска новых в природе или переделывания I-SceI можно избрать смешанный подход: выбирать фрагменты существующих белков и комбинировать их. Такие химерные нуклеазы отвечали бы двум первым требованиям к редактирующей геном нуклеазе: они были бы способны распознавать определенную выбранную последовательность ДНК и делать в ней разрез.
Чандрасекаран решил собрать химерную нуклеазу из фрагментов двух встречающихся в природе белков, которые отлично справлялись с распознаванием и разрезанием последовательностей ДНК соответственно. Для разрезания Чандрасекаран выбрал участок бактериальной нуклеазы под названием FokI, который мог инициировать разрывы в ДНК, но не обладал предпочтениями к каким-либо последовательностям. А для “нацеливания” он приспособил повсеместно распространенные натуральные белки с цинковыми пальцами (ZFN), названные так потому, что они распознают ДНК, используя похожие на пальцы структуры, связанные ионами цинка и расположенные рядом друг с другом подобно пальцам на руке. Так как эти белки с цинковыми пальцами состоят из многократно повторяющихся, тандемно расположенных участков и каждый участок распознает определенную последовательность из трех “букв” ДНК, казалось вероятным, что ученые могут видоизменить эти белки, комбинируя фрагменты по-разному, чтобы они распознавали различные последовательности ДНК.
Удивительно, но химерная нуклеаза, судя по всему, сработала. Соединив “режущий” фрагмент FokI с распознающим ДНК участком белка с цинковыми пальцами, команда Чандрасекарана продемонстрировала, что искусственно составленная нуклеаза распознавала и резала именно ту ДНК, что ожидали ученые, – даже несмотря на то, что они смешали два белковых компонента из совершенно различных источников.
Вскоре Чандрасекаран пригласил к сотрудничеству профессора университета Юты Дану Кэрролл, чтобы использовать эти новые нуклеазы с цинковыми пальцами (ZFN) в более прикладных целях. Вместе они продемонстрировали, что ZFN работают и в яйцеклетках лягушки (популярной среди биологов модельной системе) и что сделанные ZFN разрывы в ДНК стимулировали гомологичную рекомбинацию. Затем, работая с плодовыми мушками, сотрудники лаборатории Даны Кэрролл сумели запрограммировать новую ZFN на направленное воздействие на ген yellow (один из генов, определяющих окраску тела) и показали, что эта стратегия может обеспечить заданное генетическое изменение во всем организме. Это был очень важный шаг в развитии редактирования генома. ZFN проявили себя не только подходящими для применения в организмах животных; что более важно, их оказалось можно видоизменить таким образом, чтобы их мишенями стали другие, новые гены.
Научное сообщество вскоре подхватило эстафету, и исследователи начали разрабатывать ZFN под собственные цели, выбирая в качестве мишеней новые гены и работая с новыми модельными объектами. В 2003 году Мэттью Портеус и Дэвид Балтимор первыми показали: ген в клетке человека можно редактировать с высокой точностью, используя специально созданную ZFN. Вскоре после этого Федор Урнов и его коллеги исправили в клетках человека мутацию, вызывающую сцепленный с X-хромосомой ТКИД. Возможности использования редактирования генома для направленного воздействия на наследственные заболевания еще никогда не казались настолько близкими к реальности.
Тем временем ZFN также начали использовать в лабораториях, которым редактирование генома было необходимо совсем для других целей – например, создания “дизайнерских” злаков или животных моделей. В конце 2000-х технологию успешно применили к резуховидке Таля, табаку и кукурузе, показав, что двуцепочечные разрывы ДНК способствуют высокоэффективной гомологичной рекомбинации во многих типах клеток, а не только в клетках млекопитающих. В это же время стали появляться публикации, в которых рассказывалось об использовании ZFN для изменения генов у пресноводных лучеперых рыб данио-рерио, червей, крыс и мышей. Это направление работы выглядело интригующе и неизменно привлекало мое внимание – и в научных статьях, и на конференциях. Его потенциал казался чрезвычайно мощным.
Однако, несмотря на свою кажущуюся перспективность, белки ZFN никогда не применялись широко за пределами небольшого числа лабораторий. Исследователи, использовавшие эти нуклеазы, либо сами обладали громадным опытом в области белковой инженерии, либо сотрудничали с теми немногими лабораториями, в которых подобные эксперименты уже проводились, либо могли позволить себе платить баснословные деньги за нуклеазы, сконструированные на заказ. В теории создание ZFN было простым: нужно было просто соединить различные фрагменты белков с цинковыми пальцами, чтобы они распознавали последовательность ДНК, которую исследователь желает отредактировать. Однако на практике это было очень сложно. Большая доля создаваемых ZFN попросту не распознавали те последовательности ДНК, которые должны были распознавать; другие были слишком неразборчивы и воздействовали на первые попавшиеся участки ДНК, лишь отдаленно похожие на целевые, и убивали клетки, геном которых должны были отредактировать. В других случаях фрагмент с цинковыми пальцами успешно распознавал ДНК, однако нуклеазный фрагмент не разрезал ее.
Подобно тому как изменение I-SceI оказалось слишком сложной задачей, так и ZFN тоже, как выяснилось, было нелегко перепрограммировать, чтобы использовать в качестве универсального инструмента редактирования генома. Конечно, результаты экспериментов с ZFN убедительно доказали, что специально видоизмененные нуклеазы полезны, если редактирование генома – самоцель, однако в этой области науки все еще нужна была новая технология, более надежная и простая в использовании.
Такая технология – или, по крайней мере, первая ее версия – была открыта в 2009 году при изучении новых типов белков, найденных в патогенных бактериях рода Xanthomonas, поражающих растения. Эти белки, которые были названы активатороподобными эффекторами транскрипции (transcription activator – like effectors, TALE), были удивительно похожи по своему строению на белки с цинковыми пальцами: они состоят из многократно повторяющихся фрагментов, и каждый фрагмент распознает определенную область ДНК. Однако от белков ZNF их отличала важная деталь: в то время как каждый “палец” в последних распознает трехбуквенную последовательность ДНК, каждый фрагмент TALE-белков узнает всего одну “букву” ДНК. Это различие позволило ученым легко определить закономерность, по которой фрагмент будет распознавать определенную “букву” ДНК, и затем они просто расположили эти фрагменты один за другим таким образом, чтобы они распознавали более длинную последовательность ДНК в гене. В случае ZFN это лишь казалось легко сделать, однако с TALE процедура в самом деле была простой.
Ученые быстро взялись за исследование новейшей “зацепки”. Вскоре после того, как был расшифрован этот код, три лаборатории соединили белки TALE с теми же режущими ДНК фрагментами, что есть в ZFN, и создали нуклеазы TALE, или TALEN. TALE-нуклеазы были очень эффективны для инициации редактирования генома внутри клеток, и после того как удалось еще несколько усовершенствовать их строение, стало очень похоже на то, что TALEN будет гораздо проще создавать и применять, чем ZFN.
“Но как жаль бедняжек TALEN”, – писала Дана Кэрролл в статье, описывающей историю появления редактирования генома. Потому что, как только TALEN обнаружили и адаптировали для редактирования, их вытеснило следующее, и возможно последнее, открытие в области редактирования генома. Эта технология получила название CRISPR, и здесь моя история соединяется с историей редактирования генома – и вообще с этим длинным маршем истории науки, которая в тот момент подошла к порогу новой головокружительной эры.
Назад: Часть I Инструмент
Дальше: Глава 2 Новая защита

