Книга: Мозг. Такой ли он особенный?
Назад: Чем больше нейроны, тем больше отношение числа глиальных клеток к числу нейронов
Дальше: Так почему же человеческий мозг так дорог?
Сколько стоит нейрон?
В этом пункте мы знали, что отношение числа глиальных клеток к числу нейронов возрастает вместе со средним размером нейронов в ткани: более крупные нейроны встречаются с большим числом сопровождающих их глиальных клеток, как предположили в 1957 году Хокинс и Ольшевский. Но имеет ли этот факт какое-нибудь отношение к возросшей метаболической цене более крупных нейронов, что требует больше глиальных клеток для энергетической поддержки нервных клеток, как считали авторы?
Такое предположение представлялось вполне разумным и обоснованным. Поскольку нейроны по определению являются возбудимыми клетками, способными к деполяризации и реполяризации своих мембран, то можно считать, что более крупные нейроны требуют больше энергии, так как площадь возбудимых мембран у них больше, а значит, большая поверхность реполяризуется после возбуждения, то есть деполяризации; смена деполяризации и реполяризации служит характерным признаком нейронной активности. Деполяризация протекает без затрат энергии, она бесплатна – это то же самое, что открыть ворота шлюза: вода устремляется по градиенту силы тяжести; но для того, что закачать воду обратно, требуется использовать насос, то есть реполяризация требует немалых энергетических затрат.
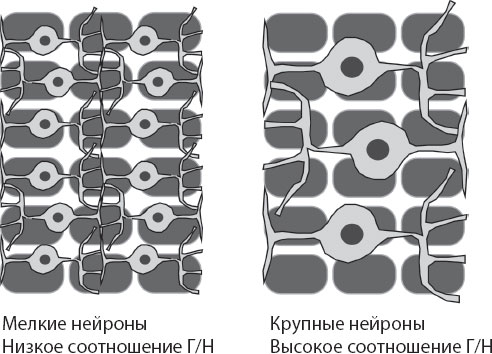
Рис. 9.9. Если средний размер глиальных клеток (скругленные прямоугольники на схеме) практически неизменен, то число глиальных клеток на данный объем мозговой ткани можно считать постоянным. Но поскольку один и тот же объем ткани может состоять из большого числа мелких нейронов (слева), небольшого числа крупных нейронов (справа) или из любой промежуточной комбинации, то отношение числа глиальных клеток к числу нейронов в каждой ткани просто зависит от среднего размера нейронов ткани: чем больше средний размер нейронов, тем выше отношение глия/нейроны в этой ткани
Кроме того, у крупных нейронов, как полагают, больше синапсов, а возбудительные синапсы, использующие в качестве медиатора глутаминовую кислоту, потребляют много энергии для ресинтеза глутамата и восполнения запасов синаптических пузырьков. В блестящем исследовании Дэвида Этвелла и Саймона Лафлина было показано, что почти 80 % энергии нейрона тратится на глутаматэргическую передачу, а 13 % уходит просто на поддержание трансмембранного потенциала покоя. Несмотря на то что высокая энергетическая стоимость синаптической передачи может в принципе снижаться за счет регуляции нейронной активности и числа синапсов, обойти расходы, связанные с процессом реполяризации мембраны, невозможно, так как любое возбуждение – это деполяризация, за которой неизбежно следует реполяризация, то есть восстановление потенциала покоя. Крупный нейрон должен потреблять больше энергии для поддержания поляризационного потенциала покоя, потому что отсутствие реполяризации, обусловленное высокой концентрацией внутриклеточного кальция, равносильно клеточной смерти.
Но действительно ли крупные нейроны расходуют больше энергии? Исследование этой гипотезы требует определения расхода энергии отдельно взятым нейроном и зависимости такого расхода от среднего размера нервной клетки. Насколько мне хотелось знать ответ, настолько я была не готова заняться совершенно новым поприщем и начать измерять, сколько энергии потребляют нейроны разных размеров в разных отделах головного мозга.
По счастью, литература пришла на помощь: некоторые ученые, занимавшиеся совершенно иными проблемами, могли поместить бодрствующих животных шести видов приматов и грызунов в камеру позитронно-эмиссионного томографа (ПЭТ) для того, чтобы посмотреть, с какой скоростью их мозг потребляет глюкозу и кислород. Более того, полученные данные были упорядочены польским физиком Яном Карбовским, который исследовал вопрос о том, как метаболизм головного мозга изменяется в зависимости от его массы (но не от количества нейронов). Карбовский подтвердил, что удельный метаболизм головного мозга (потребление глюкозы на 1 г мозговой ткани в минуту) снижается по мере увеличения массы головного мозга у млекопитающих. Это снижение описывается степенной функцией с экспонентой –0,15. При такой зависимости мозг с массой, в десять раз большей, характеризуется удельным метаболизмом, который составляет лишь 70 % от удельного метаболизма мозга, который в десять раз меньше, что можно было объяснить либо меньшим числом крупных нейронов в ткани, либо, как считал сам Карбовский, уменьшением средней частоты разрядов в более крупном мозге. Такой мозг будет обходиться организму тем не менее дороже, чем мозг меньшей массы; при десятикратной разнице в массе более тяжелый мозг будет потреблять в семь раз больше энергии: произведение десятикратно большей массы на 70 % удельной энергии дает именно такой результат. Таким образом, Карбовский обнаружил, что больший мозг потребляет больше энергии пропорционально массе мозга, возведенной в степень +0,85, у всех исследованных видов. Это означает, что метаболическая стоимость мозга возрастает быстрее, чем метаболическая стоимость организма в целом по мере увеличения его массы. Макс Клейбер показал, что экспонента зависимости равна в последнем случае +0,75. Представляется, что выращивание большого мозга обходится дороже, чем выращивание большого тела, что позволяет объяснить, почему масса мозга растет у млекопитающих медленнее, чем масса тела, как мы уже видели в главе 8.
Единственная проблема заключалась в том, что данные Карбовского расходились с тем, что нам только что удалось узнать: Карбовский объединил в одну группу приматов и грызунов, как если бы они подчинялись одним и тем же правилам нейронного шкалирования, то есть у них было одинаковое соотношение между числом нейронов, размером мозга и плотностью упаковки нейронов, что, как показали мы, не соответствует действительности. Более того, теперь мы знали, сколько нейронов содержится в каждом мозге, для которого, благодаря работе Карбовского, мы знали данные о потреблении глюкозы и кислорода, а также нам были известны значения нейронной плотности в различных мозговых структурах, откуда мы могли вывести средний размер нейрона. Я была в положении человека, первым получившего возможность узнать, как средняя метаболическая стоимость нейрона изменяется в зависимости от его размера: действительно ли она растет, как предсказывали Хокинс и Ольшевский?
Я использовала данные Карбовского по средней энергетической стоимости бодрствующего мозга трех видов грызунов (мыши, крысы и белки) и трех видов приматов (макака, бабуина и человека). К 2010 году, зная число нейронов, содержащихся в мозге каждого из этих видов, я могла, применив простейшие расчеты, определить среднюю метаболическую стоимость одного нейрона у каждого из шести видов, как для мозговой коры и мозжечка по отдельности, так и для всего мозга в целом.
То, что я обнаружила, было поистине удивительно: среднее потребление глюкозы и кислорода на один нейрон оказалось постоянным и одинаковым во всех мозговых структурах у всех шести видов. Несмотря на то что межвидовая разница в числе нейронов достигала 1200 раз, а сами клетки в размерах варьировали в три раза, потребление глюкозы на один нейрон отличались между видами с разницей всего в 1,4 раза, от 4,93 × 10–9 микромоль глюкозы на 1 нейрон в минуту у макака до 7,05 × 10–9 микромоль у белки. Средняя метаболическая стоимость человеческого мозга оказалась точно посередине, с показателем 5,44 × 10–9 микромоль глюкозы на 1 нейрон в 1 минуту. Это означает, что в одну минуту один человеческий нейрон потребляет 3,3 миллиарда молекул глюкозы, что кажется очень большой величиной. Но на самом деле это не так уж много. При скорости потребления глюкозы, равной 3,3 миллиарда в минуту на 1 нейрон, 1 г глюкозы, четверть чайной ложки, содержит достаточно молекул глюкозы для того, чтобы кормить все 86 миллиардов нейронов головного мозга в течение 12 минут, а 5 г (1,25 чайной ложки) хватит на то, чтобы кормить мозг в течение целого часа!
Не только не было больших колебаний среднего потребления энергии на один нейрон при сравнении этого показателя у разных видов – средний человеческий нейрон стоит немного больше, чем нейрон макака, и немного меньше, чем нейрон белки, – но при этом отсутствует значимая корреляция между плотностью упаковки нейронов (показатель, обратный размеру нейрона) и средним потреблением энергии на один нейрон в разных мозговых структурах (рис. 9.10). Более крупные нейроны не стоят дороже.
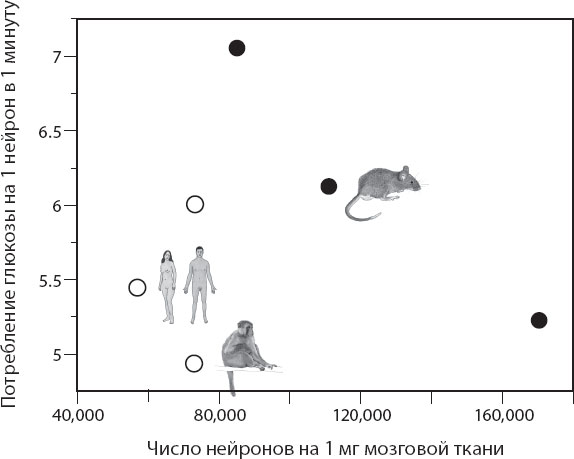
Рис. 9.10. Средняя энергетическая цена одного нейрона головного мозга (в микромолях глюкозы на 1 нейрон в 1 минуту) немного варьирует у мыши, крысы, белки (темные кружки) в сравнении с макаками, бабуинами и людьми (светлые кружки) и, что самое важное, не проявляет заметной корреляции со средней плотностью упаковки нейронов в мозге: более крупные нейроны (с низкой плотностью упаковки) потребляют не больше глюкозы в одну минуту, чем более мелкие (с более высокой плотностью упаковки)
Это был тяжелый удар по теории, согласно которой более крупные нейроны окружены большим числом глиальных клеток, потому что требуют больше энергии: более высокое отношение числа глиальных клеток к числу нейронов, характерное для более крупных нейронов в любой мозговой структуре, у любого вида животного, нельзя соотносить с повышенной потребностью в метаболической поддержке.
Еще более важно, что поскольку средняя энергетическая цена одного нейрона мало варьирует у разных видов, постольку общая энергетическая стоимость каждого отдельного мозга возрастает в простой линейной зависимости от общего числа нейронов в мозге, неважно, у приматов или грызунов, как показано на рис. 9.11, несмотря на разные правила нейронного шкалирования, соотносящие число нейронов и массу мозга этих таксономических групп животных. Чем больше в мозге нейронов, тем больше энергии потребляет этот мозг – по закону прямой пропорциональности.
Эта прямая пропорциональность иллюстрируется тем фактом, что мозг мыши, содержащий 71 миллион нейронов, потребляет 0,37 микромоля глюкозы в одну минуту; мозг макака, имеющий почти в сто раз больше нейронов (6,4 миллиарда), потребляет почти в сто раз больше глюкозы в одну минуту (31,4 микромоля), а мозг человека, который содержит нейронов в 1200 раз больше, чем мозг мыши, потребляет более чем в 1200 раз больше глюкозы, чем мозг мыши, – 497,9 микромоль в 1 минуту. В течение суток 71 миллион нейронов мышиного мозга потребляет 0,11 г глюкозы, или всего 0,4 килокалории в сутки, – для этого мышке надо откусить кусочек печенья, если она его найдет. Мозг макака с его 6,4 миллиарда нейронов потребляет 9,6 г глюкозы в сутки, то есть всего 38 килокалорий, что не очень много. По закону все той же прямой пропорциональности, мозг человека с его 86 миллиардами нейронов потребляет 129 г глюкозы для того, чтобы работать сутки, или 516 килокалорий. Такое количество калорий обеспечивает чашка сахара.
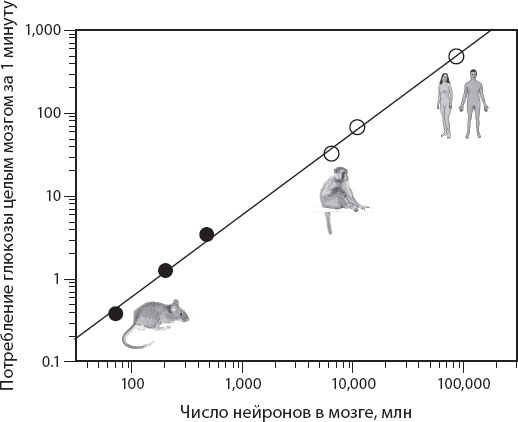
Рис. 9.11. Тотальное потребление энергии целым мозгом (в микромолях глюкозы за 1 минуту) возрастает по закону линейной зависимости у мышей, крыс, белок (темные кружки) и макака, бабуина и человека (светлые кружки). То есть чем больше нейронов содержит головной мозг, тем больше энергии он потребляет по закону прямой пропорциональности
Среднее потребление глюкозы на 1 нейрон в одну минуту в мозговой коре, равное 15,0 × 10–9 микромоль глюкозы, почти в 20 раз больше, чем в мозжечке, потребляющем 0,9 × 10–9 микромоль глюкозы, и эта пропорция между двумя структурами остается практически постоянной у всех шести исследованных видов. Разница может быть обусловлена несопоставимыми размерами нейронов этих структур, поскольку нейроны коры мозга намного крупнее, чем в мозжечке, у всех шести видов. На первый взгляд это может противоречить данным о том, что более крупные нейроны не потребляют больше энергии. Тем не менее следует ожидать, что более крупные корковые нейроны образуют большее число синапсов, чем мелкие нейроны типа крошечных зернистых клеток мозжечка. Так как энергетическая стоимость нейронов, как полагают, зависит от числа глутаматэргических возбудительных синапсов, то надо ожидать, что крупные нейроны с большим числом синапсов будут потреблять больше энергии, чем мелкие нейроны с малым числом синапсов. Однако наши данные указывают на то, что внутри каждой группы нейронов, корковых или мозжечковых, колебания размеров клеток среди разных видов не сопровождаются ни увеличением, ни уменьшением потребления энергии: нейроны одного типа стоят одинаково у разных видов независимо от размеров и характеризуются фиксированным средним энергетическим бюджетом в расчете на один нейрон.
Немного фундаментальных знаний о масштабах потребления энергии другими клетками организма поможет по-другому взглянуть на смысл фиксированного энергетического бюджета нейронов. Хотя интуитивно имеет смысл, что более крупный нейрон должен потреблять больше энергии, с биологической точки зрения это натяжка. В других органах, например в печени, метаболическая активность клеток уменьшается с увеличением размеров тела. Следуя такой логике, можно ожидать, что более крупный нейрон будет потреблять меньше энергии, а не столько же, сколько мелкий, и, уж во всяком случае, не больше. Относительно постоянные значения потребляемой энергии на 1 нейрон у млекопитающих с более низкой плотностью упаковки нейронов (то есть с большими размерами этих клеток) позволяют предположить, что энергетический бюджет одного нейрона, в противоположность энергетическому бюджету других типов клеток, практически достигает своего предела, накладывая, таким образом, ограничение на нейронную активность. Такой сценарий позволяет примирить низкую метаболическую стоимость грамма мозговой ткани млекопитающих с данными сравнительного генетического анализа: гены, отвечающие за клеточный метаболизм, относятся к генам, демонстрирующим наибольшую изменчивость в ходе эволюции человека, что позволяет предположить, что поддержание постоянного метаболизма в мозговых нейронах коренится в эволюционных генетических изменениях.
Помимо этого, существуют доказательства того, что энергетический бюджет индивидуальных нейронов ограничен не только млекопитающими, но и по времени внутри каждого индивидуального мозга, учитывая, что он не допускает больших колебаний нейронной активности. Несмотря на то что увеличение частоты нейронных разрядов вызывает прямо пропорциональное увеличение потребления энергии в человеческом мозге, это увеличение очень невелико. «Активация» участков человеческого мозга на фоне соматосенсорной стимуляции, проявляющаяся яркими красными участками на магнитно-резонансных томограммах (МРТ), говорит о резком увеличении потребления энергии в заинтересованных участках, но такая симуляция вызывает лишь 5-процентное повышение уровня метаболизма в соматосенсорной коре бодрствующего человека, а зрительная стимуляция вызывает в лучшем случае 8–12-процентное увеличение метаболической активности в зрительной коре бодрствующего человека. В типичных случаях «активация мозга», на которую указывают красные участки на МРТ, проявляется не более чем 2–5-процентным усилением метаболизма нейронов. Удивительно, как много мы можем делать за счет столь незначительных колебаний потребления энергии мозговыми нейронами.
Энергетический бюджет нейронов является одновременно ограничивающим и критически важным фактором сохранения сознания. Поскольку доставка энергии мозговым нейронам напрямую зависит от мозгового кровотока, постольку уменьшение кровоснабжения мозга всего на 1 % может вызвать значительные нарушения работы мозга, до потемнения в глазах, обморока и потери сознания. Когда мы слишком быстро встаем из положения лежа и рефлексы не успевают поднять артериальное давление до уровня, оптимального для нормального кровоснабжения мозга и доставки кислорода, необходимого для расщепления глюкозы, то первой страдает зрительная кора, что проявляется потемнением в глазах. Точно так же снижение потребления глюкозы или кислорода на 45 % в состоянии общей анестезии вполне укладывается в идею о том, что поддержание сознания сильно зависит от доступной мозгу энергии. Доступного нейронам энергетического бюджета едва хватает для простого поддержания здоровой деятельности мозга, достаточной для поддержания бодрствующего состояния и сознания: нейроны постоянно упираются в предел доступной им энергии. Нет поэтому никакого чуда в том, что мозг особенно чувствителен к уменьшению кровоснабжения, приводящему к снижению доставки кислорода и глюкозы. По той же причине хронические нарушения метаболизма нейронов вполне ожидаемо будут приводить к поражению мозговых функций и способствовать патологии мозга; такие нарушения метаболизма имеют место при эпилепсии (когда процессы возбуждения нейронов выходят из-под контроля), при болезнях митохондрий (в этих случаях мозг повреждается из-за нарушения переноса энергии), при болезни Альцгеймера (когда нейроны теряют чувствительность к инсулину и перестают поглощать глюкозу, лишая себя источника энергии) и даже при нормальном старении (когда просто нарушается метаболизм нейронов). Удержание нейронов на пределе их энергетического бюджета имеет свои последствия – и помощь нейронам в поддержании состояния на уровне этого предела перед лицом болезней и старения является новым и многообещающим подходом к лечению заболеваний головного мозга.
Жизнь на краю, на пределе энергетического бюджета, должна иметь следствия и для здоровых нейронов. Если бы более крупные нейроны потребляли больше энергии просто в силу необходимости поддержания поляризации своих больших мембран, но обладали бы столь же ограниченным энергетическим бюджетом, который относительно постоянен для всех представителей данного вида, то такие нейроны по необходимости обладали бы совершенно иным энергетическим бюджетом. Например, в них должны присутствовать механизмы, снижающие частоту разрядов и, таким образом, позволяющие избегать избыточной активности синапсов и снижать частоту, с которой приходится восстанавливать поляризацию мембраны после разряда. В самом деле, исследования показали, что крупные нейроны с большим числом синапсов образуют побочные связи, что позволяет уменьшать нагрузку на имеющиеся синапсы, частые разряды при этом направляются по обходным путям, уменьшая частоту разрядов данного нейрона, что было показано в культурах нейронов. Изменения кодирования сигналов, приводящие к уменьшению доли крупных нейронов, которые разряжаются с высокой частотой в любой момент времени, могут также быть следствием этого ограничивающего, размерно-инвариантного, фиксированного энергетического бюджета каждого данного нейрона.
Интересно подумать о том, что целый ряд фундаментальных свойств нейронов является прямым следствием ограничений нейронной активности, наложенных на нее ограниченным энергетическим бюджетом. Одно из таких свойств, «синаптический гомеостаз», которым описывают колебания чувствительности индивидуальных синапсов со временем в зависимости от уровня активности нейрона, позволяет избежать неконтролируемого повышения активности возбудительного синапса и избыточного расхода энергии. Другой механизм называют синаптической пластичностью. Это процесс удаления неиспользуемых или бесполезных синапсов на фоне добавления новых или усиления активности существующих. Это может стать необходимым механизмом, который поддерживает на достаточном уровне общее число возбудительных синапсов и контролирует расход ими драгоценной энергии. В течение жизни в мозге образуются новые синапсы, но непременно за счет отмирания уже существующих. В результате мозг в течение всей жизни остается способным к обучению.
Назад: Чем больше нейроны, тем больше отношение числа глиальных клеток к числу нейронов
Дальше: Так почему же человеческий мозг так дорог?

