Исследование № 35
Неандертальские гены влияют на наше здоровье
В заключительных главах мы обсудим исследования, проливающие свет на нашу собственную эволюцию, в том числе и на те эволюционные процессы, которые идут в человеческих популяциях прямо сейчас. Как известно сегодня каждому школьнику (хотя установлено это было лишь в 2009 году), генофонд современного внеафриканского человечества содержит примесь неандертальских генов, приобретенных в результате гибридизации 50-60 тысяч лет назад. О влиянии этих примесей на фенотип современных людей до сих пор известно немного. Появление больших баз данных по медицинской генетике позволило американским ученым в 2016 году оценить связь между наличием тех или иных неандертальских аллелей и различными заболеваниями. Оказалось, что неандертальские гены достоверно, хотя и слабо, влияют на риск развития некоторых заболеваний, таких как депрессия, актинический кератоз (патологическое изменение кожи под действием солнечного излучения), тромбоз и никотиновая зависимость. Многие из этих генов могли быть полезны нашим палеолитическим предкам, но потом стали вредными в связи с изменением условий жизни. Это еще раз демонстрирует, что вредность и полезность признаков (или мутаций) относительны и целиком и полностью зависят от контекста внешних условий и генетического окружения.


Благодаря поразительным успехам новой науки палеогенетики мы узнали, что между видами древних людей, населявшими разные области Старого Света в среднем и верхнем палеолите (сапиенсами, денисовцами, неандертальцами, гейдельбергскими людьми), неоднократно происходила межвидовая гибридизация. Наиболее убедительно обоснованы примерно семь эпизодов такой гибридизации (рис. 35.1).
Наверняка были и другие эпизоды гибридизации. Например, кроманьонец из румынской пещеры Оасе, живший 37-42 тысячи лет назад, имел предка-неандертальца в четвертом-шестом колене. Интересно, что в геномах поздних европейских неандертальцев не удалось обнаружить сапиенсных примесей. Получается, архаичные сапиенсы, денисовцы и неандертальцы гибридизовались довольно часто, но при этом, как мы знаем, все же не слились в один вид, а сохранили свою специфику вплоть до самого конца, то есть до вымирания неандертальцев (и, наверное, денисовцев). Есть основания полагать, что между тремя видами людей до того, как они начали встречаться и скрещиваться, успела сформироваться частичная генетическая несовместимость. Возможно, гибриды, особеннно гибриды мужского пола, имели пониженную плодовитость.
Самые важные последствия имел один из эпизодов гибридизации, произошедший в Западной Азии 50-60 тысяч лет назад между предками современного внеафриканского человечества, незадолго до этого покинувшими свою африканскую прародину, и местными неандертальцами. В результате в геномах всех современных сапиенсов, за исключением коренного населения Африки к югу от Сахары, присутствует небольшая неандертальская примесь.
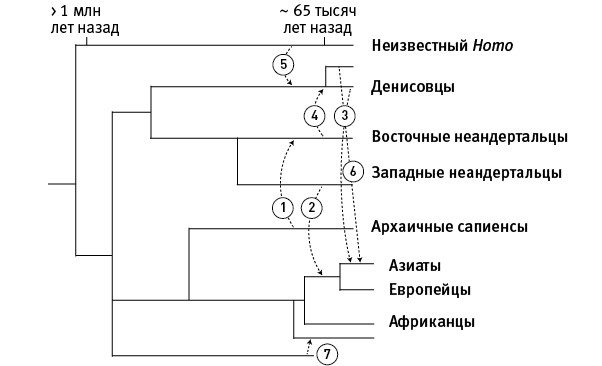
рис. 35.1. Семь эпизодов гибридизации сапиенсов, неандертальцев, денисовцев и неизвестных архаичных Homo согласно данным палеогенетики и сравнительной геномики. Стрелками показан приток генов:
1 – от архаичной популяции сапиенсов (скорее всего, ранних выходцев из Африки на Ближний Восток, не оставивших потомков среди современных людей) в геном восточных (алтайских) неандертальцев,
2 – от западных неандертальцев к предкам современного внеафриканского человечества (эпизод гибридизации, произошедший 50-60 тысяч лет назад, вскоре после начала “главной” волны миграции сапиенсов из Африки),
3, 6 – от двух разных популяций денисовцев к предкам папуасов, австралийцев и жителей Восточной Азии (причем в геномах китайцев и японцев сохранились следы скрещивания с обеими популяциями),
4 – от восточных неандертальцев к денисовцам (по последним данным, эпизодов гибридизации денисовцев с неандертальцами было как минимум два; одна особь женского пола, жившая в Денисовой пещере 90 тысяч лет назад, оказалась неандертальско-денисовским гибридом первого поколения),
5 – от неизвестных архаичных Homo (H. heidelbergensis или реликтовых поздних H. erectus) к денисовцам,
7 – от неведомой архаичной популяции, отделившейся от предков сапиенсов примерно полмиллиона лет назад, к предкам пигмеев и некоторых других африканских народностей.
Как повлияла эта примесь на дальнейшую судьбу внеафриканских сапиенсов? Помогали неандертальские гены нашим предкам в ходе их расселения по Старому Свету или, наоборот, мешали? На какие признаки современных людей влияют неандертальские аллели? Благодаря быстрому развитию палеогенетики и накоплению данных по генетическому разнообразию современных людей ответы на эти вопросы, поначалу крайне расплывчатые, становятся все четче и детальнее.
Выяснилось, что примерно за полмиллиона лет раздельного существования – от момента расхождения предков сапиенсов и неандертальцев до их гибридизации – эти две линии успели накопить достаточно генетических различий, чтобы между ними возникла частичная постзиготическая репродуктивная изоляция. Иными словами, в их генофондах закрепились взаимно несовместимые аллели, что привело к пониженной приспособленности гибридов. Это, между прочим, сильный довод в пользу того, что сапиенсов и неандертальцев правильнее считать разными видами, а не подвидами или разновидностями.
Неандертальские аллели, оказавшиеся вредными (снижающими приспособленность) в сапиенсном генетическом контексте, постепенно вычищались отбором. В результате неандертальская примесь в геномах европейцев сократилась от исходного уровня в 3 % до нынешних 2 % (примерно). У азиатов неандертальских генов осталось чуть больше (Sankararaman et al., 2014). Из некоторых участков генома отбор вычистил неандертальское наследие полностью. Очевидно, в этих участках неандертальские аллели были для наших предков абсолютно непригодными (резко снижали приспособленность). Один из таких участков включает знаменитый “ген речи” FOXP2. Белок-кодирующие последовательности этого крайне консервативного гена у сапиенсов, неандертальцев и денисовцев одинаковые (и при этом не такие, как у других приматов), а вот регуляторные – разные. Что из всего этого следует? Может, неандертальцы обладали речью, но то, как (или что) они говорили, было неприемлемо в обществе палеолитических сапиенсов?
Как бы то ни было, из того, что бóльшая часть неандертальских генов не пошла на пользу нашим предкам, вовсе не следует, что коренное неандертальское население Западной Евразии не могло передать выходцам из Африки и какие-то полезные гены. В конце концов, неандертальцы сотни тысячелетий жили в этом регионе, который и по климату, и по спектру доступных пищевых ресурсов, и по набору патогенных вирусов, бактерий и прочих паразитов сильно отличался от африканской родины сапиенсов. Поэтому было бы логично, если бы среди неандертальских генов, пошедших сапиенсам на пользу, нашлись гены, связанные с иммунной системой, строением кожи (ее пигментацией, чувствительностью к ультрафиолету и т. п.), а также с усвоением различных питательных веществ.
Эти ожидания в целом подтверждаются. Например, в 2016 году два исследования независимо друг от друга показали роль неандертальских аллелей в усилении врожденной иммунной защиты от патогенных бактерий, грибов и других паразитов (Dannemann et al., 2016; Deschamps et al., 2016). Любопытно, что даже в случае иммунитета, когда речь идет, казалось бы, о признаках безусловно полезных, они могут оказаться вредными для современного человека. Усиленный врожденный иммунитет мог быть спасительным для дикарей, недавно вышедших из Африки и начавших расселяться по неведомым территориям, но у современного горожанина, контактирующего с меньшим разнообразием паразитов, основным фенотипическим проявлением той же самой врожденной особенности стал повышенный риск аутоиммунных заболеваний и аллергий. То же касается и других признаков, полезных нашим предкам, но ставших вредными сегодня. Например, аллели, повышающие эффективность усвоения питательных веществ или усиливающие пищевую мотивацию, были крайне полезны пращурам, жившим в условиях постоянной угрозы голода, но в современном цивилизованном обществе эти же самые аллели стали “генами ожирения”.
В том же 2016 году американские биологи провели крупномасштабный поиск неандертальских аллелей, влияющих на здоровье современных европейцев (Simonti et al., 2016). Эта работа стала возможной, с одной стороны, благодаря высококачественному прочтению неандертальских геномов (что позволило выявить в геномах современных людей тысячи конкретных генетических вариантов, унаследованных от неандертальцев). С другой стороны, к настоящему времени уже подсобрались большие базы данных по медицинской генетике, в которых к сведениям о генотипе привязаны сведения о различных болезнях.
Ученые использовали данные, которые были собраны в рамках проекта eMERGE (electronic MEdical Records and GEnomics), запущенного в 2007 году Национальными институтами здравоохранения США. Из этой базы данных были взяты сведения о генотипах 28 416 взрослых американцев европейского происхождения. Для каждого из них в базе имеется электронная медицинская карта, то есть информация о наличии или отсутствии различных заболеваний и прочих “медицинских характеристик”, таких, например, как вредные привычки. Для всех этих людей известно аллельное состояние большинства полиморфных локусов (то есть участков генома, которые не у всех людей одинаковы), что, по сути, почти идентично наличию целых прочтенных геномов.
Данные электронных медицинских карт были сопоставлены с наличием или отсутствием у людей аллелей неандертальского происхождения. Чтобы получить статистически достоверные результаты, ученые рассматривали только те фенотипы (“медицинские признаки”) и те неандертальские аллели, которые встречаются в изученной выборке достаточно часто.
Для начала проанализировали связь 1495 часто встречающихся (с частотой > 1 %) неандертальских однонуклеотидных полиморфизмов с риском развития 46 распространенных патологий. Для этого смотрели, насколько сходство между людьми по набору неандертальских аллелей коррелирует со сходством по наличию или отсутствию этих патологий. Такой подход позволяет оценить комплексное влияние множества аллелей на мультигенные признаки. Выяснилось, что неандертальские аллели действительно влияют на ряд медицинских характеристик. Наиболее значимые результаты получились по депрессии, другим аффективным расстройствам, а также актиническому кератозу. С несколько меньшей достоверностью неандертальские гены влияют на риск других кератозов, мозолей, ожирения, атеросклероза, инфаркта миокарда. Все эти эффекты слабые: для депрессии, иных аффективных расстройств и актинического кератоза неандертальские аллели обуславливают 1-2 % изменчивости по риску, для остальных расстройств – менее 1 %. Среди неандертальских аллелей, связанных с перечисленными недугами, одни повышают вероятность развития патологии, другие снижают, причем число тех и других примерно одинаково. Если речь идет об одном проценте, то мы вправе задать вопрос: изменение вероятности заработать депрессию на один процент – это много или мало? С точки зрения медицинской статистики и реального риска заполучить то или иное заболевание это совсем немного. Но нас здесь интересует не столько медицинский аспект, сколько эволюционный. Для нас важно, что корреляции оказались значимыми, то есть по соответствующим неандертальским аллелям вполне может идти отбор – если только данная медицинская характеристика хоть немного влияет на количество и “качество” оставляемых потомков.
Интересно, что несколько неандертальских вариантов, повышающих вероятность депрессии, расположены в окрестностях генов, связанных с регуляцией циркадных (суточных) ритмов. В этом есть логика: известно, что на риск депрессии влияет режим освещенности, а сапиенсы и неандертальцы жили на разных широтах. Поэтому их биологические часы должны были быть настроены по-разному.
Разумеется, это не значит, что неандертальцы страдали от жестоких депрессий, а мы унаследовали от них это свойство. Скорее это означает, что заимствованные у неандертальцев аллели, влияющие на адаптацию к смене дня и ночи, сначала были полезны сапиенсам, переселявшимся из своей тропической прародины в более высокие широты, но потом, с развитием цивилизации и искусственного освещения, что-то из неандертальского наследия могло потерять полезные свойства и стать, наоборот, вредным.
Важно понимать, что поскольку изучались только те неандертальские аллели, которые встречаются у современных европейцев достаточно часто, то в выборку не могли попасть аллели, которые с самого начала были очень вредны нашим предкам. Такие аллели либо давно вычищены отбором, либо сохранились как редкие варианты и потому остались за рамками исследования.
Вот еще четыре примера неандертальских полиморфизмов, влияющих на здоровье современных европейцев.
Полиморфизм rs3917862 встречается у европейцев с частотой 6,5 %. Столь высокая частота указывает на то, что данный генетический вариант поддерживался отбором у наших предков. Этот полиморфизм маркирует неандертальский участок ДНК, который включает несколько генов, участвующих в свертывании крови. Его наличие коррелирует с повышенной свертываемостью. По-видимому, это было полезно в каменном веке, когда не было других способов остановить кровотечение после ранения или родов, а до старости все равно мало кто доживал. Для современного горожанина, однако, это вредный признак.
Полиморфизм rs12049593 встречается у европейцев с частотой 5 % (а значит, тоже был полезен предкам) и приурочен к гену, отвечающему за транспорт тиамина (витамина B1). Наличие у людей этого неандертальского варианта коррелирует с симптомами белково-энергетической недостаточности. Тиамин – обязательный участник метаболизма углеводов, а неандертальский аллель, по-видимому, снижает его поступление в клетки. Возможно, это выгодно, если в пище мало углеводов и много тиамина. Не исключено, что сапиенсам пригодился неандертальский ген, когда они расселялись по Европе, где им приходилось питаться совсем другой пищей, чем в Африке, и нужно было подстроить обмен веществ под новую, низкоуглеводную диету (попутно заметим, что сапиенсам, по-видимому, пригодились и многие неандертальские аллели, связанные с метаболизмом липидов). Но с развитием земледелия количество тиамина в пище снизилось, а доля простых углеводов возросла. Теоретически это могло привести к тому, что полезный в прошлом неандертальский ген стал вредным.
Полиморфизм rs11030043 встречается у европейцев с частотой 9 % (то есть однозначно был полезен). Соответствующий аллель – это неандертальский вариант гена STIM1, участвующего во внутриклеточной передаче сигналов при помощи ионов кальция. У людей с этим неандертальским геном понижена экспрессия STIM1 в хвостатом ядре – отделе мозга, отвечающем, помимо прочего, за работу мочевого пузыря. Наличие данного аллеля немного повышает риск недержания мочи и других нарушений работы мочевыводящих путей. Исследователи воздержались от предположений, зачем это могло быть нужно палеолитическим сапиенсам. Но какая-то польза должна была быть, иначе ген не достиг бы столь высокой частоты в европейском генофонде. Возможно, эта польза была связана с другими функциями хвостатого ядра – например, с теми, что имеют отношение к мотивации наших поступков.
Полиморфизм rs901033 встречается у европейцев с частотой 0,5 % (следовательно, мог быть вреден уже с давних пор). Соответствующий неандертальский ген повышает риск никотиновой зависимости. Этот полиморфизм расположен в интроне гена SLC6A11, отвечающего за обратный транспорт тормозного нейромедиатора ГАМК (гамма-аминомасляной кислоты) в синапсах мозга. Тут можно усмотреть некую логику, если учесть, что никотиновая зависимость нарушает передачу сигналов при помощи ГАМК и снижает экспрессию SLC6A11. Вряд ли нужно пояснять, что неандертальцы, как и кроманьонцы, не курили табак. Хотя сидеть в пещере у дымного костра тоже не очень-то хорошо для легких.
Так или иначе, исследование показало, что примесь неандертальских генов заметно влияет на здоровье современных европейцев.
Ученые сосредоточились на медицинских показателях не потому, что все прочие их не интересовали, а потому, что по другим признакам пока собрано слишком мало генетических данных для такого анализа. Дальнейшее развитие науки должно дать ответ на вопрос, какую роль играет неандертальское наследие в вариабельности внеафриканских сапиенсов по всем прочим интересным признакам, не только медицинским.

