Внутрь атома
Так как же обстояли дела в начале прошлого века? Томсон предположил, что электроны представляют собой части внутреннего строения атомов. Но, так как они обладали отрицательным зарядом, а атомы были нейтральны, это подразумевало, что атомы также должны содержать положительный заряд, который бы нейтрализовал заряд электронов. В результате Томсон предложил первую экспериментальную модель атома, в которой электроны были равномерно распределены по сфере положительно заряженного атомного «вещества». Размеры сферы можно было примерно рассчитать на основании известных в то время величин. Эта модель получила название «пудинговой» модели атома, так как электроны в ней напоминали изюм в пудинге. В то же время Беккерель и супруги Кюри пришли к выводу, что определенные типы атомов излучают радиацию. Таким образом, пока одни физики и химики даже не верили в существование атомов, другие уже имели некоторое представление, из чего они состоят.
Родившемуся в Новой Зеландии Эрнесту Резерфорду было суждено стать одним из самых влиятельных ученых XX века. Он приехал в Кембридж, чтобы работать с Томсоном, и вскоре заинтересовался новым вопросом радиоактивности. Он открыл, что существует три типа радиоактивности. Первый, который он назвал бета-лучами, как оказалось, составляли электроны Томсона. Второй, названный альфа-лучами, состоял из гораздо более тяжелых, положительно заряженных частиц, которые, как впоследствии продемонстрировал Резерфорд, оказались ионами гелия (атомами гелия без электронов). Он также показал, что третий, электрически нейтральный тип радиоактивности, открытый в 1900 году Полем Вилларом, представлял собой лишь форму электромагнитных лучей, подобных рентгеновским лучам, которые он назвал гамма-лучами. Сегодня мы, конечно, называем типы альфа и бета частицами, а не лучами.
В течение первого десятилетия двадцатого века Резерфорд сумел доказать, что возраст земной коры составляет миллиарды лет. Он сделал это, измерив содержание гелия в образцах скальных пород, заключенная в которых урановая руда медленно испускала альфа-частицы с момента формирования скал. Каждая альфа-частица оказывалась в ловушке внутри камня и быстро приобретала пару электронов, чтобы стать атомом гелия. Сторонники теории креационизма до сих пор ничего не смогли противопоставить этому обнаруженному столетие назад простому и в то же время неопровержимому доказательству, что нашей планете больше миллиарда лет.
Через несколько лет Резерфорд стал первым ученым, исполнившим мечту алхимиков о трансмутации, когда провел эксперимент, в котором преобразовал один элемент в другой. Это не стало неожиданностью, так как к тому моменту Резерфорд совместно с Фредериком Содди пришел к выводу, что радиоактивный распад представляет собой естественную форму трансмутации.
Открыв альфа-частицы, Резерфорд быстро понял, что они дают необходимый инструментарий для изучения атомной структуры. В 1911 году два его ассистента, Ханс Гейгер и Эрнест Марсден, провели серию трудоемких экспериментов, в которых пучок альфа-частиц, испускаемый радиоактивным источником направлялся на очень тонкую золотую фольгу. При столкновении с фоточувствительным экраном рассеивающиеся частицы обнаруживались благодаря крошечным вспышкам света. Несмотря на то что изначально толщина фольги составляла несколько тысяч атомов, большинство альфа-частиц проходило сквозь нее, практически не отклоняясь от своего курса. В связи с этим был сделан вывод, что атомы явно должны в основном состоять из пустоты. Более удивительным было то, что в среднем одна из восьми тысяч альфа-частиц отражалась от фольги. Если представлять атомы в соответствии с пудинговой моделью Томсона, это просто невозможно.
Резерфорд понял важность этого результата и предложил гораздо более удачную модель строения атома. Во-первых, он знал, что электроны в несколько тысяч раз легче альфа-частиц, а следовательно, не могут сбивать их с пути. Было похоже, что положительно заряженные альфа-частицы отклонялись электрическим сопротивлением положительного заряда внутри атома. Единственным способом объяснить наблюдаемое было предположить, что весь положительный заряд сконцентрирован в очень маленьком объеме для максимизации эффекта. Большинство альфа-частиц проходит мимо него, но некоторые оказываются достаточно близко, чтобы почувствовать всю силу положительного заряда атомов золота и отталкиваются от них.
Резерфорд назвал это крошечное скопление положительного заряда «ядром» атома и предложил новую модель атома. Она практически полностью состояла из пустого пространства, в центре которого находилось крошечное, положительно заряженное ядро, содержащее в себе почти всю атомную массу, а вокруг него по орбитам вращались еще более мелкие электроны.
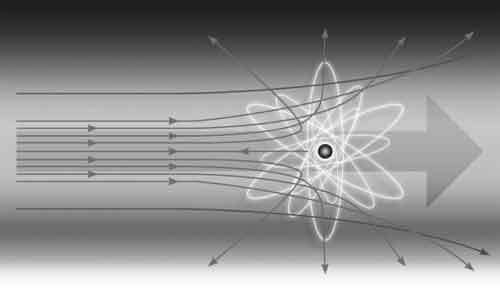
В соответствии с теорией Резерфорда, чем ближе альфа-частица оказывается к лобовому столкновению с крошечным атомным ядром, тем больше угол отклонения. Результаты экспериментов Гейгера и Марсдена прекрасно подтвердили эту картину.
Именно в этот момент – в 1912 году – работать с Резерфордом начал молодой Нильс Бор, который первым применил квантовую теорию Планка к планетарной модели, чтобы объяснить ее стабильность (я описывал это в Главе 2). Но не забывайте, что до появления полноценной квантовой механики оставалось еще целое десятилетие. В модели Бора электроны по-прежнему считались крошечными «классическими» частицами, вращающимися вокруг ядра по фиксированным орбитам. Случившиеся в 1920-х годах открытия ученых вроде Гейзенберга и Шрёдингера показали, что такая картина атома не только наивна, но и во многом неверна. Они продемонстрировали, что квантовые законы, которым, по мнению Бора, должны были подчиняться электроны, вернее было связывать с волновыми функциями электронов. Путем решения уравнения Шрёдингера физики могли объяснить, как электроны располагаются в атоме. Только задним умом стало понятно, что выведенная для конкретного случая формула Бора на самом деле возникает из полной квантовой механики. Различие теперь заключалось в том, что отдельные электроны уже нельзя было считать локализованными частицами, вращающимися по орбите вокруг ядра; их стоило описывать с помощью волновой функции, содержащей в себе некоторые ярлыки, называемые квантовыми числами, которые определяют энергию электрона и траекторию его движения вокруг атома. Волновые функции электронов занимают весь объем атома и дают нам вероятностное распределение, которое показывает, где можно с высокой вероятностью обнаружить электрон, если мы «посмотрим туда». Возможно, вам встречались фразы «электронное облако» или «вероятностная плотность» электрона. Они просто означают трехмерный рисунок вероятности, который со временем не меняется, если только электрон не переходит из одного квантового состояния в другое (что равносильно старому представлению о «перепрыгивании» электрона с одной фиксированной орбиты на другую) при потере или получении кванта энергии или момента импульса. Любое такое изменение приведет к изменению волновой функции электрона и формы соответствующего вероятностного распределения.

Вероятностные облака электронов в разрезе.
Слева: В атоме водорода единственный электрон находится в низшем энергетическом состоянии и с наибольшей вероятностью может быть обнаружен рядом с центром атома.
В центре: При возбуждении электрона в атоме водорода и его переходе на следующий энергетический уровень его облако внезапно изменяется. Теперь он с малой вероятностью может быть обнаружен рядом с центром атома, но с большей вероятностью может оказаться в пределах сферической оболочки на некотором расстоянии от центра. Вероятность обнаружить электрон в пространстве между центром и этой оболочкой равняется нулю.
Справа: Атом углерода содержит шесть электронов. Четыре из них не имеют момента импульса, и распределения их вероятностей симметричны. Два других обладают небольшим моментом импульса, а это означает, что вероятностное распределение каждого может находиться в одной из трех возможных ориентаций – на рисунке показана одна.

Электронные облака различных атомов (сверху вниз в порядке увеличения числа электронов: водород, кремний, железо и серебро). Когда заполняется каждая из орбиталей, следующим электронам приходится занимать более высокоэнергетические орбитали.
Таким образом, точно так же, как нам приходится утверждать, что атом проходит сквозь обе прорези одновременно, мы должны считать каждый электрон распространенным на весь объем атома. Это единственная приемлемая картина атома, которую нам позволяет иметь квантовая механика. Области, где каждый из электронов предпочитает проводить время, зависят от формы волновой функции конкретного электрона, которая, в свою очередь, задается квантовыми числами этого электрона. Все это связано со сложной математикой и не поддается интуитивному пониманию, в связи с чем гораздо проще придерживаться планетарной модели атома Резерфорда/Бора. Пускай она и неверна, но так мы хотя бы можем представить себе строение атома. Однако вся современная химия и значительная часть физики покоится на этой квантовой структуре атомов. Квантовые числа электронов определяют, как они распределяются по так называемым «квантовым орбиталям» (которые напоминают нечеткие, неправильной формы орбиты) или «энергетическим уровням», а это прекрасно объясняет, как именно происходит классификация элементов в соответствии с их химическими свойствами и их расстановка в таблице Менделеева.
Квантовая механика предсказывает гораздо больше, чем просто распределение электронов внутри атома. Она также делает предсказания о перемещении электронов между энергетическими уровнями. Это происходит, к примеру, когда атомы взаимодействуют со светом. Электроны могут поглощать фотоны, при условии что энергия фотонов соответствует энергетическим интервалам между различными уровнями. Если это происходит, фотон перестает существовать, так как он полностью поглощается в качестве чистой энергии для «возбуждения» электрона для перехода на более высокий энергетический уровень. Электрону, как правило, некомфортно обладать этой дополнительной энергией, и он вскоре испускает фотон ровно той энергии, которую необходимо отдать, чтобы перейти обратно на исходный уровень. Квантовая механика предсказывает частоту и интенсивность этого света, который вновь испускается возбужденными электронами атомов. Каждый тип атома обладает уникальной схемой уровней приемлемых энергий электронов, и рисунок света, отдаваемого атомами, когда их электроны опускаются на более низкие энергетические уровни, называется линейчатым спектром. Именно так астрономы понимают, какие элементы существуют в звездах и далеких галактиках, изучая лишь природу видимого света. Сегодня «спектроскопия» находит применение во многих областях.
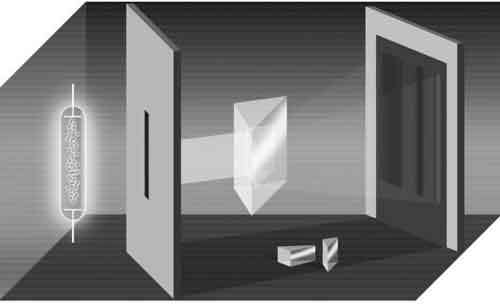
При прохождении электрического тока сквозь водородный газ внутри нагнетательной трубки газ нагревается и излучает свет. Затем этот свет разделяется на составные цвета при помощи призмы. Однако, в отличие от солнечного света, дающего мягкий радужный спектр, в котором цвета переходят друг в друга, мы видим серию отдельных цветных полосок (называемую линейчатым спектром): красную, голубую и много полосок в фиолетовой области, которые становятся все ближе друг к другу, пока не затухают за пределами видимого спектра.
Назад: Таинственные лучи повсюду
Дальше: Квантовый спин

