Книга: ДНК. История генетической революции
Назад: Глава 7 Геном человека. Сценарий жизни
Дальше: Глава 9 Изучение геномов. Эволюция в действии
Глава 8
Время первых
Как-то раз в конце 2005 года мне неожиданно позвонил предприниматель-биотехнолог по имени Джонатан Ротберг. Хотя мы с ним никогда лично не встречались, я кое-что знал о его достижениях. В начале 1990-х годов Ротберг основал в Коннектикуте биотехнологическую компанию. От Колд-Спринг-Харбора до Коннектикута было недалеко, достаточно переправиться на пароме через пролив Лонг-Айленд. Эта коммерческая организация под названием Curagen, как и многие другие биотехнологические предприятия того времени, пережила взрывной приток капитала и некоторое время оценивалась на рынке необоснованно высоко, пока не ушла в глубокое пике во время общего обвала рыночных котировок. Однако к 2005 году Ротберг основал уже новую компанию под названием 454 Life Sciences. Сначала я понятия не имел, что означали цифры 454, но потом стало понятно, что Ротберг занялся конструированием нового секвенатора ДНК. Как я потом понял, ему это удалось, поскольку в августе 2005 года я прочел в Nature статью, соавтором которой был Ротберг. В статье был описан новый секвенатор «454» – первый из так называемых секвенаторов нового поколения.
Позже я узнал, откуда взялось число 454. В 1999 году жена Ротберга родила недоношенного ребенка, сразу помещенного в инкубатор для новорожденных. Ротберг места себе не находил и в ожидании новостей брал в руки то одну вещь, то другую. Наконец он вытащил из брифкейса компьютерный журнал, на обложке которого красовался новейший высокомощный микропроцессор. Тогда его озарило: что будет, если применить в новой системе для секвенирования ДНК (которая могла бы прийти на смену системе Сенгера) два достижения компьютерной революции: миниатюризацию и распараллеливание. Он воображал, что когда-нибудь такая система помогла бы уменьшить беспокойство родителей и могла бы решить проблему ранней диагностики болезней у новорожденных.
Пару месяцев спустя Ротберг посетил меня в Колд-Спринг-Харборе.
Я увидел высокого, слегка растрепанного человека с копной непослушных темных вьющихся волос – примерно таков был и я в юности. Он обратился ко мне с совершенно необычным предложением, спросив, не хочу ли я послужить геномике в качестве подопытной морской свинки и стать первым в мире человеком, чья ДНК будет полностью расшифрована? Недолго думая, я согласился: не то чтобы я очень хотел быть первым в этом деле и тем более не горел желанием заглянуть в собственный геном; однако, думал я, такой проект мог бы очень пригодиться в просветительских целях.
Я согласился, чтобы мой геном отсеквенировали и выложили результаты в общий доступ, но поставил всего одно условие. Я хотел как можно больше узнать об одном гене из 19-й хромосомы, который называется APOE (аполипопротеин E). Нейрогенетик из Университета Дьюка по имени Аллен Розес (скоропостижно скончавшийся в 2016 году в Международном аэропорту им. Джона Кеннеди по дороге на конференцию) убедительно продемонстрировал, что редкая разновидность (аллель) этого гена под названием APOE4 повышает риск возникновения болезни Альцгеймера, особенно если человек унаследовал сразу две аллельные комбинации E4. Одна моя тетушка страдала болезнью Альцгеймера, и я, конечно, не хотел бы переживать по поводу моей предрасположенности к этому тяжелому заболеванию.
Примерно в течение года после визита Ротберга я ничего не слышал об этом проекте, но в конце 2006 года люди Ротберга вновь связались со мной, и мы договорились, что я сдам кровь для исследования. Технологии компании Ротберга серьезно усовершенствовались, а стоимость секвенирования тем временем значительно снизилась. Теперь у команды Ротберга был образец ДНК, нужный для запуска проекта, названного «Джим». В мае 2007 года я полетел в Хьюстон в качестве почетного гостя на презентацию своего генома. Хотя собственно секвенированием занимались 454 ученых, этот процесс был относительно тривиален по сравнению с требующей титанических усилий задачей, с которой столкнулись специалисты по биоинформатике и генетики, пытавшиеся осмыслить полученную информацию о миллионах оснований. Эту задачу Ротберг решал совместно с группой специалистов из Бэйлорского медицинского колледжа, во главе которой стояли генетики Ричард Гиббс и Джим Лапски, специалист по биоэтике Эми Макгуайр и биоинформатик Дэвид Уилер. На церемонии Ротберг вручил мне внешний диск для компьютера, где был записан весь мой генетический код. Хочу, чтобы читатели оценили масштаб исследования. Обратите внимание: когда мы говорим, что геном секвенирован, мы имеем в виду не «однократно секвенирован», а проанализирован как минимум 30 раз, только таким количеством исследований можно обеспечить относительно точное описание генома, дающее более-менее реальную информацию. В условиях клинического исследования необходимость повторов должна быть еще выше – примерно 45 раз. Кто-то из присутствующих поспешно обвязал этот диск тоненькой красной ленточкой, чтобы он выглядел как подарок. Мне грех было жаловаться: Ротберг оценил стоимость секвенирования моего генома примерно в один миллион долларов.

Первый из многих: в мае 2007 года основатель компании 454 Джонатан Ротберг вручает мне внешний жесткий диск, на котором записана вся информация о моем отсеквенированном геноме
На самом деле я был, мягко говоря, разочарован тем, что нашлось в моей ДНК, – вернее, тем, чего там не нашлось. Накануне за ужином группа Бейлора заранее показала мне самые интересные детали моего генома. Например, в моей ДНК оказался редкий вариант гена, кодирующего важный фермент под названием цитохром P450, – в этом заключалась причина того, что я плохо метаболизирую некоторые препараты, в частности тот, что мне прописывают от повышенного давления. Я действительно замечал, что из-за этих таблеток меня клонит в сон. Вооружившись такой генетической информацией, я решил снизить дозу и поступаю так по сей день. Это была побудительная к действию информация. В то же время я, конечно, обеспокоился, узнав, что у меня нашлись какие-то подозрительные аллели гена BRCA1, отвечающего за рак желудка, – это был серьезный повод для беспокойства о здоровье моих племянниц, также имеющих такие же маркеры. Однако впоследствии я узнал от Мэри-Клэр Кинг (той самой, которая в 1990 году картировала ген BRCA1 – об этом мы поговорим в главе 14 – и изучала функцию этого гена на сотняхсемей, члены которых страдали раком груди), что аллели в моей генетической последовательности – это всего лишь «безобидные ирландские полиморфизмы».
Линкольн Стейн, мой бывший коллега по Колд-Спринг-Харбору, создал сайт, на котором выложил всю последовательность моего генома – кроме вышеупомянутого гена APOE. Однако мы упустили одну вещь: поскольку передача наследственной информации происходит с помощью генов случайным образом (здесь можно провести аналогию с тасуемой колодой карт), любой генетик, пусть даже со средним уровнем подготовки, теоретически может определить, какие именно у меня имеются варианты гена APOE. Для этого ему достаточно просмотреть генотипы соседствующих с ним генов в 19-й хромосоме. Об этом и заявил во всеуслышание один молодой ученый, администратор сайта по имени Майкл Карьясо, занимающийся анализом и хранением информации обо всех фрагментах ДНК, ценных с медицинской точки зрения. Сайт, который он администрировал, называется SNPedia. Линкольн Стейн оперативно отреагировал, потребовав удалить информацию примерно о тридцати моих генах, то есть примерно о миллионе оснований по обе стороны от гена APOE, и принести мне извинения по поводу доставленных неудобств, связанных с разглашением информации. В 2007 году лишь один человек, кроме меня, полностью отсеквенировал свой геном. Неудивительно, что это был Крейг Вентер – ведь именно он десятью годами ранее инициировал такое исследование в Celera Genomics, когда реализация проекта «Геном человека» была в самом зените. Коллеги Вентера просекли, к чему ведет проект «Джим», и опубликовали свои результаты примерно за полгода до того, как статья с окончательным описанием моего генома наконец появилась в журнале Nature. Однако ключевое отличие состояло в том, что геном Вентера секвенировали традиционным сенгеровским методом, а мой – при помощи технологии «454», то есть с использованием секвенатора нового поколения. Поэтому ряду ученых секвенирование именно моего, довольно заурядного генома кажется фактом более важным. Френсис Коллинз назвал меня «первым из всех нас». Думаю, он был прав: после краткого затишья, вслед за которым, буквально выдавливая «по капле», секвенировали лишь единичные геномы, работа по секвенированию превратилась в настоящий шквал. Полагаю, что к моменту написания этих строк полностью отсеквенировано уже около 400 тысяч человеческих геномов, а стоимость секвенирования снижается и уверенно движется к отметке 1000 долларов, хотя сумма в 1000 долларов тогда казалась нереальной, в каком-то смысле «взятой с потолка». Последствия такой революции в персональной геномике – для науки, медицины и общества в целом – и будут рассмотрены в данной главе.

Пробел в геноме: последовательность моего генома выложена в интернете в свободном доступе; исключение составляет небольшой фрагмент 19-й хромосомы. Фрагмент охватывает окрестности гена APOE, связанного с болезнью Альцгеймера
В декабре 2001 года, примерно через девять месяцев после публикации первых черновых вариантов человеческого генома, фельдмаршал этого проекта Френсис Коллинз пригласил около сотни ведущих ученых на встречу в пасторальной Виргинии. Предполагалось, что они смогут честно и прямо обсудить перспективы будущих исследований и определить приоритеты новой эпохи в генетике, которую уже стали называть постгеномной. Один из важнейших вопросов, который им требовалось решить, – устаревание технологии для секвенирования ДНК. Метод с применением дидезокси-оснований, за который Фред Сенгер был удостоен Нобелевской премии (см. главу 4), превосходно послужил биохимическому сообществу, но отдача от него была крайне низкой, вернее сказать, медленной. Если технологии Сегнера использовать и далее, то Коллинзу и Вентеру понадобились бы целые фабрики по секвенированию, состоящие из сотен новейших машин-секвенаторов, каждая стоимостью сотни тысяч долларов, которые должны были бы обслуживать толпы лаборантов в белых халатах, работающих посменно круглые сутки. И все это для того, чтобы только сделать первые наброски нашего генетического кода. Дальнейший прогресс в геномике, а фактически в большинстве сфер биомедицинских и клинических исследований, застопорился до тех пор, пока специалисты не смогут ускорить, удешевить и оптимизировать секвенирование ДНК.
Во время дискуссий, развернувшихся в виргинской глуши, впервые речь зашла о «геноме за тысячу долларов». Вспомним время начала работы над проектом «Геном человека». Тогда, в начале пути, Уолли Гилберт написал мелом на доске в аудитории Колд-Спринг-Харбора: «3 миллиарда» – на этот раз ведущие специалисты по геномике вновь решились назвать столь же отвлеченную цифру: «1000 долларов». В такой величине не было никакого особого смысла или «магии» – просто небольшое красивое круглое число. Тем не менее, если бы его действительно удалось достичь, и стоимость секвенирования генома конкретного человека приблизилась бы к этой цифре, возможно, секвенирование человеческого генома стало бы рутинной процедурой.
Неудивительно, что различные академические и коммерческие группы ученых по обе стороны Атлантики, в том числе сотрудники Ротберга из компании 454, активно включились в разработку альтернативных методов секвенирования, на порядок дешевле и быстрее сенгеровского. В следующем году Вентер заявил на одной из конференций, что лично выплатит премию в 500 тысяч долларов той группе, которая достигнет наиболее значительного технологического прорыва в этой области. Одним из первых претендентов на премию стала компания U. S. Genomics – детище бывшего студента-медика из Гарварда по имени Юджин Чан. Он предлагал новый вариант секвенирования. Суть технологии заключалась в том, что молекула ДНК или РНК, несущая на себе существенный отрицательный заряд, под воздействием электрического поля «протискивается» через белковую пору, помещенную в бислойную мембрану, что вызывает уменьшение силы электрического тока из-за уменьшения сечения отверстия. Считывая изменение силы тока, секвенатор определяет нуклеотид, проходящий через пору в конкретный отрезок времени: оказывается, что каждый «кирпичик» в нуклеиновой кислоте имеет собственное «сечение» (и, соответственно, это влияет на силу тока). Увы, как и многие другие претенденты, компания Чана столкнулась с серией препятствий и вышла из гонки за лидерство. Таким образом, инициативу захватили компания Ротберга 454 и британская компания Solexa.
Биотехнологическую фирму Solexa основали двое молодых ученых-химиков из Кембриджского университета – Шанкар Баласубраманьян и Дэвид Кленерман. Изначально в их планы не входило преобразование медицины или секвенирование 100 тысяч человеческих геномов – они просто хотели изучить процесс биосинтеза ДНК. Планы по созданию их стартапа зародились в одном из пабов, но не в «Игл», где мы с Френсисом отмечали открытие двойной спирали, а в Panton Arms, поскольку химики из Кембриджа предпочитают именно это питейное заведение. В Solexa разработали ряд интересных методов для работы с основаниями. Эти методы позволяли синтезировать молекулы ДНК в медленном темпе – так, чтобы молекула наращивалась всего на одно и строго на одно основание за один шаг. Размечая основания флуоресцентными красителями (каждое из четырех оснований своим цветом), специалисты Solexa смогли зафиксировать каждый этап реакции и логически определить, какое основание добавляется в каждую точку ДНК, просто по цвету. Таким образом, растущие спирали можно было анализировать, как при покадровом просмотре видео. Лишь гораздо позднее компания доработала свою технологию для применения в медицине.
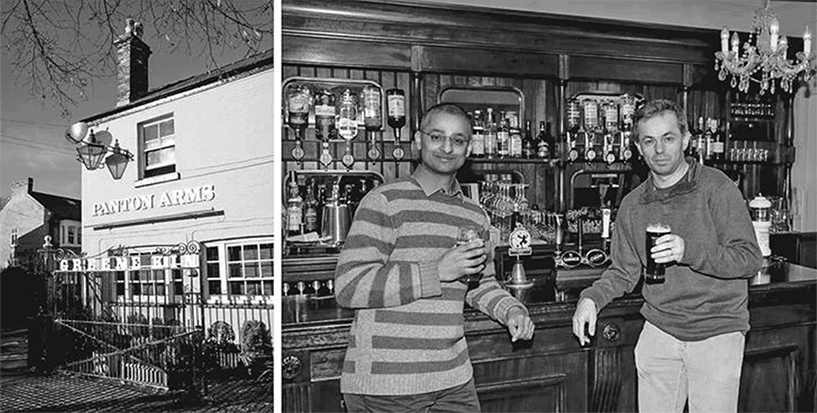
Шанкар Баласубраманьян и Дэвид Кленерман из Кембриджского университета выпивают праздничную пинту в пабе Panton Arms, где они сформулировали принципы работы системы секвенирования нового поколения, применяемой в компании Solexa
При всей своей красоте этот метод с технологической точки зрения тоже был далеко не идеален. В частности, на первом этапе за каждый шаг удавалось считывать совсем мелкие фрагменты, всего по несколько десятков оснований каждый. Поэтому выстроить полную картину какого-либо генома было очень сложно. Тем не менее Solexa не сдавалась, и однажды воскресным вечером в феврале 2005 года Клайв Браун отправил старшим коллегам электронное письмо, тема которого была: «МЫ СДЕЛАЛИ ЭТО!!!» Им удалось успешно секвенировать свой первый геном – речь о геноме крошечного вируса ФХ174, секвенированием которого прославился в 1977 году и Фред Сенгер. Пусть это и был в буквальном смысле самый маленький геном на нашей планете, причем уже известный, это достижение стало ключевой вехой не только для компании Solexa, но и для всей новой эпохи секвенирования. Однако Браун с коллегами, в том числе новый гендиректор компании Джон Уэст, не поддались соблазну сразу открывать шампанское и публиковать статью с самопиаром в каком-нибудь престижном журнале. Они хранили молчание, оставляя Ротбергу и прочим по ту сторону океана догадываться, насколько они продвинулись в работе.
После принятого в 1999 году спонтанного решения основать компанию 454 Ротберг рассмотрел несколько стратегий развития и наконец остановился на новой методике под названием пиросеквенирование, ранее разработанной шведскими исследователями. Идея пиросеквенирования заключается в регистрации пирофосфата, который образуется при присоединении очередного нуклеотида ДНК-полимеразой. Детекция пирофосфата осуществляется за счет каскада химических реакций, который заканчивается выделением кванта света. Для реализации метода создается иммобилизованная на твердой фазе клональная библиотека одноцепочечных фрагментов ДНК. Ко всем фрагментам ДНК присоединяется адаптер, с которым будет комплементарно связываться праймер – затравка для синтеза комплементарной цепи ДНК-полимеразой. Далее производится серия последовательных циклов, в процессе которых к закрепленной на твердой фазе ДНК по очереди добавляют дезоксинуклеотидтрифосфаты всех четырех типов: A, T, Г, Ц. Если на секвенируемой цепи ДНК есть комплементарный к добавленному нуклеотиду, то при образовании фосфодиэфирной связи побочным продуктом станет пирофосфат. Он активирует каскад химических реакций: пирофосфат вместе с адено-зинсульфофосфатом (АСФ) при помощи фермента АТФ-сульфурилазы образуют АТФ, который является источником энергии для проведения реакции окисления фермента люциферина (фермент, обеспечивающий биолюминесценцию у светлячков) в оксилюциферин с выделением кванта света. Интенсивность выделяемого света пропорциональна числу включенных в цепь нуклеотидов (чем больше подряд одинаковых нуклеотидов, тем сильнее световой сигнал). Команда Ротберга состояла из талантливых ученых и программистов; один из инженеров даже участвовал в разработке телескопа «Хаббл». Успешная стратегия компании способствовала ее переходу на коммерческие рельсы.
Летом 2005 года компания 454 опубликовала статью (я прочел ее в журнале Nature), в которой был описан не только ее прибор GS20, но и методика секвенирования бактериального генома. В следующем году при помощи секвенатора GS20 учеными было успешно реализовано несколько проектов, упоминания о которых неизменно становились «научным хитом». Так, по кусочкам секвенировали геном неандертальца, идентифицировали вирус, из-за которого таинственно исчезали медоносные пчелы, и (это буквально сюжет для сериала «CSI: Место преступления») обнаружили редкий вирус, из-за которого умер европейский студент, пешком путешествовавший по Австралии. Наступила новая эра секвенирования. Технология крепла, Ротберг решил взяться за секвенирование генома реально живущего человека – и зародился проект «Джим». Хотя до «генома за 1000 долларов» было еще очень далеко, смета проекта «Джим» в один миллион долларов была ничтожно мала по сравнению с сотнями миллионов долларов, потраченных на первое секвенирование генома человека.
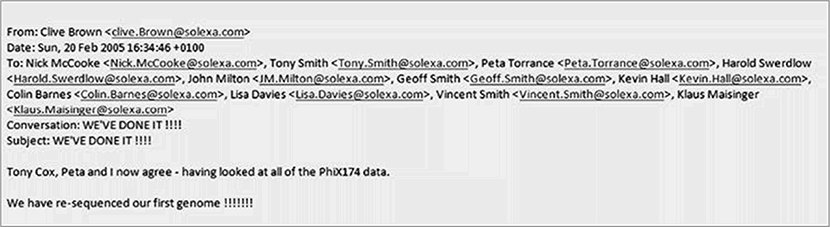
Маленький шаг вперед: внутрикорпоративное письмо руководителям Solexa, в котором сообщается о ключевом достижении – отсеквенирован первый геном крошечного вируса ФХ174
К апрелю 2008 года, когда статья об этом исследовании была опубликована в Nature (через 50 лет после публикации статьи о двойной спирали), у Ротберга и компании 454 развеялись всяческие сомнения по поводу поля и места деятельности. На ниве «новаторского секвенирования» становилось людно. В 2005 году талантливый профессор из Стэнфорда Стив Квейк опубликовал статью с описанием нового метода одномолекулярного секвенирования ДНК. Метод был применен для считывания всего пяти оснований, но это настолько впечатлило венчурного капиталиста и предпринимателя Стэна Лапидуса, что он немедленно полетел в Калифорнию, чтобы уговорить Квейка на открытие новой биотехнологической компании. Helicos сконструировала секвенатор, который позволил наблюдать на уровне единичной молекулы за синтезом комплементарной цепи одной молекулы одноцепочечной ДНК с помощью одной молекулы ДНК-полимеразы. В этой технологии флуоресцентно меченные нуклеотиды и конфокальная микроскопия высокого разрешения позволяют секвенировать последовательность в реальном времени и одновременно для многих полимераз. Лапидус окрестил его «генным микроскопом». С помощью этого микроскопа Квейк собирался секвенировать собственный геном за каких-нибудь 50 тысяч долларов. Увы, компания Helicos столкнулась с технологическими сложностями и разорилась, но ее технологиями по-прежнему пользуются некоторые весьма солидные фирмы.
Компания Pacific Biosciences (PacBio) коммерциализировала технологию одномолекулярного секвенирования. В основе метода лежало использование Zero-mode waveguide (ZMW) – углублений диаметром несколько десятков нанометров, ко дну которых прикреплена единичная молекула ДНК-полимеразы. Сквозь дно в ZMW-ячейку подается свет в виде крошечного прожектора, который специалисты именуют «волновод нулевой моды». Особенность конструкции ZMW-ячейки не дает распространяться световой волне и оставляет освещенным только объем порядка 20 цептолитров (20 × 10–21 литров) около дна ячейки. Компания PacBio использовала ту же самую технологию, которая применяется на сетке в дверце вашей микроволновки; сетка не допускает утечки микроволн, пока вы наблюдаете, как ваша курочка карри шкворчит внутри. Технологические новшества позволили наблюдать флуоресценцию единичной флуорохромной метки, прикрепленной к тому нуклеотиду, который в данный момент встраивается ДНК-полимеразой. Соответственно, к четырем типам нуклеотидов пришиты разные флуоресцентные метки, что позволяет их идентифицировать. В результате при полимеризации цепи ДНК зафиксированным в Zero-mode waveguide ферментом можно получить зависимость интенсивности флуоресценции от времени, из графика которой по пикам разного спектра затем и будет определена последовательность ДНК.
Хью Мартин, первый гендиректор и основатель PacBio, побился о заклад, что к 2013 году будет секвенировать человеческий геном за 15 минут. Он и близко не подошел к решению этой проблемы, поскольку секвенатор, применявшийся в компании, напоминал саркофаг и весил почти тонну, а продажи на первом этапе шли отчаянно медленно. Тем не менее по мере совершенствования технологии PacBio удавалось считывать все более и более длинные отрезки ДНК – в некоторых случаях по 50–60 тысяч оснований, а именно такие фрагменты удобно сшивать при окончательной сборке генома. Более того, компания предполагает найти рынок сбыта для своих технологий в зарождающейся отрасли – эпигенетике. В компании планируют использовать изменения кинетических показателей полимеризации ДНК и, опираясь на полученные результаты, обнаруживать химически помеченные нуклеотиды. В 2015 году появилась информация о новой версии секвенатора с очень удачным названием Sequel, который стоит всего 350 тысяч долларов и может параллельно обрабатывать до миллиона одномолекулярных реакций. С его помощью можно в полном объеме и очень точно отсеквенировать геном человека всего за 10–20 тысяч долларов.
Важнейшее деловое событие в области новых технологий секвенирования произошло в 2007 году, когда компания Illumnia из Сан-Диего приобрела Solexa за 650 миллионов долларов. На тот момент Illumnia была активно развивающейся генно-инженерной компанией, отвоевавшей у Affymetrix львиную долю на рынке биологических микрочипов, однако ей не хватало коммерческой технологии секвенирования ДНК. Пилотные модели настольных приборов-секвенаторов от Solexa только начинали поступать в крупнейшие геномные центры: Сенгеровский институт фонда Wellcome Trust в Кембридже в Великобритании и в Броудовский институт в Кембридже, штат Массачусетс. Вскоре логотип Solexa, красовавшийся на этих аппаратах, сменился на логотип Illumnia. Один ведущий ученый из Life Technologies – эта компания являлась одним из основных конкурентов Illumnia – был настолько раздосадован сделкой с Сенгеровским институтом, что даже написал жалобу в Палату лордов британского парламента, потребовав расследовать дело и намекая, что здесь не обошлось без коммерческого сговора.
К концу 2008 года – спустя шесть месяцев после того, как информацию о моем геноме опубликовали в Nature, – у Illumnia не осталось сомнений в том, что именно их компания обладает более выигрышной технологией секвенирования. В одном из выпусков Nature были опубликованы три исследовательские статьи, описывавшие секвенирование геномов от трех разных людей. Статья специалистов из Вашингтонского университета в Сент-Луисе рассказывала о секвенировании первого генома онкобольного; группа китайских ученых из Пекинского института геномики (ПИГ) впервые секвенировала геном монголоида; компания Illumnia описала секвенирование генома анонимного африканского мужчины, снискав заслуженное признание ученых из Solexa, которые неотступно и целенаправленно разрабатывали эту технологию в течение предшествующего десятилетия. На тот момент секвенирование человеческого генома по-прежнему обходилось дороже 500 тысяч долларов. Тем не менее это было вдвое дешевле стоимости секвенирования моего генома. Никогда ранее в одном номере научного журнала не публиковалось нескольких работ о нескольких человеческих геномах. Уже просматривались перспективы секвенирования сотен, если не тысяч, различных человеческих геномов – некоторые секвенировались бы исходя из медицинской необходимости, а другие – из чистого любопытства.

Секвенирование путем синтеза молекулы ДНК: схематическое изображение метода секвенирования ДНК, изобретенного в компании Solexa и впоследствии доработанного в компании Illumnia. Молекулы ДНК прикрепляются к подложке и амплифицируются. Нуклеотиды, помеченные флуоресцентными веществами – каждое основание своим цветом, пропускаются через участки ДНК и связываются с теми основаниями, которые им комплементарны. На снимке заметно местоположение всех встроившихся флуоресцентных оснований. После того как краситель будет удален химическим путем, цикл повторяется (обычно выполняется 100–200 таких циклов). Из последовательностей распознанных оснований в каждом кластере ДНК выстраивается вся последовательность генома
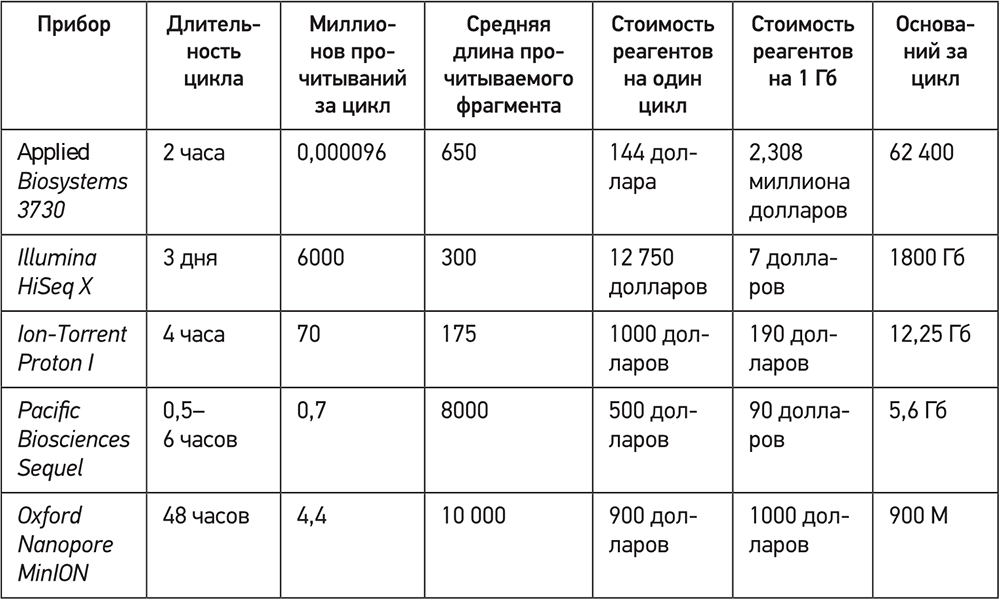
Сравнительные показатели основных коммерческих платформ для секвенирования нового поколения (по состоянию на 2016 год)
Стоит ли говорить, что идея персонального секвенирования генома привлекает далеко не только горстку самых состоятельных людей, даже если с научной точки зрения такой проект сравним с приобретением персонализированного автомобильного номера. Джордж Чёрч из Гарвардской медицинской школы – ученый-генетик и ярый сторонник секвенирования – основал компанию Knome, которая собралась зарабатывать именно на таких «особых клиентах» персональной генетики. Первым из этой компании стал швейцарский топ-менеджер из биотехнологической отрасли Дэн Стоическу, заплативший 350 тысяч долларов за то, что ему окажут особую честь: его ДНК будет интерпретирована командой светил медицины и биоинформатики. Он сообщил газете New York Times, что собирается изучить свой геном – записанный на фирменной флешке компании – не менее внимательно, чем разбирал бы инвестиционный портфель.
Ходили слухи, что среди первых клиентов компании Knome был и кто-то из членов британской королевской семьи. Открыто сообщалось, что секвенирование генома заказывал Оззи Осборн – вокалист Black Sabbath и известная звезда телевизионных реалити-шоу. Главный инженер компании Knome по интерпретации геномов Натан Пирсон летал в Великобританию, чтобы лично вручить Осборну результаты секвенирования в его шикарном имении в Букингемшире. Однако секрет долголетия звезды хэви-метал по-прежнему остается тайной, зашифрованной в его геноме. В 2010 году компания Illumnia также начала предоставлять подобные услуги со стартовой ценой 50 тысяч долларов за геном. Генеральный директор компании Джей Флэтли заказал секвенирование собственного генома и предсказал, что вскоре самые обычные люди будут разглядывать собственные геномные последовательности в приложениях для смартфонов и планшетов. Актриса Гленн Клоуз, активно пропагандирующая благотворительную помощь душевнобольным, также выразила желание секвенировать свой геном. Среди первых претендентов на секвенирование был топ-менеджер биотехнологической компании Solexa – Джон Уэст, организовавший вхождение Solexa в состав Illumnia. Уэст также оплатил секвенирование генома своей жены и двух детей-подростков, пытаясь выяснить семейную предрасположенность к таким заболеваниям, как тромбоз глубоких вен, а через пару лет опубликовал подробный анализ этой информации. Предлагая услуги по персонализированной геномике, Флэтли принял важное стратегическое решение. Опасаясь возмутить Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA), которое могло воспротивиться прямому «обращению к клиентам», он рассудил, что все испытуемые должны перед секвенированием пройти медицинское обследование и получить направление врачей на исследование своего генома. В результате появились первые рекомендации на персональное секвенирование генома. Сегодня Illumnia проводит по всему миру конференции «Узнай свой геном», посетители которых могут за несколько тысяч долларов получить полную информацию о собственном геноме и ее предварительную медицинскую интерпретацию.
Правы оказались те, кто говорил, что мой геном будет лишь первым из многих полностью секвенированных человеческих геномов. Однако существует гораздо более дешевый и эффективный способ предоставления персональной генетической информации потребителю, без такого полного секвенирования, которое делали для меня. Берется ДНК из буккального мазка или пробы слюны, а затем выполняется стандартноегенотипирование этого образца. Проще говоря, мы не считываем все три миллиарда оснований в геноме, а исследуем около одного миллиона заранее выбранных сайтов – так называемых однонуклеотидных полиморфизмов или SNP («снипов»). В геноме есть места, где генетический код у разных индивидуумов различается очень сильно: там, где у вас А, у меня может быть Г. Большинство этих генетических трансформаций совершенно безобидны (хотя по-своему полезны в качестве маркерных участков в экспериментах по генетическому картированию), но среди них есть и тысячи таких, которые ассоциированы с редкими или распространенными заболеваниями, а также с разными физиологическими и поведенческими признаками. Каждую неделю генетики каталогизируют медицинские проявления и ассоциации для все новых и новых SNP, и эта информация появляется на страницах ведущих медицинских и специализированных журналов по генетике.
В ноябре 2007 года две исключительно респектабельные компании – калифорнийская 23andMe и исландская deCODE Genetics – стали рекламировать персональный анализ генома на основе SNP. Руководители этих компаний – Энн Войжитски и Кари Стефанссон соответственно – были убеждены в том, что благодаря таким услугам человек сможет в какой-то степени контролировать свое здоровье. Энн Войжитски на тот момент была замужем за Сергеем Брином, сооснователем Google – таким образом, и Энн, и Сергей занимались поиском. В течение более чем десяти лет компания deCODE успела исследовать геномы большинства исландцев (население страны невелико), выполнив при этом массу прорывных исследований в области генетических ассоциациях и облегчив поиск множества новых лекарств. Однако ни 23andMe, ни deCODE не рекламировали свои услуги как диагностические анализы, пусть и сообщали информацию о некоторых генах, важных с медицинской точки зрения. Обсуждение результатов чьей-либо генетической экспертизы с врачом или генетиком-консультантом допускалось, но не являлось обязательным.
Всего за 199 долларов компания 23andMe предлагала любому желающему узнать свои генетические факторы риска. Длинный персонализированный каталог однонуклеотидных полиморфизмов (SNPs) сводился к самой обычной таблице в Excel. В нее включались те однонуклеотидные маркеры, которые, по мнению большинства специалистов и публикаций в рецензируемых научных изданиях, связаны с серьезными патогенетическими нарушениями, в частности с болезнью Паркинсона и некоторыми сердечно-сосудистыми заболеваниями. Также эти SNP могут быть связаны с менее интересными признаками, например с вязкостью ушной серы или способностью ощущать запах спаржи в собственной моче (опять же если до этого вы ели спаржу). Теперь любой желающий мог воспользоваться услугами по составлению собственного каталога однонуклеотидных полиморфизмов и проверить, есть ли у него А или Г в конкретной точке 17-й хромосомы. Для человека это может быть признаком критической мутации в гене, вызывающей рак. Мутационные изменения в 7-й хромосоме свидетельствуют о высоком риске тромбоза – речь идет о мутации фактора коагуляции V (также именуемого «фактор Лейдена»). Кроме того, можно установить наличие гена APOE, ассоциированного с болезнью Альцгеймера, это как раз тот фрагмент моей генетической информации, которую я осознанно решил не афишировать. Также всем желающим были предложены анализы на аллельные варианты генов, ассоциированные с повышенным риском развития широко распространенных, но сложно диагностируемых болезней: рака, сердечных заболеваний, рассеянного склероза и др. Компании, пользуясь патентованными алгоритмами, могут рассчитать ваш персональный риск и сравнить его с общепопуляционным риском.
Персональный анализ генома позволяет судить о предках исследуемого человека: сколько в вас европейской, азиатской и африканской крови. Проводится анализ Y-хромосомы, наследуемой от отца, и митохондриальной ДНК, передаваемой исключительно по материнской линии. Компания 23andMe стала весьма успешно выпускать линию одежды, в частности футболки, на каждой из которой запечатлено, какова же доля генов неандертальца у ее обладателя.

В 2010 году я оказался на конференции в Бостоне вместе с примерно двадцатью другими первопроходцами геномики – теми, чьи геномы были полностью секвенированы. Среди них были генеральные директора компаний, занимающихся секвенированием: Джей Флэтли (у меня за спиной), Грег Люсьер (в первом ряду с левого края) и Джордж Чёрч (мужчина с бородой в заднем ряду). Также присутствовали волонтеры, участвовавшие в гарвардском проекте «Персональный геном», в том числе гарвардский историк Генри Луис Гейтс по прозвищу Скип (в заднем ряду с левого края). Справа от меня – самая младшая в компании первопроходцев Энн Уэст

Один из первых рецептов на полное секвенирование генома, выданный тинейджеру Энн Уэст (дочери бывшего гендиректора компании Solexa Джона Уэста)
Очевидно, что недостаток информации в области персональной генетики и геномики может быть опасным или как минимум бессмысленным. После выхода компании 23andMe на рынок посыпались бесчисленные проклятия со стороны медицинского истеблишмента и стали слышаться шутки о «развлекательной геномике». Наиболее широкий отклик получила редакционная статья в «Медицинском журнале Новой Англии» (New England Journal of Medicine). Главный редактор Джеффри Дрейзен и его коллеги писали: «Пока мы не можем употребить геном ради практической пользы, клиентам лучше тратить деньги на тренажерный зал или на личного инструктора по фитнесу», а также рекомендовали придерживаться здоровой диеты и заниматься физкультурой, чтобы снизить риск сердечно-сосудистых заболеваний и т. д. Например, мой друг Сидней Бреннер порицал так называемую развлекательную геномику, ставя ее в один ряд с астрологией.
Хотя медицинский истеблишмент имеет право настороженно относиться к научной значимости и клинической применимости анализов ДНК, предлагаемых пациентам «в розницу» как товар, их скептические замечания были изрядно сдобрены патернализмом. Неудивительно: они не учитывали в своих «уравнениях» среднестатистического врача. С одной стороны, я чистосердечно приветствую право потребителя знать собственную персональную генетику и на основе этих данных принимать меры, которые он сам сочтет необходимыми. Генетические стартапы, нацеленные на потребителя, всего лишь цитируют уже опубликованные в литературных источниках сведения на предмет наличия известных ассоциаций между маркерами ДНК и болезнями, а затем соотносят эту информацию с ДНК конкретных клиентов, предусматривая при этом все необходимые оговорки. С другой стороны, одно дело – раскрывать генетические тонкости, связанные с консистенцией ушной серы (влажная она или сухая), атлетическими талантами (спринтер или стайер) или с феноменом внезапного чихания при раздражении сетчатки глаза ярким светом, и совершенно иное – озвучивать, каков у конкретного пациента риск болезни Альцгеймера или возникновения мутации, вызывающей рак груди.
На этом тесном рынке компания 23andMe скоро стала выделяться среди прочих, причем в большей степени благодаря талантливому маркетингу, чем техническому совершенству методов и качеству предлагаемых услуг. На первом этапе фирма получала финансовую поддержку от Google, а также выгодно использовала свои «корни» из Кремниевой долины. Компания давала «светские рауты», на которых присутствовали рок-звезды, модели и голливудские знаменитости – от Питера Гэбриэла в Давосе до Харви Вайнштейна и Руперта Мёрдока на Манхэттене. Рекламные дирижабли с логотипом 23andMe можно было заметить над бухтой Сан-Франциско, а в 2008 году фирма выиграла конкурс «Изобретение года», проводимый журналом Time (тогда их исландские конкуренты были в ярости). Шокирущим откровением поделился и сам Сергей Брин: в истории его семьи были случаи болезни Паркинсона, и Брин обнаружил у себя мутацию в гене LRRK2, как раз отвечающем за эту болезнь. Конкуренция понемногу угасла, вскоре представители deCODE отправились в суд оформлять банкротство. Другой ранний конкурент, компания Pathway Genomics, ненадолго опередила 23andMe, заключив сделку с аптечной сетью Walgreens, в результате которой их наборы для анализа ДНК оказались на аптечных полках. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов, обеспокоенно наблюдавшее со стороны за индустрией потребительской генетики, довольно быстро задавило эту инициативу Pathway Genomics, пока такая диагностика не приняла неконтролируемые масштабы.
За шесть лет 23andMe собрала базу данных из более чем 650 тысяч индивидуальных профилей ДНК, или, как бы мы сказали, генетических паспортов. Большинство клиентов компании дали добровольное согласиена обработку персональной информации о состоянии своего здоровья, предоставленной в анкетах через онлайн-сервисы, что позволило ученым из 23andMe проводить виртуальное моделирование по генетическому картированию и находить новые гены, отвечающие за болезнь Паркинсона, астму и другие заболевания. Однако в ноябре 2013 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов, встревоженное очередной рекламной кампанией на телевидении, наконец не выдержало. Агентство направило Войжитски письмо с требованием о приостановлении и последующем прекращении деятельности, запретив 23andMe сообщать клиентам о генетических аспектах их состояния здоровья. Новые клиенты могли получить генетическую информацию исключительно о своих предках. Серьезное беспокойство было связано с тем, что клиент мог получить ошибочную информацию либо такие данные, которые можно неправильно интерпретировать. В качестве примера агентство приводило такую гипотетическую ситуацию: женщина получает ложноположительный результат анализа на наличие гена BRCA1, который может ввести в заблуждение лечащего врача и спровоцировать его на проведение ненужной хирургической операции. При этом любопытно, что FDA не запрещало клиентам скачивать из интернета их генетическую информацию в необработанном виде либо получать ДНК-отчет, действуя наоборот: загружать информацию о геноме на сайты, предлагающие услуги по интерпретации генов; одним из таких сервисов был Promethease.
В основе столкновения между FDA и 23andMe лежал фундаментальный вопрос: следует ли позволять индивиду иметь доступ к подробной информации о собственном геноме без посредничества врача-профессионала, играющего, по сути, роль «ключника»? Я твердо убежден: да, следует. FDA заняло эту позицию, видимо, полагая, что широкая общественность может столкнуться с некой гипотетической катастрофой, хотя и не продемонстрировало ни единого реального примера. Действительно, большинство фактов (в том числе описанных в многочисленных рецензируемых статьях, опубликованных не где-нибудь, а в New England Journal of Medicine) свидетельствуют о том, что общество вполне в состоянии понимать риски, связанные с потребительскими генетическими анализами. Генетик Роберт Грин и специалист по биоэтике Нита Фарахани в своей статье, опубликованной в Nature, писали следующее: «агентство должно воздерживаться от ограничений в сфере потребительской геномики, пока не выявлены эмпирические факты нанесенного ею вреда».
Через несколько месяцев после того, как FDA ввело запрет, все-таки удалось задокументировать случай некачественного потребительского генетического анализа. Как сообщили Кэт Браунстейн и ее коллеги из Детской больницы Бостона, клиент неназванной компании, получивший результаты генетического тестирования, был неверно проинформирован, что у него найдена серьезная мутация в гене TPMT. От этого гена зависит, излечима ли в его случае болезнь Крона, которой он страдает. Наличие этой мутации делает неэффективной и даже токсичной всю ранее проводимую терапию. Ситуация могла обернуться катастрофой для пациента. К счастью, секвенирование генома, выполненное другой диагностической компанией, показало, что заявленной мутации на самом деле нет. Таким образом, при получении результата необходимо учитывать, что анализ генома, как и любой медицинский анализ, может давать определенный процент как ложноположительных, так и ложноотрицательных результатов. Учитывая вышесказанное, необходимо понимать, что выбор лечебных мероприятий не должен быть основан на результатах только одного генетического анализа.

Флуоресцентное окрашивание хромосом позволяет представить себе состав генома того или иного индивида. Ивонн Морантес – сотрудница компании 23andMe, у нее мексиканские и пуэрториканские корни. Теперь она гораздо лучше представляет себе свою генетическую родословную
Компании 23andME, столкнувшейся с препонами, которые чинило агентство FDA, пришлось принять меры. Во-первых, после долгих дискуссий с агентством компания 23andMe в апреле 2017 года наконец одержала победу, получив разрешение передавать клиентам результаты анализов и их интерпретацию по набору из 10 болезней, в том числе по болезням Альцгеймера и Паркинсона. Во-вторых, компания открыла в Великобритании и других странах филиалы, не подчиняющиеся ограничениям, наложенным FDA. Наборы для анализа ДНК теперь снова свободно продавались в одной из британских аптечных сетей, ориентированной на массового потребителя. Имея в распоряжении более миллиона профилей ДНК, 23andMe наконец достигла критической массы, при которой она стала представлять интерес для больших фармацевтических компаний, заключила с ними несколько прибыльных сделок и наняла на работу гениального специалиста – бывшего директора компании Genentech по научным исследованиям и разработкам, которому и поручила возглавить корпоративную программу поиска новых лекарств.

Николас Волкер: ребенок-символ, демонстрирующий, как секвенирование генома может положить конец безнадежной диагностической одиссее
Николас Волкер только что отпраздновал свой одиннадцатый день рождения, как любой другой мальчик, он был счастлив носиться по танцевальному залу, заниматься йогой, плаванием и карате. Хотя, глядя на него, не скажешь, что он – также ребенок-символ в истории революции клинического секвенирования геномов.
Эта история началась в один уик-энд летом 2009 года, когда Говард Джейкоб, генетик из Медицинского колледжа штата Висконсин, открыл электронное письмо от коллеги-врача, в котором тот в душераздирающих тонах изложил просьбу храброго четырехлетнего мальчика. Врачи, наблюдавшие и лечившие маленького Ника, никак не могли диагностировать, чем же он болен, – подозревали аутоиммунное заболевание, медленно сжирающее его пищеварительный тракт. Ник перенес больше сотни операций – врачи тщетно пытались залатать дыры у него в кишках. Большую часть времени из четырех лет своей жизни он провел в детской больнице.
В письме, открытом на экране компьютера у Джейкоба, был единственный вопрос: если отсеквенировать геном Ника – появится ли шанс обнаружить генетическую подоплеку болезни мальчика в том случае, если дело действительно в генах? В лаборатории Джейкоба ставили эксперименты на крысах, а не на людях, но он ждал подходящего момента, чтобы опробовать клиническое секвенирование генома. В данном случае представилась отличная возможность. Что, если странное заболевание Ника в мельчайших подробностях прослеживается в его генетическом коде? Однако в то время врачи могли лишь предложить тестировать подозрительные гены по одному. Джейкоб сознавал, что для поиска истины, которая помогли бы завершить генетическую одиссею Ника (так он ее называл), врачи должны были провести полномасштабный поиск: секвенировать геном ребенка и систематически отсеивать все варианты ДНК, пока наконец не выявят тот, из-за которого болеет Ник.

Иголка в стоге сена: чтобы вычленить редкую разрушительную мутацию из пула с тысячами потенциальных вариантов ДНК в геноме пациента, исследователи сужают поле поиска, отсеивая такие изменения последовательностей, которые сравнительно широко распространены, либо те мутации, которые, скорее всего, не будут влиять на функцию белков. Таким образом, список «подозрительных» мутаций иногда сужается менее чем до десяти
Еще в 2009–2010 годах стоимость полного секвенирования генома оставалась запредельно высокой, поэтому команда Джейкоба, сотрудничавшая с Life Sciences, пошла на хитрость, секвенировав экзом Ника, то есть 2–3 % генома, на которые приходится около 20 тысяч генов, и наудачу предположив, что мутация не затеряна в куче некодирующей «мусорной» ДНК. Одна из коллег Джейкоба, шотландский биоинформатик Лиз Уортисоставила список примерно из двух тысяч потенциально подозрительных генов – это целых 10 % генетического багажа человека.
Никаких особенных мутаций там не обнаружилось. Но Лиз обратила внимание на ген XIAP, находящийся в X-хромосоме. У Ника на этом участке оказался такой вариант последовательности, который явно указывал на редкое генетическое заболевание, именуемое «X-сцепленный лимфопрофилеративный синдром второго типа», разрушающий нормальную работу иммунной системы. Команда из Висконсина догадалась, «откуда ветер дует»: нужно было срочно действовать, ведь теперь лечащие врачи Ника имели все основания назначить ему трансплантацию костного мозга.
Эпопея Ника была изложена в виде серии статей в Milwaukee Journal Sentinel, удостоенной Пулитцеровской премии, а затем в книге One in a billion («Один на миллиард»), написанной теми же авторами. После успешной трансплантации Ник впервые в жизни смог с удовольствием отметить Хэллоуин, попробовать твердую пищу и даже пошел в школу. Увы, невзгоды Ника пока не закончились: он стал страдать настолько частыми приступами эпилепсии, что вынужден был носить защитный шлем. Родители Ника обратились в Законодательное собрание штата Висконсин с просьбой разрешить мальчику принимать ограниченные дозы марихуаны, которая помогает от эпилепсии. Все-таки для Ника это был огромный прогресс. Выражение «конец диагностической одиссеи» стало ассоциироваться прежде всего с тем подходом, который впервые опробовали Джейкоб с коллегами. Это и неудивительно: сегодня стоимость полного секвенирования генома пациента составляет от двух до трех тысяч долларов, что, по иронии судьбы, даже меньше платежей, взимаемых за секвенирование единственного ракового гена, запатентованного некоторыми компаниями, такими как, например, Myriad Genetics, контролирующая проведение теста BRACAnalysis.
После того как генетики, выступив в роли сыщиков, смогли идентифицировать характерные для ряда заболеваний мутации, многие дети повторили путь Ника; в некоторых случаях (но пока их очень мало) удалось достичь весьма примечательных результатов. Так, близнецы, дети Ретты и Джо Берри, с раннего детства страдали неврологическими расстройствами. Им было выставлено огромное количество крайне противоречивых диагнозов, в том числе судорожная параплегия. Лечение нейрохимическим препаратом L-диоксифенилаланином ненадолго давало положительный эффект, но затем маленькой Алексис снова становилось хуже. К счастью, Джо Берри, отец детей, работал главным системным администратором в Life Technologies, поэтому у него были полезные связи, позволившие провести секвенирование. Когда коллеги секвенировали ДНК его детей, там обнаружилась редкая мутация, указывающая на синдром Сегавы. Достаточно было дополнить L-диоксифенилаланин селективным ингибитором обратного захвата серотонина (это очень распространенное и доступное лекарство) – и близнецы практически полностью выздоровели.
Многие дети избежали диагностических одиссей с тех пор, как история Ника Волкера попала на первые полосы газет. Это были Лилли Гроссман из Ла-Хольи, штат Калифорния; Джейкоб и Дилан Эллингемы из Сакраменто, храбрый Шелби Вейлинт из Финикса, штат Аризона (Шелби теперь может ходить благодаря тому, что удалось открыть критическую ошибку в его гене, отвечающем за синтез дофамина). Когда Кэт Браунстейн и ее коллеги из детской больницы Бостона устроили соревнование между тридцатью командами, которым было поручено идентифицировать мутации у трех пациентов, одна мама, узнавшая, что мышечное расстройство у ее сына обусловлено мутацией в гигантском гене титина, едва сдерживала слезы, когда благодарила ученых. Ее сын одиннадцать лет блуждал по медицинским лабиринтам, и вот эта история закончилась постановкой диагноза.
В настоящее время все больше и больше медицинских центров предлагают те или иные варианты клинического генетического секвенирования. В детской больнице города Мэдисон, штат Висконсин, врачи ежемесячно проводят встречи, на которых представляют и обсуждают пациентов-кандидатов, которым безотлагательно требуется полное секвенирование генома. Ни в одном другом медицинском центре не изучили столько полных геномов пациентов, сколько в Бэйлорском медицинском колледже, город Хьюстон. Кристин Энг с коллегами секвенировали ДНК двух тысяч пациентов; при этом в 25 % случаев удалось верифицировать диагноз. Аналогичные показатели успешной диагностики наблюдаются и в большинстве других центров, в частности у группы Джейкоба, открывшей специализированный центр клинической геномики в Хантсвилле, штат Алабама. По мере того как медицинская польза от клинического секвенирования генома становится все очевиднее, страховые компании также стараются на этом зарабатывать: зачастую все затраты на секвенирование генома возмещаются, хотя такую работу можно сравнить просто с высокотехнологичным походом на рыбалку.
Правда, даже у самых многообещающих подходов есть свои недостатки. Во-первых, приходится компилировать колоссальную массу генетической информации, не связанной с рассматриваемым заболеванием, – генетик Айзек Кохейн назвал эти данные словом «инциденталом». Какие права имеют пациенты и их родственники на эту дополнительную информацию? Следует ли сообщать им информацию лишь об одном, рассматриваемом гене? Как поступать с информацией о десятках других обнаруженных генов, которые могут серьезно влиять на здоровье?
С разрешения Американского колледжа медицинской генетики (АКМГ) ученые, занимающиеся этим вопросом, составили список примерно издвадцати генов, которые врач должен проверять вне зависимости от обстоятельств. Критики возражали, говоря, что при этом нарушаются права пациента, который, возможно, чего-то о себе знать не хочет, но Роберт Грин, один из авторов доклада, развенчивает такие опасения: «Радиолог, интерпретирующий ваш рентгеновский снимок… по долгу службы обязан изучить весь снимок и сообщить вам обо всех случайных находках, которые потенциально может обнаружить». Невозможно оправдать врача, который не скажет пациенту об опухоли в почке, потому что искал у него всего лишь камни. То же должно касаться и генетических анализов. Проанализировав результаты общественного мнения в отношении своих исходных рекомендаций, АКМГ выпустил обновленные рекомендации, согласно которым семьи должны иметь возможность добровольно отказаться от информации о каких-либо дополнительных результатах, полученных при секвенировании, но это должно произойти до момента проведения процедуры секвенирования, а не после предоставления результатов.
Стоимость секвенирования геномов резко снизилась, и это событие резонировало во всей индустрии, специализирующейся на диагностике генов. Кажется абсурдным, что сегодня можно секвенировать геном пациента полностью за ту же цену – несколько тысяч долларов, какую некоторые компании требуют за анализ единственного гена. Думаю, что со временем врачи массово перейдут к полному секвенированию геномов, хотя для этого понадобится решить множество проблем – от поддержки компьютерных систем до обеспечения страхового возмещения и пересмотра всей системы преподавания современной генетики студентам-медикам. Добавьте сюда и некоторые юридические аспекты.
В мае 2009 года Американский союз защиты гражданских свобод (ACLU) подал иск от лица двух женщин против Патентного бюро США и Myriad Genetics, диагностической компании из Солт-Лейк-Сити, запатентовавшей гены BRCA1 и BRCA2, отвечающие за рак груди. В иске говорилось, что компания Myriad, агрессивно отстаивая собственную монополию на проведение генетических исследований, позволяющих выявить рак груди, не позволила одной из истиц перепроверить результат ее же собственных анализов, другая истица не смогла получить страхового покрытия по программе Medicare за анализ. Дело дошло до Верховного суда США. На кону была не только судьба патентов Myriad, связанных с генами BRCA; теперь уже был подвергнут сомнению один из центральных столпов биотехнологической индустрии – убеждение, что идентифицированные человеческие гены подобны изобретениям и что их можно патентовать.
Адвокаты компании Myriad доказывали, что их фирма не просто идентифицировала BRCA1 в 17-й хромосоме, но и первой выделила его, то есть фактически «изобрела», изготовив отредактированную копию гена, которую затем использовала во всех своих анализах. Истицы ответили двумя следующими ключевыми доводами. Во-первых, ген – это естественная часть хромосомы, поэтому обычное выделение участка ДНК едва ли может быть объектом для патентования. Судья Соня Сотомайор парировала речь адвоката следующими словами: «Если отрезать ломтик печени, это же не позволяет запатентовать печеночную ткань. Вы берете ген и вырезаете из него кусочек, верно? Так в чем же разница?»
Излагая свой второй аргумент, Эрик Ландер камня на камне не оставил от фундаментального допущения, применявшегося при патентовании генов, согласно которому изолированные гены – это фрагменты ДНК, не встречающиеся в природе. Ландер утверждал, что все как раз наоборот: исследования показывают, что копии генов действительно существуют в крови и их там вполне достаточно для диагностических целей. Я прибавил к этому собственное консультативное заключение, в котором указывал, что ради блага науки гены не должны патентоваться; гены по природе своей уникальны в отличие от любых прочих обычных, пригодных для патентования «составов вещества».
13 июня 2013 года, четыре года спустя после первого процесса, Верховный суд отменил «генетические патенты». «Myriad ничего не создала, – постановила судья Кларенс Томас. – Следует признать, что Myriad открыла важный и полезный ген, но выделение этого гена из окружающего генетического материала не является актом изобретения». В сущности, суд постановил, что идентификация и извлечение важного гена из человеческого генома ценны само по себе, но не дают права патентовать генетическую последовательность.
Такое решение было с восторгом воспринято среди ученых-генетиков. Гарри Острер из Медицинского колледжа города Нью-Йорка им. Альберта Эйнштейна выразил мысли многих: «Такое решение возвращает изолированную ДНК и ее гены в собственность Природы, где им и положено быть… это решение откроет возможности для новых анализов и даст второй шанс тем, кто сейчас его лишен». А Мэри-Клэр Кинг, впервые выделившая ген BRCA1 (это было в то время, когда многие вообще сомневались в наличии генетической предрасположенности к раку груди; об этом мы поговорим в главе 14), приветствовала это решение как «фантастический результат в пользу пациентов, врачей, ученых и здравого смысла». В течение считаных недель после этого вердикта несколько диагностических фирм запустили собственные программы анализа на наличие BRCA1 уже по гораздо более доступным ценам.
Стремительное удешевление секвенирования ДНК вкупе с другими технологическими достижениями изменило весь профиль клинической диагностики. Одним из важнейших достижений стал метод NIPT (неинвазивная пренатальная диагностика); метод основан на том, что ДНКплода в небольшом количестве присутствует в материнском кровотоке. Следовательно, при помощи обычного анализа крови можно выявить такие расстройства, как синдром Дауна и иные так называемые трисомии, связанные с наличием лишней хромосомы в геноме плода. Такой анализ позволит многим будущим матерям обойтись без аниоцентеза или биопсии хориона; обе эти процедуры представляют хоть и небольшой, но доказанный риск для плода (теперь такие анализы могут проводиться лишь для подтверждения положительного результата NIPT). Несколько компаний, в том числе Sequenom, Ariosa, Ventara и Natera, теперь предлагают на рынке анализы для определения таких состояний.
В настоящий момент NIPT-тестирование позволяет выявлять лишь немногочисленные врожденные аномалии. В принципе, с помощью такого метода можно полностью исследовать геном плода. Новаторскую идею предложил Джей Шендью, врач-исследователь из Вашингтонского университета. Он вместе с коллегами разработал метод, позволяющий почти со стопроцентной точностью вычислять геномную последовательность плода, полученную из образца материнской крови, сравнивая ее с последовательностями, взятыми у обоих родителей. Им удалось на основе анализа проб крови матери и слюны отца полностью реконструировать наследственный материал будущего ребенка и проверить его на наличие так называемых моногенных заболеваний.
Этические проблемы в области секвенирования генов предположительно здорового плода будут обсуждаться еще много лет. Но сегодня такая практика существует. Разиб Хан, аспирант тридцати с небольшим лет, блогер, решил секвенировать ДНК своего первого ребенка, когда жена еще была беременна. Хотя еще в 2012 году в New England Journal of Medicine появилась статья о полном секвенировании генома плода на этапе внутриутробного развития, эта операция была проделана для подтверждения положительного цитогенетического анализа. Хан решил секвенировать геном своего еще не рожденного ребенка не из-за каких-то безотлагательных проблем с его здоровьем, а потому что это «круто» и Хану нравилось «раздвигать границы возможного». Он убедил коммерческую компанию, занимавшуюся генетическими анализами, провести биопсию хориона на материале кусочка плаценты жены, но чтобы образец ДНК врачи вернули обратно Хану. (Представители компании колебались: как правило, образец ДНК передают лечащему врачу, а не мужу пациентки.) Затем Хан уговорил коллегу запустить ДНК на свободную дорожку в рамках текущего высокопроизводительного эксперимента по секвенированию. Воспользовавшись бесплатным веб-ресурсом Promethease, Хан проанализировал данные и с облегчением убедился, что ДНК его ребенка «довольно скучная». В чарующем своей новизной новом мире персональной геномики «скучная» означает «ура, пронесло».

Президент Джордж Буш подписывает закон о запрете дискриминации на основе генетической информации (GINA) в 2008 году
Еще одно юридическое решение, на сей раз касающееся генетической конфиденциальности, серьезно повлияло на нарождающуюся геномную медицину. По мере того как все больше и больше людей получали доступ к своей генетической информации, неудивительно, что становится необходимо позаботиться о приватности и безопасности этой информации. Что если данные о моей ДНК окажутся в распоряжении моей страховой компании? После нескольких неудачных попыток удалось принять в Конгрессе закон, запрещавший использовать генетическую информацию для какой-либо дискриминации при трудоустройстве либо отказывать в страховании здоровья исходя из такой информации. В 2008 году президент Джордж Буш утвердил закон о запрете дискриминации на основе генетической информации, сокращенно GINA. Неясно, удалось ли предотвратить при помощи этого закона случаи такой дискриминации. Также отметим, что GINA никак не влияет ни на страхование жизни, ни на долгосрочное страхование по медицинскому уходу. Генетик Роберт Грин припоминает случай из практики: несколько лет назад он проводил клиническое исследование того, как родственники пациентов с болезнью Альцгеймера воспринимают собственные анализы на присутствие гена APOE. Прежде всего, было изучено, какой психологический эффект оказывает новость о повышенном риске развития деменции с поздним началом. Грин отметил, что волнение по этому поводу минимально; однако, как показываютнаблюдения, многие носители этого гена интересуются долгосрочным страхованием по медицинскому уходу. Конечно, можно понять, почему эти люди пользовались «инсайдерской» информацией с целью переиграть систему. Следует признать, что эта упреждающая информация является формой знаний о самом себе. Однако если такая практика распространится на другие состояния и станет широко использоваться, то в результате будет уничтожен бизнес долгосрочного страхования по медицинскому уходу, а также частное медицинское страхование, когда здоровые платят за больных, но никто заранее не знает, в какой из категорий кто окажется. Поэтому руководство страховых компаний крайне заинтересовано в выявлении случаев использования данных такой «агентурной разведки». Да, уж вот где есть веские причины для паранойи.
В 2013 году Янив Эрлих, израильский ученый, тогда работавший в Институте Уайтхеда, опубликовал результаты исследования, которые всколыхнули все генетическое сообщество. Группа Эрлиха использовала для исследования предположительно анонимную геномную информацию из открытых баз данных и путем перекрестного сравнения этой информации с подборками родословных смогла идентифицировать конкретные личности. Эрлих хотел доказать, что людям, сдающим ДНК для клинических исследований, не гарантирована конфиденциальность. Какие еще лазейки могут быть найдены в период всего биоинформационного бума нашего времени?
В 2005 году генетик Джордж Чёрч из Гарвардской медицинской школы основал проект PGP («Личный геном»), стремясь изменить подходы к ранее имевшимся проблемам Проект PGP архивирует и собирает информацию с абсолютно открытых для общего пользования источников. Чёрч предлагает добровольцам полностью расшифровать их геном, в обмен на что они соглашаются выложить в открытый доступ полученные генетические данные. Среди первых добровольцев были двое гарвардских коллег Чёрча – Генри Луис Гейтс-младший по прозвищу Скип, психолог и писатель Стивен Пинкер, а также инвестор Эстер Дайсон и Миша Ангрист из Университета Дьюка, описавший становление всего проекта в книге Here Is a Human Being («Это человек»). «А король-то голый, – говорит в своей книге Миша Ангрист, – абсолютная приватность и конфиденциальность – это всего лишь иллюзия». Правда, в утопических представлениях о полной прозрачности мира в целом и конкретного генома в частности нравится жить далеко не каждому члену социума.
В январе 2014 года бывший генеральный директор Illumnia Джей Флэтли стал возмутителем спокойствия на крупной медицинской конференции в Сан-Франциско. В аудитории, до отказа забитой банкирами, инвесторами и аналитиками, он заявил, что его компания вот-вот преодолеет рубеж «геном за тысячу долларов». Компания уже захватила лидерство в гонке по производству аппаратуры для секвенирования, а здесь представила новый инструмент: HiSeq X Ten. Работая на полную мощность в течение проектного срока (четыре года), машина должна была отсеквенировать тысячи человеческих геномов по тысяче долларов за каждый. Проблема заключалась в том, что сами машины можно было заказать только в комплекте по 10 штук (отсюда и название) и стоимость каждой составляла миллион долларов. Тем не менее исследовательские центры и корпорации поспешили закупить эти машины, отчаянно стремясь не отстать в гонке по секвенированию геномов. Среди заказчиков были крупные геномные центры из Бостона, Нью-Йорка и Великобритании, азиатские организации, занимающиеся заказными научными исследованиями, а также новая компания Крейга Вентера Human Longevity.
Не все были готовы признать, что Illumnia достигла психологического рубежа «геном за тысячу долларов». В журнале Nature появился комментарий автора, назвавшегося Уинстоном Черчиллем, который доказывал, что этот ценовой порог может быть достигнут только в 2018 году. Но попутный ветер благоприятствовал Флэтли и его фирме из Сан-Диего. После того как в конце 2008 года Illumnia опубликовала свои первые несколько последовательностей геномов, она набрала темп, повысила качество работы и длину считываемых фрагментов, а гонка тем временем практически прекратилась. Конкуренты один за другим сошли с дистанции. Среди них была компания Helicos, разработчик прибора HeliScope для одномолекулярного секвенирования; в компании не смогли справиться с технологическими сложностями своего аппарата, который был размером с заводской рефрижератор. Не выдержала конкуренции и Roche, фармацевтический гигант, который на раннем этапе приобрел 454 Life Sciences, но так и не смог развить их технологию, подняв ее на более высокий уровень.
На протяжении нескольких лет наиболее серьезную конкуренцию для Illumnia составляла компания Life Technologies, которая приобрела небольшую бостонскую фирму Agencourt и взялась за разработку альтернативного метода секвенирования. В отличие от Illumnia и большинства других конкурентов, работавших с ДНК-полимеразой, в основе системы SOLiD использовалась ДНК-лигаза. Командой секвенаторов SOLiD руководил Кевин Маккернан, умный словоохотливый энтузиаст-биотехнолог, который по иронии судьбы ранее выступал конкурентом предшественника Life (Applied Biosystems). Это было в те годы, когда он когда работал в команде Эрика Ландера на проекте «Геном человека». Система секвенирования SOLiD конкурировала непосредственно с HiSeq. В течение года с небольшим Маккернан и Флэтли упражнялись в немного ребяческой пикировке мнениями, выпуская пресс-релизы в духе «у меня точно как у тебя, но на один больше». Тот факт, что штаб-квартиры обеих компаний – LifeTechnologies и Illumnia – располагались в районе Сан-Диего, лишь распалял их соперничество.
Пока многие академические лаборатории, в том числе Бэйлорский геномный центр Ричарда Гиббса, осваивали приборы SOLiD, на тот момент компании Life не удавалось выдавить Illumnia с ее лидерских позиций. В 2010 году Life сменила курс, рискнув по-крупному: она выделила около 725 миллионов долларов на поддержку новейшей компании Джонатана Ротберга Ion Torrent Systems. После ухода из компании 454 Ротберг продолжал разрабатывать альтернативные варианты секвенирования. Он придумал хитроумный метод, суть которого заключалась в следующем: метод основан на связи между химической и цифровой информацией, что позволяет быстрее и проще секвенировать большое количество образцов. Эта технология также называется рН-индуцированным секвенированием. Процесс основан на детекции протонов, которые получаются при синтезе цепи ДНК как побочный продукт. Как следствие, рН раствора меняется, что и можно детектировать. Платформа Ion Torrent отличается от остальных технологий секвенирования тем, что в ней не используются модифицированные нуклеотиды и оптические методы. Метод Ion Torrent позволяет исследовать транскриптомы, малые РНК. Платформа Ion Torrent позволяет считывать последовательность ДНК гораздо дешевле, чем другие имеющиеся инструменты, работа которых связана с использованием мощных лазеров и дорогих камер.
Когда воодушевленный Ротберг представил аппарат Personal Genome Machine в переполненной аудитории на конференции по геномике в 2011 году, он даже заявил, что еще вчера эта машина секвенировала ДНК прямо у него в гостиничном номере, хотя это, возможно, противоречило указаниям FDA. Двое коллег Ротберга водрузили прибор на сцену, чтобы продемонстрировать, насколько (относительно) мобильна эта машина. Аппарат Ротберга, стоивший каких-то 50 тысяч долларов, был призван демократизировать секвенирование – и это в какой-то степени удалось. Продажи росли благодаря заманчивой перспективе, что каждое последующее поколение чипов в основе системы позволит экспонентно повышать темпы секвенирования. В результате состязание за победу в деле инновационного секвенирования превращалось в гонку двух фаворитов – Illumnia и LifeTechnologies; компания 454 проигрывала конкуренцию, а замыкала этот дивизион компания Roche.
Однако «гонка секвенаторов», несомненно, должна была пройти еще немало зигзагов и поворотов. Более двух десятилетий исследователи работали над, казалось бы, простой новой концепцией: дело в том, что при протягивании ДНК через бактериальные белковые мембраны, образованные естественным образом и именуемые нанопорами, можно определять последовательность нуклеотидов. Впервые эту идею сформулировал химик Дэвид Димер из Калифорнийского университета в Санта-Крусе, обрисовавший такую систему в 1989 году на листе желтоватой линованной бумаги.
Через несколько лет Димер совместно с Дэном Брэнтоном из Гарварда опубликовал результаты исследования, подтверждающие эту концепцию. «При условии дальнейшей доработки этот метод, в принципе, мог бы обеспечить непосредственное и высокоскоростное обнаружение последовательности оснований в отдельно взятых молекулах ДНК или РНК», – прогнозировали авторы, в то время как коллеги еще только готовились к первым черновым работам по секвенированию человеческого генома.
Спустя чуть более десяти лет британский химик и специалист по нанопоровому секвенированию оксфордский профессор Хаган Бейли основал компанию Oxford Nanopore Technologies. Компания пригласила на работу двух «ветеранов» из Solexa: Клайва Брауна и Джона Милтона, – которым было поручено разработать технологии: от компьютерных и программных систем до создания самих нанопор и других компонентов. Работа в значительной степени базировалась на идеях, сформулированных Димером и Брэнтоном еще в 1990-е годы: проделываем белковую нанопору в плоской полимерной мембране, так что ДНК может проникнуть через мембрану лишь сквозь эту крошечную нанопору. Пропускаем через мембрану электрический ток и измеряем сопротивление (изменение тока) за период времени. ДНК проскальзывает сквозь эту пору со скоростью, стремящейся к 500 основаниям в секунду. Далее задействуем хитрую информатику – например, такой инструментарий, как рекуррентные нейронные сети, – чтобы идентифицировать конкретные основания исходя из результатов измерения тока.
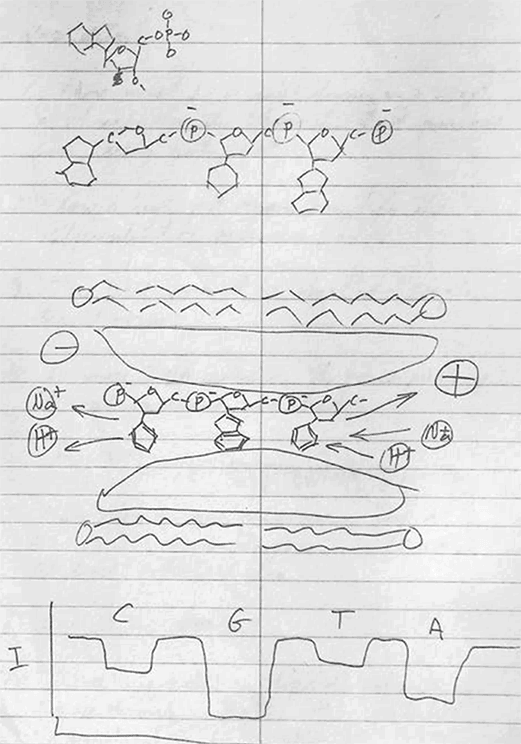
В 1989 году Дэвид Димер схематически изобразил идею нанопорового секвенирования ДНК
Разумеется, будь все так просто, Oxford Nanopore – либо одна из конкурирующих компаний – стала бы известна в каждом доме. На самом деле ученым из компании предстояло методом проб и ошибок отмести множество стратегий, прежде чем остановиться на системе, применяемой в настоящее время. Исходная идея, которую окрестили «срежь и брось», была связана с использованием фермента под названием экзонуклеаза. Фермент отхватывает отдельные нуклеотиды с хвостового конца последовательности ДНК, примерно как «Пакман», после чего эти фрагменты один за другим проходят через пору, расположенную снизу. Но эта идея оказалась провальной; от нее отказались и стали пропускать через пору цельную ДНК, используя другой фермент, расплетающий двойную спираль.
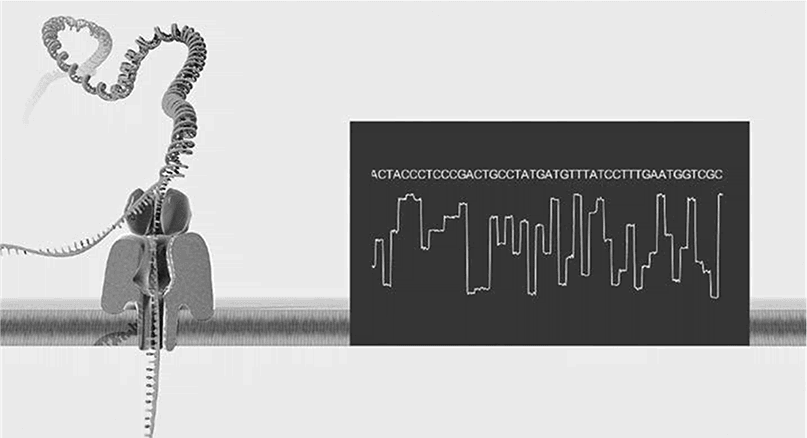
Замечательный прибор-секвенатор от компании Oxford Nanopore. Фермент расплетает двойную спираль, и одиночная нить ДНК, извиваясь, проходит сквозь центральную пору бактериального нанопорного белка. Анализ флуктуаций электрического тока позволяет идентифицировать конкретные основания, проникающие через пору

Секвенатор сильно уменьшился: Oxford Nanopore планирует запустить производство прибора SmidgION, который буквально вставляется в смартфон, как флешка
Возможно, наиболее революционное достижение оксфордской технологии – сам прибор. Это крошечное мобильное устройство не больше смартфона, которое подключается к ноутбуку через обычный USB-кабель.
Качественно подготовленный образец ДНК помещают в маленький приемник (нишу в устройстве), откуда биоматериал поступает в камеру с нанопорами. Каждая нанопора находится в центре специальной зоны в этом устройстве, как горошина посреди футбольного поля. Единственного устройства MinION, конечно, недостаточно для секвенирования целого человеческого генома, но благодаря мобильности и удобству применения этого устройства для него открываются новые рынки и области прикладного использования: от полевой исследовательской работы и прогнозирования до изучения инфекционных заболеваний и применения в школах. Так, MinION применяли в Гвинее (Западная Африка) для изучения вспышек вируса Эболы, в Бразилии для контроля эпидемии вируса Zika, а также на Международной космической станции для анализа штаммов микроорганизмов в режиме реального времени. Компания планирует создать обширную облачную базу данных, информация в которую поступает с мобильных секвенаторов ДНК. Браун намерен «сломить редуты медицинских и страховых компаний, после чего миллионы людей смогут свободно обмениваться генетической информацией, создавая виртуальные рекомбинации и так называемых виртуальных интернет-существ».
Спустя годы ожиданий может показаться, что генетическое сообщество весьма скептически воспринимает перспективы новых технологий. Когда в 2014 году исследователь из Броудовского института предъявил первые общедоступные данные, сгенерированные при помощи оксфордской технологии MinION, аудитория явно не впечатлилась. Однако, пока коллеги с нетерпением дожидались дальнейшего повышения точности и производительности этой технологии, я с восхищением отметил, что теперь, с новой технологией, мы обрели возможность определять генетическиепоследовательности в реальном времени, читая код жизни по обычным флуктуациям тока. Да, предстоит еще долгая работа, но я верю, что эта технология – либо некая ее альтернатива, например работа с искусственными нанопорами, вытравленными на кремниевых пластинах, – будет следующим большим прорывом в секвенировании.

Инга Моралес из Университета Сан-Паулу, охотница за вирусами, закладывает образец в портативный секвенатор ДНК, занимаясь проектом ZiBRA (анализ на бразильский вирус Zika в реальном времени)
В 2010 году в Колд-Спринг-Харборе состоялась конференция по персонализированной геномике, где мы познакомились с молодым человеком по имени Боги Элиазен, у которого были наполеоновские планы: секвенировать геномы всех своих соотечественников. Родом он с небольшого архипелага, численность населения которого всего 50 тысяч человек, и генетической меккой эта территория пока не считается. Я был заинтригован.
Фарерские острова – это группа из одиннадцати живописных островов в Северном море; архипелаг расположен примерно на полпути между Шотландией и Исландией. Цель проекта FarGen, основным устроителем которого стал Элиасен, заключается в секвенировании геномов всех фарерцев, что должно быть полезно для медицинского обслуживания проживающего населения. Эти данные не будут предоставляться гражданам – их станут вносить в медицинские карты, которыми смогут пользоваться врачи.
С тех пор было анонсировано еще несколько амбициозных национальных геномных проектов, в том числе Саудовская программа по секвенированию генома человека и программа Genomics England, финансируемая британским правительством. Каждая из подобных программ нацелена на то, чтобы секвенировать по 100 тысяч геномов произвольно отобранных индивидов. «Великобритания станет первой страной, которая внедрит эту технологию в основную систему здравоохранения и возглавит глобальную гонку за более качественные анализы, препараты и – самое главное – за персонализированный уход, что поможет спасать человеческие жизни», – обещал министр здравоохранения Джереми Хант.
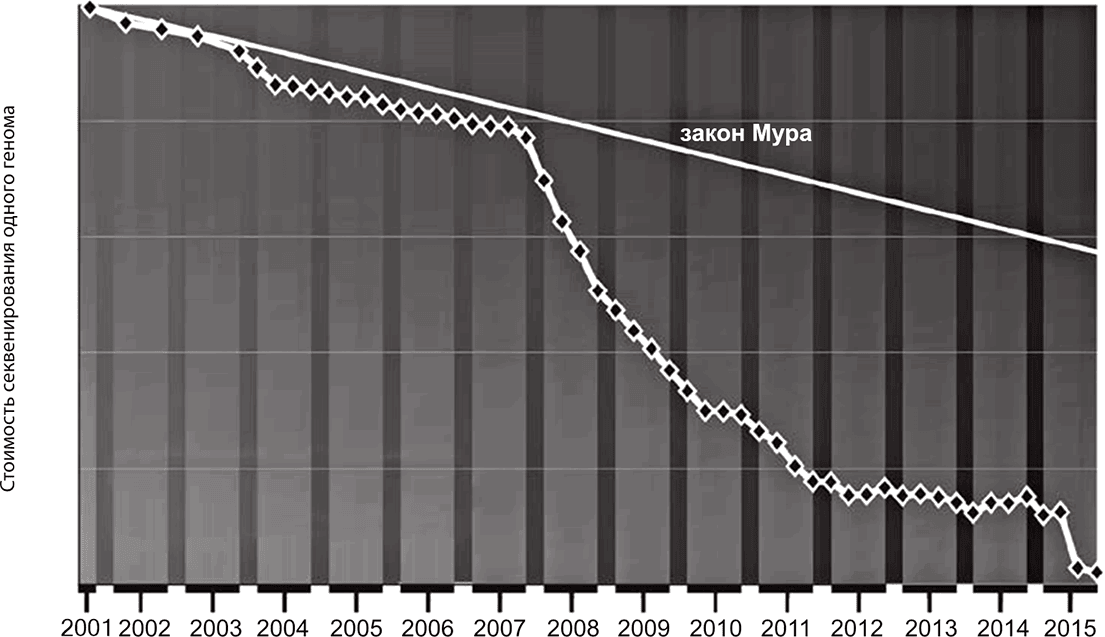
Значительное (на порядки) удешевление секвенирования человеческого генома с 2007 года (коммерческий запуск секвенирования нового поколения) до наших дней. Уже достигнута контрольная точка в 1000 долларов, а в ближайшие годы процедура может стать даже еще дешевле. Технологии секвенирования развиваются настолько быстро, что давно не подчиняются закону Мура (сплошная линия). Так называется знаменитая закономерность, указанная сооснователем компании Intel Гордоном Муром, согласно которой вычислительная мощность компьютеров, доступных за конкретную сумму, должна удваиваться примерно каждые два года
Проекты по секвенированию геномов в больших популяциях не могли не заинтересовать и представителей частного сектора экономики. Крейг Вентер, который (как ни странно) около десяти лет оставался невостребованным в области геномики, вернулся в высшую лигу во главе новой компании Human Longevity, стартовый инвестиционный капитал которой составил 70 миллионов долларов. Цель проекта, по утверждению Вентера, – идентифицировать ключевые варианты ДНК, обеспечивающие здоровье и долголетие; для этого были отсеквенированы геномы сотен пациентов, в том числе страдавших болезнью Альцгеймера. Забавно, что, как и во времена компании Celera, Вентер сулит, что часть этой информации может представлять ценность для фармацевтических компаний. Однако времена изменились: секвенирование геномов стремительно превращается в повседневную практику, и сложно вообразить, как единственная компания могла бы обеспечить себе монополию на всю такую информацию. Кроме того, кажется вполне логичным (если не сказать – неизбежным), что в большинстве фармацевтических компаний секвенирование геномов скоро станет неотъемлемой частью процесса этапа клинических исследований и тем самым средством, которое позволит отсортировать добровольцев на группы, где препарат был эффективен и где нет, с целью анализа механизмов действия каждого нового фармацевтического средства.
В начале этой главы я вспоминал, как около десяти лет назад мой геном отсеквенировали примерно за один миллион долларов. Сегодня такие компании, как Veritas Genetics, предлагают персонализированное секвенирование генома и интерпретацию данных за 1000 долларов, с дополнительной консультацией врача. В январе 2017 года новый генеральный директор компании Illumnia Френсис де Суза продемонстрировал новейший прибор для секвенирования, разработанный в их организации. Прибор называется NovaSeq, и уже через несколько лет он скорее всего сможет обеспечить секвенирование генома всего за 100 долларов. В будущем нас, несомненно, ждет повсеместное распространение геномики и получение информации о геноме в режиме реального времени, что реорганизует всю сферу здравоохранения и персонального медицинского ухода. Пока это лишь отдаленная перспектива. У нас в организме находится не только геном любой из соматических клеток, прослеживаемый вплоть до оплодотворенной яйцеклетки, из которой развился каждый человек; кроме того, человеческий организм содержит миллиарды микроорганизмов, и у каждого свой геном. Совокупность этих микробов может составлять от одного до трех процентов массы нашего тела, и от тонкого баланса этой микрофлоры может зависеть многое: реализация аутоиммунных реакций, риск развития ожирения, некоторые психические расстройства, связанные с уровнем нейромедиаторов (на уровень нейромедиаторов также может влиять состояние нашей кишечной микробиоты). Каждый день подтверждается, что так называемый микробиом (собирательный термин, означающий совокупность геномов триллионов бактерий, живущих у нас на коже, во рту, в кишечнике и в других полостях) влияет на наше здоровье гораздо сильнее, чем можно было бы предположить. В самом деле, по сравнению с имеющейся у нас бактериальной ДНК объем человеческой ДНК просто ничтожен. Возможно, нам не удастся полностью реализовать потенциал геномики для улучшения качества жизни, пока не будут учтены все ДНК, которые для нас, строго говоря, чужеродны, но необходимы для нашей жизни. Если трактовать секвенирование в таком контексте, оно никогда не станет ни молниеносно быстрым, ни слишком дешевым.
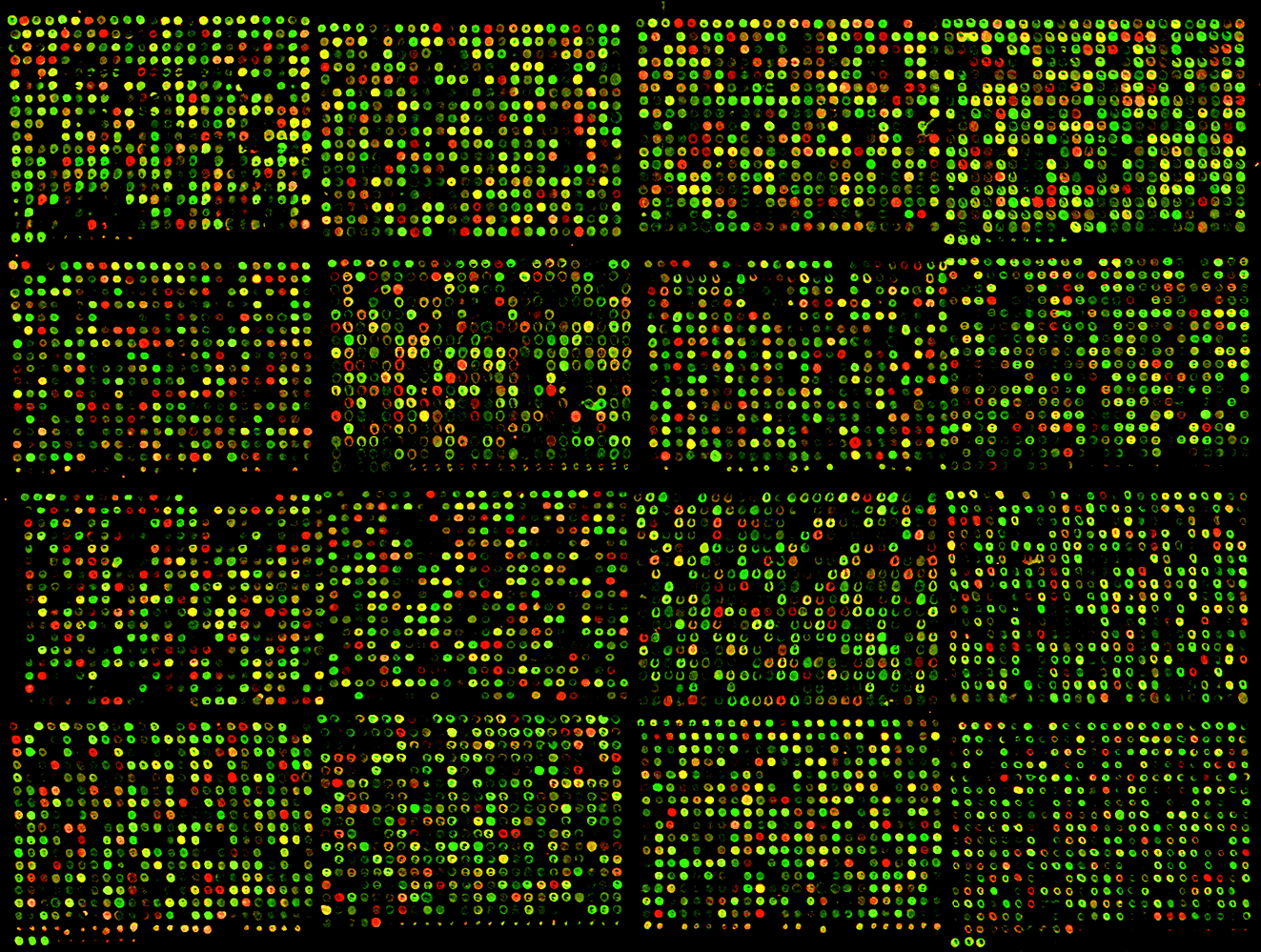
За пределами генома: микроматричный анализ молекулярного «переключения» генов. Здесь каждая точка соответствует одному из шести тысяч различных генов Plasmodium falciparum, микроорганизма, который является причиной тяжелейшей формы малярии. Для поиска эффективных лекарств или вакцины от этого заболевания необходимо выяснить, какие гены активны на разных этапах жизненного цикла плазмодия. Красным цветом обозначены гены, активные лишь в первой фазе, а не во второй, а зеленым – активные во второй фазе, но не в первой. Гены, активные в обеих фазах, обозначены желтым цветом

