Книга: Медицинская микробиология, иммунология и вирусология
Назад: Глава 66 Риккетсии, ориенции, коксиеллы, эрлихии, бартонеллы, хламидии и вызываемые ими болезни
Дальше: Глава 68 Патогенные актиномицеты и нокардии
Глава 67
Патогенные микоплазмы
Микоплазмы – уникальная группа мелких плеоморфных широко распространенных в природе грамотрицательных микроорганизмов, отличающихся от остальных бактерий полным отсутствием клеточной стенки. Впервые с этой группой мельчайших бактерий столкнулся Л. Пастер, изучая плевропневмонию крупного рогатого скота. Его возбудитель имеет настолько малые размеры, что он не виден под микроскопом, к тому же он не растет на обычных питательных средах, поэтому Л. Пастеру не удалось его выделить. Лишь в 1898 г. Е. Нокар и Э. Ру, используя сложную питательную среду, смогли получить культуру возбудителя плевропневмонии, а в 1931 г. У. Эльфорд с помощью бактериальных фильтров определил размеры этого микроорганизма – 125 – 150 нм.
Аналогичные микроорганизмы были выделены из различных источников внешней среды, из многочисленных животных, а также из организма человека при различных заболеваниях. Ввиду их сходства с возбудителем плевропневмонии рогатого скота их стали называть организмами, подобными ему – PPLO (pleuropneumoniaelike organisms). Оказалось, что к группе PPLO относится и агент Итона – возбудитель атипичной пневмонии человека, обнаруженный М. Итоном в 1942 г. В связи с тем, что эти микроорганизмы существенно отличаются от других бактерий мелкими размерами и отсутствием клеточной стенки, они были выделены в отдельную группу. Название «микоплазмы» было предложено в 1929 г. К. Новаком, оно подчеркивает их пластичность и то, что они имеют гомогенную консистенцию, «не дифференцирующуюся на экто– и эндоплазму».
У микоплазм нет клеточной стенки. Они не способны синтезировать предшественников пептидогликана (мураминовую и диаминопимелиновую кислоты) и окружены лишь тонкой трехслойной мембраной толщиной 7,5 – 10,0 нм. Поэтому их выделили в особый класс Mollicutes («нежная кожа»), семейство Mycoplasmataceae. К этому семейству относятся патогенные микоплазмы (вызывают заболевания у людей, зверей и птиц), условно-патогенные (очень часто бессимптомными носителями их являются культуры клеток) и микоплазмы-сапрофиты. Микоплазмы – наиболее мелкие и просто организованные прокариоты, способные к автономному размножению, а минимальные элементарные тельца, например Acholeplasma laidlawii, по размерам сопоставимы с минимальной исходной клеткой-прогенотой. Согласно теоретическим расчетам, простейшая гипотетическая клетка, способная автономно размножаться, должна иметь диаметр около 500 ангстрем, содержать ДНК с м. м. 360 000 Д и около 150 макромолекул. Элементарное тельце A. laidlawii имеет диаметр около 1000 ангстрем, т. е. всего в 2 раза больше, чем гипотетическая клетка, содержит ДНК с м. м. 2 880 000 Д, т. е. осуществляет гораздо больше метаболических процессов, и содержит не 150, а около 1200 макромолекул. Можно полагать, что микоплазмы являются наиболее близкими потомками исходных прокариотных клеток.
Размер генома у микоплазм – самый маленький для прокариот, например у членов семейства Mycoplasmataceae он составляет 0,45 МД. В связи с этим микоплазмы имеют целый ряд особенностей: очень малые размеры (100 – 450 нм), благодаря чему многие микоплазмы могут проходить (фильтроваться) через бактериальные фильтры; наличие минимальных количеств органелл (цитоплазматическая мембрана, нуклеоид, рибосомы); отсутствие многих биосинтетических процессов, имеющихся у других бактерий; малые размеры колоний, образующихся на плотных средах (0,1 – 0,6 мм); нечувствительность к бета-лактамным антибиотикам и другим агентам, угнетающим синтез клеточной стенки (из-за ее отсутствия); плеоморфизм, высокая осмотическая чувствительность. Характерно для большинства микоплазм также сравнительно низкое суммарное содержание Г + Ц в ДНК (от 23 – 35 мол % – у некоторых видов, до 39 – 46 мол % – у других). Морфология их различна – шаровидные, вакуолизированные, нитевидные (нередко ветвящиеся), гранулярные (элементарные тельца) структуры. Обычно неподвижные, но некоторые виды обладают скользящей подвижностью. Размножаются путем бинарного поперечного деления шаровидных и нитевидных (фрагментация) клеток, почкования и высвобождения множества элементарных телец, образующихся в нитях. Большинство видов микоплазм для роста нуждаются в стеролах и включают их непосредственно в свою трехслойную мембрану, которая состоит главным образом из липидов и белков. Поэтому микоплазмы являются паразитами мембран эукариотных клеток и способны длительное время персистировать на мембранах различных клеток человека, млекопитающих, птиц, рыб, моллюсков, насекомых и растений.
Микоплазмы размножаются на бесклеточных питательных средах, но для своего роста большинство из них нуждается в холестерине, который является уникальным компонентом их мембраны (даже у микоплазм, не требующих для своего роста стеролов), в жирных кислотах и нативном белке. Для выделения культур могут быть использованы жидкие и плотные питательные среды. Рост в жидких средах сопровождается едва видимым помутнением, на плотных средах с дрожжевым экстрактом и лошадиной сывороткой формирование колоний происходит следующим образом (рис. 110). В связи с их малыми размерами и отсутствием ригидной клеточной стенки микоплазмы способны проникать с поверхности агара и размножаться внутри его – в промежутках между нитями агара. При нанесении капли материала, содержащего микоплазмы, она проникает через имеющуюся на поверхности агара водную пленку и адсорбируется агаром, образуя небольшое уплотнение между его нитями. В результате размножения микоплазм, приблизительно через 18 ч, внутри сплетенных нитей агара формируется маленькая сферическая колония под поверхностью агара; она растет и через 24 – 48 ч инкубации достигает поверхностной водной пленки, в результате чего образуются две зоны роста – мутный гранулярный центр, врастающий в среду, и плоская ажурная полупросвечивающая периферическая зона (вид глазуньи). Колонии мелкие, диаметром от 0,1 до 0,6 мм, но могут быть и меньшего (0,01 мм) и большего (4,0 мм) диаметра. На кровяном агаре очень часто вокруг колоний наблюдаются зоны гемолиза, обусловленного действием образующейся Н2О2. Колонии некоторых видов микоплазм способны адсорбировать на своей поверхности эритроциты, эпителиальные клетки различных животных, клетки культур тканей, сперматозоиды человека и некоторых животных. Адсорбция лучше происходит при 37 °C, менее интенсивно – при 22 °C и специфически угнетается антисыворотками. Температурный оптимум для роста микоплазм 36 – 37 °C (диапазон 22 – 41 °C), оптимальная рН 7,0 или слегка кислая, или слегка щелочная. Большинство видов – факультативные анаэробы, хотя лучше растут в аэробных условиях, некоторые виды – аэробы; немногие лучше растут в анаэробных условиях. Микоплазмы неподвижны, но отдельные виды обладают скользящей активностью; являются хемоорганотрофами, в качестве главного источника энергии используют либо глюкозу, либо аргинин, редко – оба вещества, иногда – ни то, ни другое. Они способны ферментировать галактозу, маннозу, гликоген, крахмал с образованием кислоты без газа; протеолитическими свойствами не обладают, лишь некоторые виды разжижают желатин и гидролизуют казеин. Антигенная специфичность микоплазм определяется антигенами цитоплазматической мембраны, в частности содержащимися в ней белками и гликопротеидами. Микоплазмы обладают родо-, видо– и типоспецифическими антигенами. Кроме того, они могут иметь антигены, общие с антигенами мембран клеток-хозяев или включают их в результате длительной персистенции на мембранах этих клеток, что может стать причиной антигенной мимикрии и привести к развитию аутоиммунной патологии.
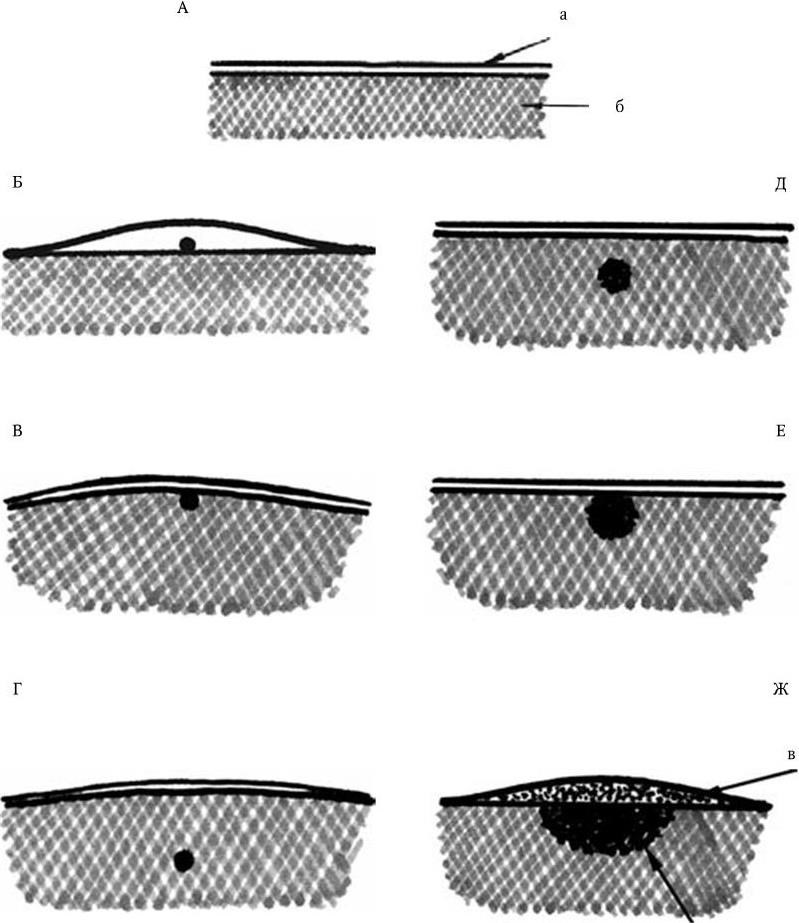
Рис. 110. Формирование колонии микоплазмы на плотной среде (Прокариоты. 1981, т. II):
А. Вертикальный срез агара перед посевом (а – пленка воды, б – нити агара).
Б. Капля, содержащая жизнеспособные микоплазмы, нанесена на поверхность агара.
В. Через 15 мин после посева капля адсорбирована агаром.
Г. Приблизительно через 3–6 ч после посева. Жизнеспособная частица проникла в агар.
Д. Приблизительно через 18 ч после посева. Маленькая сферическая колония сформировалась ниже поверхности агара.
Е. Приблизительно через 24 ч после посева. Колония достигла поверхности агара.
Ж. Приблизительно через 24–48 ч после посева. Колония достигла свободной водной пленки, образуя периферическую зону (г – центральная зона, в – периферическая зона колонии)
Резистентность. Из-за отсутствия клеточной стенки микоплазмы более чувствительны, чем другие бактерии, к воздействию механических, физических и химических факторов (УФ-облучению, действию прямых солнечных лучей, рентгеновскому облучению, изменению рН среды, к действию высокой температуры, высушиванию). При нагревании до 50 °C погибают в течение 10 – 15 мин, очень чувствительны к обычным химическим дезинфектантам.
Семейство микоплазм насчитывает более 100 видов. Человек является естественным носителем не менее 13 видов микоплазм, которые вегетируют на слизистых оболочках глаза, дыхательных, пищеварительных и мочеполовых путей. В патологии человека наибольшую роль играют несколько видов Mycoplasma: M. pneumoniae, M. hominis, M. arthritidis, M. fermentans и, возможно, M. genitalium, и единственный вид рода Ureaplasma – U. urealyticum. Основное биохимическое отличие последнего от видов Mycoplasma заключается в том, что U. urealyticum обладает уреазной активностью, которой лишены все члены рода Mycoplasma (табл. 52).
Таблица 52
Дифференциальные признаки некоторых патогенных для человека микоплазм
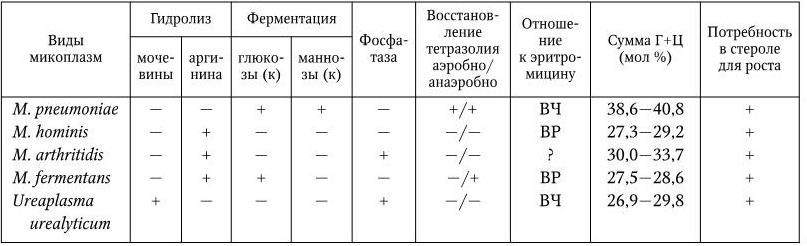
Примечание. (к) – образование кислоты; ВР – высокорезистентны; ВЧ – высокочувствительны; (+) – признак положительный; ( – ) – признак отрицательный.
Патогенные для человека микоплазмы вызывают у него заболевания (микоплазмозы) дыхательных, мочеполовых путей и суставов с разнообразными клиническими проявлениями.
Респираторный микоплазмоз
Респираторный микоплазмоз имеет глобальное распространение. По данным ВОЗ (1985), ежегодно болеет 8 – 15 млн человек. Очень часто протекает в виде острой пневмонии (сегментарной, очаговой или интерстициальной). Основной возбудитель – M. pneumoniae, значительно реже – M. hominis, и очень редко заболевание дыхательных путей у детей в возрасте до 1 года вызывает U. urealyticum.
M. pneumoniae. Основные биологические и морфологические свойства типичны для рода Mycoplasma, однако имеется ряд отличительных признаков. По форме это короткие нити длиной 2 – 5 мкм, клетки обладают скользящей подвижностью. Размножаются путем бинарного деления и высвобождения элементарных телец из нитей. Свежеизолированные колонии часто лишены полупрозрачной периферической зоны, а имеют вид приподнятой кольцевидной гранулярной структуры диаметром 30 – 100 мкм. Растут медленнее, чем другие микоплазмы. Колонии появляются через 5 – 10 дней инкубации, иногда позднее. Требуется несколько последовательных пересевов, чтобы колонии приобрели вид «глазуньи». Колонии на плотной среде адсорбируют эритроциты, трахеальные эпителиальные клетки обезьян, крыс, морских свинок, кур, клетки некоторых культур (HeLa, куриных эмбриональных тканей и др.), а также сперматозоиды человека и быков. Рецепторы эритроцитов и эпителиальных клеток для M. pneumoniae разрушаются нейраминидазой; адсорбция клеток предотвращается, если микоплазмы обработать предварительно нейраминовой кислотой. M. pneumoniae вызывает гемагглютинацию эритроцитов человека и животных, обладает гемолитической активностью, обусловленной продукцией Н2О2; митогенным действием в отношении Т– и В-лимфоцитов и цитотоксическим действием; высокочувствительна к эритромицину. В антигенном отношении вид M. pneumoniae представляет собой однородную группу, типоспецифических антигенов не обнаружено.
Резистентность к действию физических и химических факторов невелика.
Факторы патогенности: высокое сродство к эпителиальным клеткам дыхательных путей, гемадсорбционные, гемолитические, цитотоксические свойства микоплазм, их подвижность.
Эпидемиология. Источником инфекции является больной человек, а также носители, в том числе перенесшие болезнь в бессимптомной форме. Заражение происходит воздушно-капельным путем, так как возбудитель локализуется главным образом на клетках реснитчатого эпителия дыхательных путей. Респираторный микоплазмоз – малоконтагиозное заболевание, что объясняется кратковременным сроком выживания возбудителя во внешней среде, поэтому для заражения требуется тесное и длительное общение с источником инфекции. Этим и обусловливается более высокая заболеваемость в организованных коллективах, в особенности во вновь организованных, где через 2 – 3 мес. заражается до 50 % его членов. Болеют чаще лица в возрасте от 1 года до 30 лет.
Патогенез и клиника. Инкубационный период длится 7 – 14 дней, иногда до 25 дней. Возбудитель адсорбируется на слизистой оболочке верхних дыхательных путей, размножается и активно распространяется по слизистой оболочке трахеи и бронхов, достигает альвеолоцитов, внедряется в межальвеолярные перегородки. В результате повреждения клеток возникают перибронхиальные, периваскулярные и интерстициальные инфильтраты. Для микоплазменной пневмонии, которая развивается обычно постепенно, типичен сухой или со скудной мокротой длительный изнуряющий кашель; физикальные изменения в легких выражены слабо или отсутствуют, поэтому пневмония выявляется при рентгенологическом исследовании. Воспалительные инфильтраты рассасываются медленно – в течение 3 – 4 нед., иногда дольше. У детей раннего возраста нередко наблюдается двустороннее поражение легких. Течение болезни, как правило, доброкачественное.
Постинфекционный иммунитет после острой инфекции сохраняется в течение 5 – 10 лет, иногда дольше. Он обусловлен как секреторными, так и гуморальными антимикробными антителами, а также сохраняющимися более продолжительный срок антителами, подавляющими метаболизм микоплазм, и клеточными элементами (макрофаги, Т-лимфоциты). После бессимптомных и стертых форм инфекции иммунитет кратковременный и слабо выражен.
Лабораторная диагностика. Поскольку атипические пневмонии имеют различную этиологию, решающая роль в их диагностике принадлежит лабораторным методам. Для диагностики респираторного микоплазмоза (микоплазменной пневмонии) используют бактериологические и серологические методы, а также выявление микоплазм и их идентификацию с помощью иммунологических приемов. Материалом для бактериологического исследования служат мокрота, слизь из глотки, плевральная жидкость, лаваж (франц. lavage – промывать), смывы с поверхности бронхиол и альвеолярных структур легких, полученные при бронхоскопии. Для получения культур посевы производят на среды, содержащие все необходимые для роста микоплазм питательные вещества. Для угнетения роста сопутствующих бактерий в питательную среду добавляют пенициллин и ацетат таллия, к которым M. pneumoniae устойчива. Выделенную культуру идентифицируют на основании морфологических, культуральных свойств, признаков, указанных в табл. 52, а также с помощью диагностических иммунных сывороток, полученных путем иммунизации кроликов препаратами цитоплазматических мембран M. pneumoniae.
Микоплазмы и их антигены могут быть обнаружены в исследуемом материале с помощью иммунофлуоресценции, РПГА, РАГА, ИФМ. Кроме того, для идентификации микоплазм используют еще 2 теста: угнетение роста и угнетение метаболизма, которые достигаются с помощью специфических антител.
Для серологической диагностики применяют РПГА, РСК, иммунофлуоресценцию, ИФМ с использованием специфической гликолипидной фракции мембран M. pneumoniae. Нарастание титра антител определяют в парных сыворотках. В качестве одного из ускоренных методов может быть использована и внутрикожная проба с аллергеном из M. pneumoniae. Для выявления M. pneumoniae разработана и предложена тест-система на основе ЦПР, позволяющая обнаружить носительство микоплазм даже в тех случаях, когда они не обнаруживаются никакими другими методами.
Лечение. При острой форме микоплазменной пневмонии наиболее эффективно применение эритромицина и тетрациклинов.
Профилактика. Неспецифическая профилактика такая же, как в отношении острых респираторных вирусных заболеваний. Для специфической профилактики разрабатываются инактивированные вакцины, химические вакцины (из антигенов цитоплазматической мембраны M. pneumoniae), а также живые вакцины из аттенуированных штаммов возбудителя.
Микоплазмы – возбудители урогенитальных заболеваний
Воспалительные болезни мочеполовой системы, такие как уретриты, циститы, гломерулонефриты, пиелонефриты, простатиты; у женщин – вагиниты, сальпингиты, кольпиты, цервициты, эндометриты, параметриты, этиологически очень часто связаны с микоплазмами, особенно с M. hominis и U. urealyticum. Этими видами микоплазм инфицировано не менее 50 % здоровых мужчин и женщин в возрасте 30 – 50 лет, причем до 30 % женщин являются носителями одновременно обеих микоплазм. Существует мнение, что уреаплазменная инфекция (уреаплазмоз) может быть причиной бесплодия: женского – вследствие воспалительных процессов гениталий; и мужского – в результате воздействия на сперматогенез и сперматозоиды (уреаплазмы адсорбируются на сперматозоидах, нарушают их подвижность и изменяют форму). Кроме того, M. hominis при внутриутробном заражении плода может быть причиной врожденных аномалий развития ребенка в связи с ее способностью воздействовать на хромосомы клетки.
M. hominis обычно имеет форму коротких нитей длиной 2 – 5 мкм, иногда до 30 мкм, не обладает протеолитической активностью, не восстанавливает ни тетразолия, ни метиленового синего ни в аэробных, ни в анаэробных условиях. В качестве источника энергии использует аргинин; глюкозу и маннозу не ферментирует. На плотных средах с дрожжевым экстрактом и лошадиной сывороткой образует характерные колонии типа «глазуньи», обладает гемолитическим действием, которое связано с продукцией Н2О2. Колонии на плотных средах адсорбируют клетки HeLa и клетки куриных эмбриональных тканей, но не адсорбируют эритроцитов и трахеальных эпителиальных клеток обезьян, крыс, морских свинок. Рецепторы на клетках HeLa и куриных фибробластах не разрушаются нейраминидазой. M. hominis высокорезистентны к эритромицину (минимальная бактериостатическая концентрация 500 – 1000 мкг/мл и выше). В антигенном отношении гетерогенны: различают 8 серотипов. В организме человека чаще всего паразитирует на слизистой оболочке нижних отделов мочеполовых путей (уретра, влагалище, шейка матки), реже – на слизистой оболочке зева и глотки.
Ureaplasma urealyticum. Первоначально в связи с очень маленькими колониями, которые они образуют (15 – 30 мкм в диаметре), были названы как Т-группа микоплазм (англ. tiny – мельчайшие). Но поскольку они отличаются от всех других видов микоплазм своей способностью гидролизовать мочевину, впоследствии были выделены в самостоятельный род Ureaplasma, представленный пока единственным видом U. urealyticum. Их морфология, ультраструктура и способ размножения такие же, как и у других микоплазм. Очевидно, мочевина, в дополнение к холестерину, является жизненно важным питательным веществом для этого вида микоплазм. Ее гидролиз сопровождается выделением аммиака. Глюкозу, маннозу и аргинин не потребляют, тетрозолия не восстанавливают, обладают протеолитической и фосфатазной активностью и вызывают гемолиз эритроцитов морской свинки. Высокочувствительны к эритромицину – минимальная ингибирующая доза 0,8 – 3,0 мкг/мл. На плотных средах образуют очень мелкие колонии, но на некоторых средах и более крупные, диаметром до 175 – 200 мкм. Хотя они обычно грубо гранулярные и не имеют или имеют едва заметный центральный бугорок, на соответствующих средах становятся гладкими и приобретают типичный вид «глазуньи». На дифференциально-диагностической среде А-7, содержащей кроме дрожжевого экстракта и лошадиной сыворотки мочевину и соли марганца, образуются псевдоколонии в виде коричневого преципитата непосредственно над колониями только Ureaplasma (но не других микоплазм). Псевдоколонии возникают в результате взаимодействия ионов Mn2+ c продуктами гидролиза уреаплазмой мочевины.
Температурный оптимум для роста 35 – 37 °C, оптимальная рН 6,0 – 6,5. Колонии на плотных средах, как правило, не адсорбируют эритроцитов человека и морской свинки. В антигенном отношении неоднородны: различают 8 серотипов штаммов человеческого происхождения и 8 серотипов животного происхождения. U. urealyticum обычно паразитирует на мембранах слизистой оболочки мочеполовой системы человека, а также крупного рогатого скота, собак и обезьян, иногда на слизистой оболочке зева и глотки человека и на слизистой оболочке зева и конъюнктиве крупного рогатого скота.
Роль M. genitalium в этиологии урогенитальных микоплазмозов требует выяснения.
Эпидемиология. Источник инфекции – инфицированный человек, в том числе, и очень часто, бессимптомный носитель микоплазм. Заражение происходит главным образом путем полового контакта. У инфицированных беременных женщин возможно внутриутробное заражение плода через околоплодные воды (возбудитель проникает восходящим путем из шейки матки), гематогенно или во время родов. При внутриутробном заражении поражаются органы дыхания, зрения, почки, печень, ЦНС, что может быть причиной гибели плода. Во время беременности уреаплазменная инфекция нередко активизируется и может также стать причиной преждевременных родов и спонтанных абортов.
Лабораторная диагностика играет решающую роль в распознавании урогенитальных микоплазмозов. Это тем более важно, что среди людей широко распространено бессимптомное носительство этих условно-патогенных микроорганизмов. Используются главным образом бактериологический и серологический методы. Материалом для выделения возбудителей служат слизь из уретры и влагалища, секрет простаты, сперма, моча. Посевы производят на селективные для микоплазм питательные среды, а для роста U. urealyticum – обязательно с мочевиной. Выделенные культуры идентифицируют по морфологическим, культуральным и иным признакам (см. табл. 52). Кроме того, для их типирования используют реакции угнетения роста или метаболизма специфическими иммунными сыворотками. Для обнаружения микоплазм или их антигенов используют непрямую иммунофлуоресценцию, РПГА с антительным диагностикумом, ИФМ, реакции преципитации, РАГА. Для серологической диагностики также могут быть использованы ИФМ, РПГА, РАГА. Однако серологическая диагностика недостаточно надежна, так как нет четкой зависимости между титром специфических антител и присутствием возбудителя.
Лечение. Если возбудителем острой инфекции является U. urealyticum, наиболее эффективно применение эритромицина, в случае M. hominis – тетрациклинов.
Профилактика урогенитальной инфекции должна быть такой же, как и других венерических заболеваний. Целесообразна организация диспансерного учета больных и носителей микоплазм в группах повышенного риска (проститутки, гомосексуалисты). Особого внимания требуют женщины детородного возраста, которые страдают хроническими урогенитальными заболеваниями неясной этиологии, для предупреждения внутриутробного микоплазмоза.
Микоплазмы – возбудители артритов
Ревматоидным артритом болеют около 1 – 2,5 % населения Европы и Америки, и приблизительно у 60 – 80 % таких больных обнаруживаются различные виды микоплазм или их антигены. Это обстоятельство, а также воспроизведение заболевания, сходного с ревматоидным артритом, при экспериментальном заражении животных дают основание рассматривать микоплазмы как возможных возбудителей ревматоидного артрита. Однако многие вопросы, касающиеся этиологии, способа заражения и механизма патогенеза ревматоидного артрита, требуют изучения.
Из синовиальной жидкости и ткани суставов при ревматоидном артрите выделяют M. arthritidis, M. fermentans, M. pneumoniae и U. urealyticum, дифференциальные признаки их представлены в табл. 52. Отличительной особенностью M. arthritidis является также то, что они способны разжижать желатин, но не свертывают сыворотку, не гидролизуют казеин. Данных о способности их колоний адсорбировать эритроциты опубликовано не было. Гемолизин идентифицирован как Н2О2.
Источником возбудителя ревматоидного артрита является больной человек или бессимптомный носитель микоплазм.
Лабораторная диагностика основана на выделении возбудителя из синовиальной жидкости, ткани суставных хрящей и последующей его идентификации или на обнаружении возбудителя (его антигенов) в исследуемых биосубстратах и в сыворотке крови (в том числе в составе циркулирующих иммунных комплексов) с помощью иммунофлуоресценции, РСК, РПГА, РАГА и ИФМ.
Для диагностики заболеваний, вызываемых микоплазмами и хламидиями, все шире используется метод ЦПР. В России создана и применяется тест-система «Полимик», содержащая реагенты, в том числе праймеры, для обнаружения ДНК Chlamydia trachomatis, Mycoplasma hominis и Ureaplasma urealyticum в биологических пробах.
Назад: Глава 66 Риккетсии, ориенции, коксиеллы, эрлихии, бартонеллы, хламидии и вызываемые ими болезни
Дальше: Глава 68 Патогенные актиномицеты и нокардии

