Книга: Медицинская микробиология, иммунология и вирусология
Назад: Глава 61 Возбудители кишечных инфекций
Дальше: Глава 63 Листерии, легионеллы и вызываемые ими болезни
Глава 62
Возбудители капельных инфекций
Микробиология дифтерии
Дифтерия – острое инфекционное заболевание преимущественно детского возраста, которое проявляется глубокой интоксикацией организма дифтерийным токсином и характерным фибринозным воспалением в месте локализации возбудителя. Название болезни происходит от греческого слова diphthera – кожа, пленка, так как в месте размножения возбудителя образуется плотная, серовато-белого цвета пленка.
Возбудитель дифтерии – Corynebacterium diphtheriae – был обнаружен впервые в 1883 г. Э. Клебсом в срезах из пленки, получен в чистой культуре в 1884 г. Ф. Леффлером. В 1888 г. Э. Ру и А. Иерсен обнаружили его способность продуцировать экзотоксин, играющий главную роль в этиологии и патогенезе дифтерии. Получение в 1892 г. антитоксической сыворотки Э. Берингом и использование ее с 1894 г. для лечения дифтерии позволило значительно снизить летальность. Успешное наступление на эту болезнь началось после 1923 г. в связи с разработкой Г. Рамоном метода получения дифтерийного анатоксина.
Возбудитель дифтерии относится к роду Corynebacterium (класс Actinobacteria). В морфологическом отношении характеризуется тем, что клетки булавовидно утолщены на концах (греч. coryne – булава), образуют ветвление, особенно в старых культурах, и содержат зернистые включения.
Установлена этиологическая роль коринебактерий, не относящихся к коринебактерии дифтерии, так называемых Corynebacterium non diphtheriae, которые способны вызывать не только заболевания верхних дыхательных путей, но и отиты, эндокардиты, бронхиты, пневмонии, уретриты, пиелонефриты и др. Возбудителями таких заболеваний чаще всего бывают Corynebacterium pseudodiphtheriticum, C. xerosis, C. pseudotuberculosis и C. urealyticum.
C. diphtheriae – прямые или слегка изогнутые неподвижные палочки длиной 1,0 – 8,0 мкм и диаметром 0,3 – 0,8 мкм, спор и капсул не образуют. Очень часто они имеют вздутия на одном или обоих концах, часто содержат метахроматические гранулы – зерна волютина (полиметафосфаты), которые при окрашивании метиленовым синим приобретают голубовато-пурпурный цвет. Для их обнаружения предложен особый метод окрашивания по Нейссеру. При этом палочки окрашиваются в соломенно-желтый, а зерна волютина – в темно-коричневый цвет, и располагаются обычно по полюсам (см. цв. вкл., рис. 102.2 и 3). C. diphtheriae хорошо окрашивается анилиновыми красителями, грамположительна, но в старых культурах нередко обесцвечивается и имеет отрицательную окраску по Граму. Для нее характерен выраженный полиморфизм, особенно в старых культурах и под влиянием антибиотиков (см. рис. 102.1). Содержание Г + Ц в ДНК около 60 мол %.
Дифтерийная палочка является аэробом или факультативным анаэробом, температурный оптимум для роста 35 – 37 °C (границы роста 15 – 40 °C), оптимальная рН 7,6 – 7,8. К питательным средам не очень требовательна, но лучше растет на средах, содержащих сыворотку или кровь. Избирательными для дифтерийных бактерий являются свернутые сывороточные среды Ру или Леффлера, рост на них появляется через 8 – 12 ч в виде выпуклых, величиной с булавочную головку колоний серовато-белого или желтовато-кремового цвета. Поверхность их гладкая или слегка зернистая, на периферии колонии несколько более прозрачные, чем в центре. Колонии не сливаются, вследствие чего культура приобретает вид шагреневой кожи. На бульоне рост проявляется в виде равномерного помутнения, либо бульон остается прозрачным, а на его поверхности образуется нежная пленка, которая постепенно утолщается, крошится и хлопьями оседает на дно.
Особенностью дифтерийных бактерий является их хороший рост на кровяных и сывороточных средах, содержащих такие концентрации теллурита калия, которые подавляют рост других видов бактерий. Это связано с тем, что C. diphtheriae восстанавливают теллурит калия до металлического теллура, который, откладываясь в микробных клетках, придает колониям характерный темно-серый или черный цвет. Применение таких сред повышает процент высеваемости дифтерийных бактерий (рис. 103).
C. diphtheriae ферментируют глюкозу, мальтозу, галактозу с образованием кислоты без газа, но не ферментируют (как правило) сахарозу, имеют цистиназу, не имеют уреазы и не образуют индола. По этим признакам они отличаются от тех коринеформных бактерий (дифтероидов), которые чаще других встречаются на слизистой оболочке глаза (C. xerosus) и носоглотки (C. pseudodiphtheriticum) и от других дифтероидов (табл. 44).
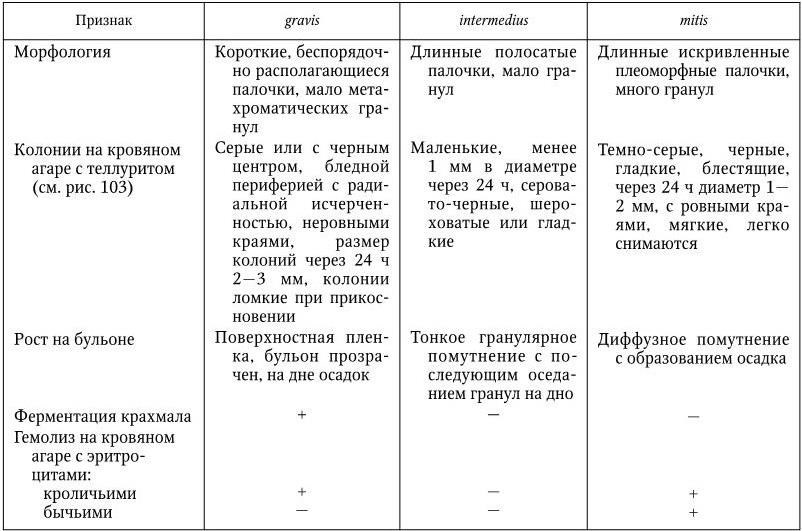
В природе существуют три основных варианта (биотипа) дифтерийной палочки: gravis, intermedius и mitis. Они различаются по морфологическим, культуральным, биохимическим и другим свойствам (табл. 45).
Деление дифтерийных бактерий на биотипы было произведено с учетом того, при каких формах течения дифтерии у больных они выделяются с наибольшей частотой. Тип gravis чаще выделяется от больных с тяжелой формой дифтерии и вызывает групповые вспышки. Тип mitis вызывает более легкие и спорадические случаи заболеваний, а тип intermedius занимает промежуточное положение между ними. C. belfanti, ранее относимый к биотипу mitis, выделен в самостоятельный, четвертый, биотип. Его главное отличие от биотипов gravis и mitis – способность восстанавливать нитраты в нитриты. Штаммы C. belfanti обладают выраженными адгезивными свойствами, и среди них обнаруживаются как токсигенные, так и нетоксигенные варианты.
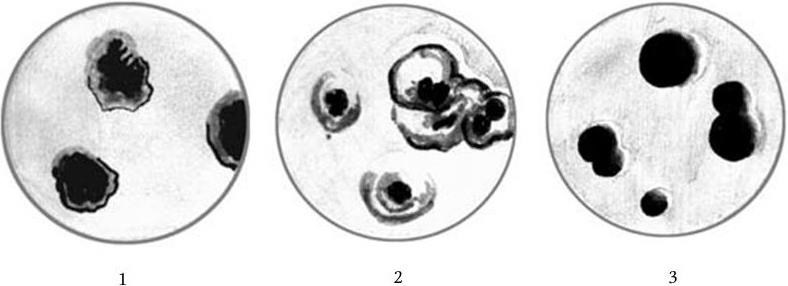
Рис. 103. Рост биотипов Corynebacterium diphtheriae на среде с теллуритом:
1 – gravis; 2 – intermedius; 3 – mitis
Таблица 44
Дифференциальные признаки, отличающие C. diphtheriae от некоторых дифтероидов
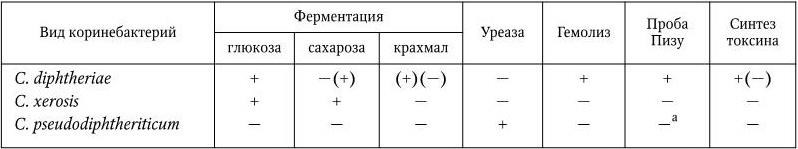
Примечание.(+) – признак положительный; ( – ) – признак отрицательный; (+)( – ) – признак иногда положительный, иногда отрицательный; а – проба Пизу выявляет наличие цистиназы.
Таблица 45
Дифференциальные признаки биотипов gravis, intermedius и mitis
Антигенная структура коринебактерий очень гетерогенна и мозаична. У возбудителей дифтерии всех трех типов обнаружено несколько десятков соматических антигенов, по которым их делят на серотипы. В России принята серологическая классификация, по которой различают 11 серотипов дифтерийных бактерий, из них 7 основных (1 – 7) и 4 дополнительных, редко встречающихся серотипов (8 – 11). Шесть серотипов (1, 2, 3, 4, 5, 7) относятся к типу gravis, а пять (6, 8, 9, 10, 11) – к типу mitis. Недостатком метода серотипирования является то, что многие штаммы, особенно нетоксигенные, обладают спонтанной агглютинацией или полиагглютинабельностью.
Фаготипирование C. diphtheriae. Для дифференциации дифтерийных бактерий предложены различные схемы фаготипирования. По схеме М. Д. Крыловой с помощью набора из 9 фагов (A, B, C, D, F, G, H, I, K) удается типировать большинство токсигенных и нетоксигенных штаммов типа gravis. С учетом чувствительности к указанным фагам, а также культуральных, антигенных свойств и способности синтезировать корицины (бактерицидные белки) М. Д. Крылова выделила 3 самостоятельные группы коринебактерий типа gravis (I – III). В каждой из них имеются подгруппы токсигенных и их нетоксигенных аналогов возбудителей дифтерии.
Резистентность возбудителей дифтерии. C. diphtheriae проявляет большую устойчивость к низким температурам, но быстро погибает при высокой температуре: при 60 °C – в течение 15 – 20 мин, при кипячении – через 2 – 3 мин. Все дезинфицирующие вещества (лизол, фенол, хлорамин и др.) в обычно применяемой концентрации уничтожают ее за 5 – 10 мин. Однако возбудитель дифтерии хорошо переносит высушивание и может долго сохранять жизнеспособность в высохшей слизи, слюне, в частичках пыли. В мелкодисперсном аэрозоле дифтерийные бактерии сохраняют жизнеспособность в течение 24 – 48 ч.
Факторы патогенности. Патогенность C. diphtheriae определяется наличием ряда факторов:
1. Факторов адгезии, колонизации и инвазии. Структуры, ответственные за адгезию, не идентифицированы, однако без них дифтерийная палочка не смогла бы колонизировать клетки. Их роль выполняют какие-то компоненты клеточной стенки возбудителя. Инвазивные свойства возбудителя связаны с гиалуронидазой, нейраминидазой и протеазой.
2. Токсического гликолипида, содержащегося в клеточной стенке возбудителя. Он представляет собой 6,6'-диэфир трегалозы, содержащий коринемиколовую кислоту (С32Н64О3) и коринемиколиновую кислоту (С32Н62О3) в эквимолярных отношениях (трегалозо-6,6'-дикоринемиколат). Гликолипид оказывает разрушающее действие на клетки ткани в месте размножения возбудителя.
3. Экзотоксина, обусловливающего патогенность возбудителя и характер патогенеза заболевания. Нетоксигенные варианты C. diphtheriae дифтерии не вызывают.
Экзотоксин синтезируется в виде неактивного предшественника – единой полипептидной цепи с м. м. 61 кД. Его активация осуществляется собственной бактериальной протеазой, которая разрезает полипептид на два связанные между собой дисульфидными связями пептида: А (м. м. 21 кД) и В (м. м. 39 кД). Пептид В выполняет акцепторную функцию – он распознает рецептор, связывается с ним и формирует внутримембранный канал, через который проникает в клетку пептид А и реализует биологическую активность токсина. Пептид А представляет собой фермент АДФрибозилтрансферазу, который обеспечивает перенос аденозиндифосфатрибозы из НАД на один из аминокислотных остатков (гистидина) белкового фактора элонгации EF-2. В результате модификации EF-2 утрачивает свою активность, и это приводит к подавлению синтеза белка рибосомами на стадии транслокации. Токсин синтезируют только такие C. diphtheriae, которые несут в своей хромосоме гены умеренного конвертирующего профага. Оперон, кодирующий синтез токсина, является моноцистронным, он состоит из 1,9 тыс. пар нуклеотидов и имеет промотор toxP и 3 участка: toxS, toxA и toxB. Участок toxS кодирует 25 аминокислотных остатков сигнального пептида (он обеспечивает выход токсина через мембрану в периплазматическое пространство бактериальной клетки), toxA – 193 аминокислотных остатка пептида А, и toxB – 342 аминокислотных остатка пептида В токсина. Утрата клеткой профага или мутации в tox-опероне делают клетку малотоксигенной. Напротив, лизогенизация нетоксигенных C. diphtheriae конвертирующим фагом превращает их в токсигенные бактерии. Это доказано однозначно: токсигенность дифтерийных бактерий зависит от лизогенизации их конвертирующими tox-коринефагами. Коринефаги интегрируются в хромосому коринебактерий с помощью механизма сайт-специфической рекомбинации, причем штаммы дифтерийных бактерий могут содержать в своих хромосомах по 2 сайта рекомбинации (attB), и коринефаги интегрируются в каждый из них с одинаковой частотой.
Генетический анализ ряда нетоксигенных штаммов дифтерийных бактерий, проведенный с помощью меченых ДНК-зондов, несущих фрагменты tox-оперона коринефага, показал, что в их хромосомах имеются последовательности ДНК, гомологичные tox-оперону коринефага, но они либо кодируют неактивные полипептиды, либо находятся в «молчащем» состоянии, т. е. неактивны. В связи с этим возникает очень важный в эпидемиологическом отношении вопрос: могут ли нетоксигенные дифтерийные бактерии превращаться в токсигенные в естественных условиях (в организме человека), подобно тому, как это происходит in vitro? Возможность подобного превращения нетоксигенных культур коринебактерий в токсигенные с помощью фаговой конверсии была показана в опытах на морских свинках, куриных эмбрионах и белых мышах. Однако происходит ли это в ходе естественного эпидемического процесса (и если происходит, то как часто), пока установить не удалось.
В связи с тем, что дифтерийный токсин в организме больных оказывает избирательное и специфическое воздействие на определенные системы (поражаются в основном симпатико-адреналовая система, сердце, сосуды и периферические нервы), то очевидно, он не только угнетает биосинтез белка в клетках, но и вызывает другие нарушения их метаболизма.
Для обнаружения токсигенности дифтерийных бактерий можно использовать следующие способы:
1. Биологические пробы на животных. Внутрикожное заражение морских свинок фильтратом бульонной культуры дифтерийных бактерий вызывает у них некроз в месте введения. Одна минимальная смертельная доза токсина (20 – 30 нг) убивает морскую свинку весом 250 г при подкожном введении на 4 – 5-й день. Наиболее характерным проявлением действия токсина является поражение надпочечников, они увеличены и резко гиперемированы (см. цв. вкл., рис. 102.4).
2. Заражение куриных эмбрионов. Дифтерийный токсин вызывает их гибель.
3. Заражение культур клеток. Дифтерийный токсин вызывает отчетливый цитопатический эффект.
4. Метод твердофазного иммуноферментного анализа с использованием меченных пероксидазой антитоксинов.
5. Использование ДНК-зонда для непосредственного обнаружения tox-оперона в хромосоме дифтерийных бактерий.
Однако наиболее простым и распространенным способом определения токсигенности дифтерийных бактерий является серологический – метод преципитации в геле. Суть его состоит в следующем. Полоску стерильной фильтровальной бумаги размером 1,5 × 8 см смачивают антитоксической противодифтерийной сывороткой, содержащей 500 АЕ в 1 мл, и наносят на поверхность питательной среды в чашке Петри. Чашку подсушивают в термостате 15 – 20 мин. Исследуемые культуры засевают бляшками по обе стороны от бумажки. На одну чашку засевают несколько штаммов, один из которых, заведомо токсигенный, служит контролем. Чашки с посевами инкубируют при 37 °C, результаты учитывают через 24 – 48 ч. Вследствие встречной диффузии в геле антитоксина и токсина в месте их взаимодействия образуется четкая линия преципитации, которая сливается с линией преципитации контрольного токсигенного штамма (см. рис. 73, с. 288). Полоски неспецифической преципитации (они образуются, если в сыворотке кроме антитоксина присутствуют в небольшом количестве другие антимикробные антитела) появляются поздно, выражены слабо и никогда не сливаются с полоской преципитации контрольного штамма.
Эпидемиология. Единственным источником заражения является человек – больной, выздоравливающий или здоровый бактерионоситель. Заражение происходит воздушно-капельным, воздушно-пылевым путем, а также через различные предметы, бывшие в употреблении у больных или здоровых бактерионосителей: посуда, книги, белье, игрушки и т. п. В случае инфицирования пищевых продуктов (молоко, кремы и т. п.) возможно заражение алиментарным путем. Наиболее массивное выделение возбудителя имеет место при острой форме заболевания. Однако наибольшее эпидемиологическое значение имеют лица со стертыми, нетипичными формами заболевания, так как они часто не госпитализируются и выявляются далеко не сразу. Больной дифтерией заразен в течение всего периода болезни и части периода выздоровления. Средний срок бактерионосительства у выздоравливающих варьирует от 2 до 7 нед., но может продолжаться и до 3 мес.
Особую роль в эпидемиологии дифтерии играют здоровые бактерионосители. В условиях спорадической заболеваемости именно они являются основными распространителями дифтерии, способствуя и сохранению возбудителя в природе. Средняя продолжительность носительства токсигенных штаммов несколько меньше (около 2 мес.), чем нетоксигенных (около 2 – 3 мес.).
Причина формирования здорового носительства токсигенных и нетоксигенных дифтерийных бактерий раскрыта не до конца, так как даже высокий уровень антитоксического иммунитета не всегда обеспечивает полное освобождение организма от возбудителя. Возможно, определенное значение имеет уровень антибактериального иммунитета. Первостепенное эпидемиологическое значение имеет носительство токсигенных штаммов дифтерийных бактерий.
Особенности патогенеза и клиники. К дифтерии восприимчивы люди любого возраста. Возбудитель может проникнуть в организм человека через слизистые оболочки различных органов или через поврежденную кожу. В зависимости от локализации процесса различают дифтерию зева, носа, гортани, уха, глаза, половых органов и кожи. Возможны смешанные формы, например дифтерия зева и кожи и т. п. Инкубационный период – 2 – 10 дней. При клинически выраженной форме дифтерии в месте локализации возбудителя развивается характерное фибринозное воспаление слизистой оболочки. Токсин, вырабатываемый возбудителем, сначала поражает эпителиальные клетки, а затем близлежащие кровеносные сосуды, повышая их проницаемость. В выходящем экссудате содержится фибриноген, свертывание которого приводит к образованию на поверхности слизистой оболочки серовато-белого цвета пленчатых налетов, которые плотно спаяны с подлежащей тканью и при отрыве от нее вызывают кровотечение. Следствием поражения кровеносных сосудов может быть развитие местного отека. Особенно опасной является дифтерия зева, так как она может стать причиной дифтерийного крупа вследствие отека слизистой оболочки гортани и голосовых связок, от которого раньше погибало в результате асфиксии 50 – 60 % больных дифтерией детей. Дифтерийный токсин, поступая в кровь, вызывает общую глубокую интоксикацию. Он поражает преимущественно сердечно-сосудистую, симпатико-адреналовую системы и периферические нервы. Таким образом, клиника дифтерии складывается из сочетания местных симптомов, зависящих от локализации входных ворот, и общих симптомов, обусловленных отравлением токсином и проявляющихся в виде адинамии, вялости, бледности кожных покровов, понижения кровяного давления, миокардита, паралича периферических нервов и других нарушений. Дифтерия у привитых детей, если и наблюдается, протекает, как правило, в легкой форме и без осложнений. Летальность в период до применения серотерапии и антибиотиков составляла 50 – 60 %, ныне – 3 – 6 %.
Постинфекционный иммунитет прочный, стойкий, фактически пожизненный, повторные случаи заболевания наблюдаются редко – у 5 – 7 % переболевших. Иммунитет носит главным образом антитоксический характер, меньшее значение имеют антимикробные антитела.
Для оценки уровня противодифтерийного иммунитета ранее широко применялась проба Шика. С этой целью внутрикожно детям вводилась 1/40 Dlm токсина для морской свинки в объеме 0,2 мл. При отсутствии антитоксического иммунитета через 24 – 48 ч на месте введения появляется краснота и припухлость диаметром более 1 см. Такая положительная реакция Шика свидетельствует либо о полном отсутствии антитоксина, либо о том, что его содержание составляет менее 0,001 АЕ/мл крови. Отрицательная реакция Шика наблюдается, когда содержание антитоксина в крови выше 0,03 АЕ/мл. При содержании антитоксина ниже 0,03 АЕ/мл, но выше 0,001 АЕ/мл реакция Шика может быть или положительной, или, иногда, отрицательной. Кроме того, сам токсин обладает выраженным аллергенным свойством. Поэтому для определения уровня противодифтерийного иммунитета (количественное содержание антитоксина) лучше пользоваться РПГА с эритроцитарным диагностикумом, сенсибилизированным дифтерийным анатоксином.
Лабораторная диагностика. Единственным методом микробиологической диагностики дифтерии является бактериологический, с обязательной проверкой выделенной культуры коринебактерий на токсигенность. Бактериологические исследования на дифтерию проводят в трех случаях:
1) для диагностики дифтерии у детей и взрослых с острыми воспалительными процессами в области зева, носа, носоглотки;
2) по эпидемическим показаниям лиц, находившихся в контакте с источником возбудителя дифтерии;
3) лиц, вновь поступающих в детские дома, ясли, школы-интернаты, другие специальные учреждения для детей и взрослых, с целью выявления среди них возможных бактерионосителей дифтерийной палочки.
Материалом для исследования служат слизь из зева и носа, пленка с миндалин или других слизистых оболочек, являющихся местом входных ворот возбудителя. Посевы производят на теллуритовые сывороточные или кровяные среды и одновременно на свернутые сывороточные среды Ру (свернутая лошадиная сыворотка) или Леффлера (3 части бычьей сыворотки + 1 часть сахарного бульона), на которых рост коринебактерий появляется уже через 8 – 12 ч. Выделенную культуру идентифицируют по совокупности морфологических, культуральных и биохимических свойств, по возможности используют методы серо– и фаготипирования. Во всех случаях обязательна проверка на токсигенность одним из указанных выше методов. Морфологические особенности коринебактерий лучше изучать, используя три метода окрашивания препарата-мазка: по Граму, Нейссеру и метиленовым синим (или толуидиновым синим).
Лечение. Специфическим средством лечения дифтерии является применение противодифтерийной антитоксической сыворотки, содержащей не менее 2000 МЕ в 1 мл. Сыворотку вводят внутримышечно в дозах от 10 000 до 400 000 МЕ в зависимости от тяжести течения болезни. Эффективным методом лечения является применение антибиотиков (пенициллины, тетрациклины, эритромицин и др.) и сульфаниламидных препаратов. С целью стимулирования выработки собственных антитоксинов можно использовать анатоксин. Для освобождения от бактерионосительства следует использовать те антибиотики, к которым данный штамм коринебактерий высокочувствителен.
Специфическая профилактика. Основным методом борьбы с дифтерией является массовая плановая вакцинация населения. С этой целью используют различные варианты вакцин, в том числе комбинированные, т. е. направленные на одновременное создание иммунитета против нескольких возбудителей. Наибольшее распространение в России получила вакцина АКДС. Она представляет собой адсорбированную на гидроокиси алюминия взвесь коклюшных бактерий, убитых формалином или мертиолятом (20 млрд в 1 мл), и содержит дифтерийный анатоксин в дозе 30 флоккулирующих единиц и 10 единиц связывания столбнячного анатоксина в 1 мл. Вакцинируют детей с 3-месячного возраста, а затем проводят ревакцинации: первую через 1,5 – 2 года, последующие в возрасте 9 и 16 лет, а далее через каждые 10 лет.
Благодаря массовой вакцинации, начатой в СССР в 1959 г., заболеваемость дифтерией в стране к 1966 г. по сравнению с 1958 г. была снижена в 45 раз, а ее показатель в 1969 г. составил 0,7 на 100 000 населения. Последовавшее в 80-х гг. ХХ в. снижение объема прививок привело к тяжелым последствиям. В 1993 – 1996 гг. Россию охватила эпидемия дифтерии. Болели взрослые, в основном не получившие прививок, и дети. В 1994 г. было зарегистрировано почти 40 тыс. больных. В связи с этим была возобновлена массовая вакцинация. В этот период были привиты 132 млн человек, в том числе 92 млн взрослых. В 2000 – 2001 гг. охват детей прививками в установленный срок составил 96 %, а ревакцинацией – 94 %. Благодаря этому уровень заболеваемости дифтерией в 2001 г. снизился по сравнению с 1996 г. в 15 раз. Однако для того чтобы довести уровень заболеваемости до единичных случаев, необходимо охватить вакцинацией не менее 97 – 98 % детей первого года жизни и обеспечить в последующие годы массовую ревакцинацию. Добиться полной ликвидации дифтерии в ближайшие годы вряд ли возможно из-за распространенного носительства токсигенных и нетоксигенных дифтерийных бактерий. Для решения этой проблемы также потребуется определенное время.
Микробиология коклюша и паракоклюша
Коклюш – острое инфекционное заболевание преимущественно детского возраста, характеризующееся циклическим течением и приступообразным спазматическим кашлем.
Возбудитель – Bordetella pertussis – впервые был обнаружен в 1900 г. в мазках из мокроты ребенка и затем выделен в чистой культуре в 1906 г. Ж. Борде и О. Жангу. Возбудитель сходного с коклюшем, но протекающего более легко заболевания – Bordetella parapertussis – был выделен и изучен в 1937 г. Г. Эльдерингом и П. Кендриком и независимо от них в 1937 г. У. Брэдфордом и Б. Славиным. Bordetella bronchiseptica, возбудитель редко встречающегося у человека коклюшеподобного заболевания, был выделен в 1911 г. у собак Н. Ферри, а у человека – в 1926 г. Брауном. В 1984 г. был выделен новый вид – Bordetella avium, патогенность которого для человека пока не установлена.
Бордетеллы относятся к классу Betaproteobacteria, грамотрицательны, хорошо окрашиваются всеми анилиновыми красителями. Иногда выявляется биполярная окраска за счет зерен волютина на полюсах клетки. Возбудитель коклюша имеет форму овоидной палочки (коккобактерии) размером 0,2 – 0,5 × 1,0 – 1,2 мкм. Паракоклюш-
ная палочка имеет такую же форму, но несколько крупнее (0,6 × 2 мкм). Расположены чаще поодиночке, но могут располагаться попарно. Спор не образуют, у молодых культур и у бактерий, выделенных из макроорганизма, обнаруживается капсула. Бордетеллы неподвижны, за исключением B. bronchiseptica, которая является перитрихом. Содержание Г + Ц в ДНК составляет 61 – 70 мол %. Относятся к гемофильным бактериям. Бордетеллы – строгие аэробы, хемоорганотрофы. Оптимальная температура роста – 35 – 36 °C. Возбудитель коклюша в гладкой S-форме (так называемая фаза I), в отличие от двух других видов бордетелл, не растет на МПБ и МПА, так как его размножению мешают накопление в среде ненасыщенных жирных кислот, образующихся в процессе роста, а также возникающая при росте коллоидная сера и другие продукты метаболизма. Для их нейтрализации (или адсорбции) в среду выращивания коклюшных бактерий необходимо добавлять крахмал, альбумин и древесный уголь или ионообменные смолы. Микроб требует наличия в среде выращивания 3 аминокислот – пролина, цистеина и глутаминовой кислоты, источником которых служат гидролизаты казеина или фасоли. Традиционная среда для выращивания коклюшной палочки – среда Борде – Жангу (картофельно-глицериновый агар с добавлением крови), на ней она растет в виде гладких, блестящих, прозрачных куполообразных с жемчужным или металлическим ртутным оттенком колоний диаметром около 1 мм, которые вырастают на 3 – 4-й день. На другой среде – казеиново-угольном агаре (КУА) – также на 3 – 4-й день вырастают гладкие выпуклые колонии диаметром около 1 мм, имеющие серовато-кремовый цвет и вязкую консистенцию. Колонии паракоклюшных бактерий по внешнему виду не отличаются от коклюшных, но крупнее и выявляются на 2 – 3-й день, а колонии B. bronchiseptica выявляются уже на 1 – 2-й день.
Характерной особенностью коклюшных бактерий является их наклонность к быстрому изменению культуральных и серологических свойств при изменении состава питательной среды, температуры и других условий выращивания. В процессе перехода от S-формы (фаза I) к стабильной шероховатой R-форме (фаза IV) через промежуточные фазы II и III наблюдаются плавные изменения антигенных свойств;
патогенные свойства теряются.
Паракоклюшные бактерии и B. bronchiseptica, а также фазы II, III и IV коклюшных бактерий растут на МПА и МПБ. При выращивании на жидкой среде наблюдается диффузное помутнение с придонным плотным осадком; клетки могут быть несколько крупнее и полиморфными, иногда образуют нити. В R-форме и промежуточных формах бактерии проявляют выраженный полиморфизм.
На среде Борде – Жангу все бордетеллы образуют вокруг колоний нерезко ограниченную зону гемолиза, распространяющуюся диффузно в среду.
Бордетеллы не ферментируют углеводов, не образуют индола, не восстанавливают нитраты в нитриты (за исключением B. bronchiseptica). Паракоклюшные бактерии выделяют тирозиназу, образуя пигмент, окрашивающий среду и культуру в коричневый цвет. Дифференциальные признаки бордетелл приведены в табл. 46.
Бордетеллы содержат несколько антигенных комплексов. Соматический О-антиген видоспецифичен (см. табл. 43); родовым антигеном является агглютиноген 7. Главные агглютиногены у возбудителя коклюша – 7-й (родовой), 1-й (видовой) и наиболее часто обнаруживаемые типоспецифические 2-й и 3-й. В зависимости от их сочетания у Bordetella pertussis выделяют четыре сероварианта: 1, 2, 3; 1, 2, 0; 1, 0, 3 и 1, 0, 0.
Факторы патогенности. Фимбрии (агглютиногены), белок наружной мембраны пертактин (69 кД) и филаментозный гемагглютинин (поверхностный белок) отвечают за адгезию возбудителя на цилиарном эпителии средних отделов респираторного тракта (трахея, бронхи). Капсула защищает от фагоцитоза. Часто присутствуют гиалуронидаза, лецитиназа, плазмокоагулаза, аденилатциклаза. В составе эндотоксина
Таблица 46
Дифференциальные признаки бордетелл
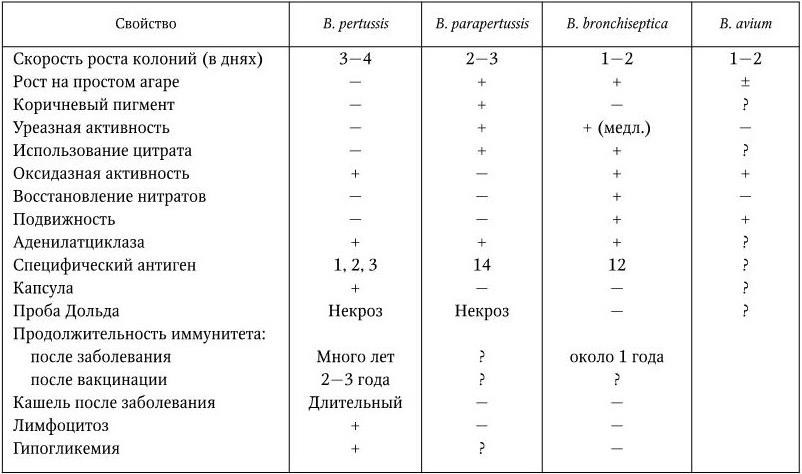
Примечание. (+) – признак положительный; ( – ) – признак отрицательный; (±) – признак иногда положительный, иногда отрицательный; (?) – нет данных.
(ЛПС) два липида: А и Х. Биологическая активность ЛПС определяется липидом Х, липид А обладает низкой пирогенностью и нетоксичен. ЛПС обладает иммуногенностью (цельноклеточная вакцина), но вызывает сенсибилизацию. Имеются три экзотоксина. Коклюшный токсин (117 кД) по структуре и функции подобен холерогену, проявляет активность АДФ-рибозилтрансферазы (рибозилирует трансдуцин – белок мембраны клетки-мишени, являющийся частью системы, ингибирующей клеточную аденилатциклазу), сильный иммуноген, повышает лимфоцитоз и выработку инсулина. Трахеальный цитотоксин представляет собой фрагмент пептидогликана, обладает пирогенностью, артритогенностью, индуцирует медленноволновой сон и стимулирует продукцию IL-1, в ответ на который синтезируется оксид азота (цитотоксический фактор). Повреждает эпителиальные клетки трахеи и вызывает цилиостаз. Термолабильный дермонекротоксин обладает нейротропностью, сосудосуживающей активностью, гомологичен цитотоксическому некротизирующему фактору 1 (CNF1) кишечной палочки. Мишенью его являются Rho-белки мембран клеток. Обнаруживают дермонекротоксин внутрикожной пробой на кроликах (проба Дольда).
Эпидемиология. Источник инфекции при коклюше и паракоклюше – больной типичной или стертой формой, особенно в период до появления спазматического кашля. При коклюшеподобном заболевании, вызванном B. bronchiseptica, источником инфекции могут быть домашние и дикие животные, среди которых иногда наблюдаются эпизоотии (свиньи, кролики, собаки, кошки, крысы, морские свинки, обезьяны), при этом чаще всего у животного поражается респираторный тракт. Механизм заражения – воздушно-капельный. Бордетеллы обладают специфическим тропизмом к цилиарному эпителию респираторного тракта хозяина. К инфекции восприимчивы люди всех возрастов, но более всего дети от 1 года до 10 лет.
Патогенез и клиника. Инкубационный период при коклюше от 3 до 14 дней, чаще 5 – 8 дней. Возбудитель, попавший на слизистую оболочку верхних дыхательных путей, размножается в клетках цилиарного эпителия и далее бронхогенным путем распространяется в более низкие отделы (бронхиолы, альвеолы, мелкие бронхи). При действии экзотоксина эпителий слизистой оболочки некротизируется, в результате чего раздражаются кашлевые рецепторы и создается постоянный поток сигналов в кашлевой центр продолговатого мозга, в котором формируется стойкий очаг возбуждения. Это приводит к возникновению спазматических приступов кашля. Бактериемии при коклюше не бывает. Вторичная бактериальная флора может приводить к осложнениям.
В течении заболевания выделяют следующие стадии: 1) катаральный период, длящийся около 2 нед. и сопровождающийся сухим кашлем; состояние больного постепенно ухудшается; 2) конвульсивный (судорожный), или спазматический, период, длящийся до 4 – 6 нед. и характеризующийся возникающими до 20 – 30 раз в сутки приступами неукротимого «лающего» кашля, причем приступы могут быть спровоцированы даже неспецифическими раздражителями (свет, звук, запах, медицинские манипуляции, осмотр и т. д.); 3) период разрешения, когда приступы кашля становятся реже и все менее продолжительными, отторгаются некротизированные участки слизистой оболочки верхних дыхательных путей, часто в виде «слепков» с трахеи и бронхов; продолжительность – 2 – 4 нед.
Иммунитет. После перенесенного заболевания формируется стойкий пожизненный иммунитет; поствакцинальный иммунитет сохраняется всего 3 – 5 лет.
Лабораторная диагностика. Основными методами диагностики являются бактериологический и серологический; для ускоренной диагностики, особенно на ранней стадии болезни, может быть использована реакция иммунофлуоресценции. Для выделения чистой культуры в качестве материала используют слизь из носоглотки или мокроту, которые высевают на КУА или среду Борде – Жангу. Посев также может быть сделан методом «кашлевых пластинок». Выросшую культуру идентифицируют по совокупности культуральных, биохимических и антигенных свойств. Серологические реакции – агглютинации, связывания комплемента, пассивной гемагглютинации – ставятся в основном для ретроспективной диагностики коклюша или в тех случаях, когда не выделена чистая культура. Антитела к возбудителю появляются не ранее 3-й нед. заболевания, диагноз подтверждается возрастанием титра антител в сыворотках, взятых с 1 – 2-недельным интервалом. У детей первых двух лет жизни серологические реакции часто бывают отрицательными.
Специфическая профилактика и лечение. Для плановой профилактики коклюша у детей используют адсорбированную коклюшно-дифтерийно-столбнячную вакцину (АКДС), содержащую 20 млрд убитых коклюшных бактерий в 1 мл. На этом же компоненте основана выпускаемая отдельно убитая коклюшная вакцина, применяемая в детских коллективах по эпидемиологическим показаниям. Этот компонент реактогенен (нейротоксическое свойство), поэтому сейчас активно изучаются бесклеточные вакцины, содержащие от 2 до 5 компонентов (коклюшный анатоксин, филаментозный гемагглютинин, пертактин и 2 агглютиногена фимбрий). Для лечения применяют антибиотики (гентамицин, ампициллин), эффективные в катаральном и бесполезные в судорожном периоде заболевания.
Палочка инфлюэнцы
Палочка инфлюэнцы – Haemophilus influenzae – часто присутствует на слизистой оболочке верхних дыхательных путей здорового человека. При ослаблении устойчивости организма она может вызвать менингит (особенно у ослабленных детей), бронхит, пневмонию, гнойный плеврит, трахеит, ларингит, конъюнктивит, отит и другие заболевания.
Возбудитель был открыт М. И. Афанасьевым (1891) и описан Р. Пфейффером и С. Китазато в 1892 г. во время пандемии гриппа, причиной которого палочка инфлюэнцы ошибочно считалась более 40 лет.
Род Haemophilus входит в состав семейства Pasteurellaceae и состоит из 16 видов. Для человека патогенны два вида: H. influenzae – возбудитель воспалительных процессов дыхательных путей, и H. ducreyi – возбудитель мягкого шанкра; эта болезнь в России с 1961 г. не обнаруживается.
Гемофилы – короткие палочки кокковидной формы размерами 0,3 – 0,4 × 1,0 – 1,5 мкм (см. цв. вкл., рис. 104). Иногда располагаются короткими цепочками, чаще – поодиночке. Они очень полиморфны, могут образовывать нити, что зависит от условий культивирования; неподвижны, спор не имеют. Палочка инфлюэнцы в организме и в первых генерациях на питательных средах может иметь капсулу. Бактерии медленно окрашиваются анилиновыми красителями: фуксином Пфейффера прокрашиваются в течение 5 – 15 мин.
Бактерии рода Haemophilus относятся к группе гемофильных. Они требуют для культивирования богатые питательные среды, обычно содержащие кровь или ее препараты. Для их роста требуется наличие в среде гемина или некоторых других порфиринов (Х-фактор) и (или) никотинамидадениндинуклеотида (V-фактор). Установлено, что из 16 известных представителей рода Haemophilus 2 вида (H. influenzae и H. haemolyticus) требуют наличия одновременно Х-фактора и V-фактора, 4 вида требуют только Х-фактора и 10 видов – только V-фактора. Х-фактор термостабилен, и в качестве его источников используют кровь различных животных или водный раствор хлористого гематина. V-фактор термолабилен и содержится в тканях растений, животных, вырабатывается многими бактериями.
Палочка инфлюэнцы – факультативный анаэроб, оптимальная температура для ее роста 37 °C. Содержание Г + Ц в ДНК составляет 39 – 42 мол %. На «шоколадном» агаре (агаре с прогретой кровью) колонии палочки инфлюэнцы вырастают через 36 – 48 ч и достигают диаметра 1 мм. На кровяном агаре с добавлением сердечно-мозгового экстракта через сутки вырастают мелкие, округлые, выпуклые колонии с радужными переливами. Гемолиз отсутствует. У колоний бескапсульных вариантов радужная расцветка отсутствует. На жидких средах с добавлением крови наблюдается диффузный рост, иногда образуются белесые хлопья и осадок на дне.
Специфической особенностью палочек инфлюэнцы является способность их колоний вырастать гораздо быстрее и быть крупнее вблизи колоний стафилококков или других бактерий («спутниковый», или сателлитный, рост). Пневмококки же являются ингибиторами роста палочки инфлюэнцы.
Сахаролитические свойства выражены слабо и непостоянны. Обычно ферментирует с образованием кислоты рибозу, галактозу и глюкозу, обладает уреазной активностью, имеет щелочную фосфотазу, восстанавливает нитраты в нитриты. По способности образовывать уреазу, индол и орнитиндекарбоксилазу H. influenzae подразделяют на шесть биотипов (I – VI).
Капсульные штаммы палочки инфлюэнцы по специфичности полисахаридного антигена делятся на 6 серовариантов: a, b, c, d, e, f. Этот антиген иногда дает перекрестную реакцию с антигенами капсульных пневмококков. Капсульный полисахаридный антиген обнаруживается по реакции набухания капсулы, РИФ, реакции преципитации в агаре. От больных людей чаще выделяется серовар b. Кроме капсульного антигена у возбудителя инфлюэнцы имеется соматический антиген, в составе которого обнаружены термостабильный и термолабильный протеины.
Экзотоксинов палочка инфлюэнцы не продуцирует, патогенность ее связана с термостабильным эндотоксином, выделяющимся при разрушении бактериальных клеток. Инвазивность и подавление фагоцитоза связаны с наличием капсулы.
Во внешней среде возбудитель малоустойчив, быстро погибает под действием прямых солнечных и ультрафиолетовых лучей и дезинфицирующих веществ в обычных рабочих концентрациях. При температуре 60 °C он погибает в течение 5 – 10 мин.
Эпидемиология. Источником инфекции при заболеваниях, вызванных палочкой инфлюэнцы, служат больные люди; капсульные штаммы в этом случае передаются от человека к человеку воздушно-капельным путем. Часто заболевание развивается как проявление аутоинфекции при снижении реактивности организма на фоне какого-либо другого заболевания, например гриппа. Палочка инфлюэнцы у здоровых людей обнаруживается не только на слизистой оболочке верхних дыхательных путей, но и в полости рта, среднего уха, иногда на слизистой оболочке влагалища.
Патогенез и клиника связаны прежде всего с особенностями возбудителя (имеется капсула или нет), а также с основным заболеванием, на фоне которого снижается резистентность макроорганизма. Палочка инфлюэнцы может размножаться на слизистых оболочках как вне-, так и внутриклеточно, иногда проникая в кровь. В этом случае возбудитель может далее проникнуть через гематоэнцефалический барьер и вызвать менингит. Палочка инфлюэнцы, наряду с менингококками и пневмококками, относится к наиболее частым возбудителям менингита. Летальность при таком нелеченном менингите может достигать 90 %. Клиника определяется доминирующими в каждом конкретном случае симптомами в зависимости от степени поражения того или иного органа.
Иммунитет. Дети первых трех месяцев жизни мало восприимчивы к возбудителю инфлюэнцы, так как у них в сыворотке присутствуют антитела, переданные через плаценту от матери. Впоследствии они исчезают, и ребенок становится восприимчив к возбудителю. Инфекция может протекать бессимптомно или с поражением респираторного тракта. Менингиты чаще всего развиваются у детей в возрасте от 6 мес. до 3 лет. К 3 – 5 годам у многих детей появляются комплементсвязывающие и бактерицидные антитела к капсульному полисахаридному антигену (полирибозофосфату).
Лабораторная диагностика. Для диагностики заболеваний, вызванных палочкой инфлюэнцы, используют РИФ, бактериологический метод и серологические реакции. При достаточной концентрации возбудителя в исследуемом материале (гной, слизь, ликвор) он легко и быстро может быть обнаружен с помощью реакции набухания капсулы и РИФ; ликвор можно также исследовать с помощью метода встречного иммуноэлектрофореза. Чистую культуру выделяют посевом материала на специальные питательные среды («шоколадный» агар, среда Левинталя, сердечно-мозговой агар); типичные колонии идентифицируют по реакции набухания капсулы, потребности в факторах роста и другим тестам (биохимические свойства, реакции преципитации в агаре и др.). Для серологической диагностики могут быть использованы реакции агглютинации и преципитации.
Специфическая профилактика и лечение. Для профилактики используют вакцину из капсульного полисахарида (полирибозофосфата). В настоящее время болезни, вызываемые Haemophilus influenzae типа b, рассматривают в качестве кандидатов на искоренение. Для лечения наиболее эффективны аминогликозиды, левомицетин, сульфаниламиды, однако у выделенных возбудителей необходимо определять степень чувствительности к антибиотикам.
Назад: Глава 61 Возбудители кишечных инфекций
Дальше: Глава 63 Листерии, легионеллы и вызываемые ими болезни

