Глава 1. Воздух в квартире
1.1. Окислы азота
В атмосфере находятся, конечно, и более вредные газы (например, хлор или цианиды), но их не так много, как окислов азота. В широком смысле окислов азота минимум четыре (N2O5 так называемый «веселящий газ»), NO, N2O3, NO2 – вместе их объединяют формулой NOx, совместно с окислами серы и углерода этот газ инициирует выпадение кислотных дождей.
Среди «кислых» газов (NОx, SO2 и СО2) окислы азота по вредности занимают «по праву» первое место. Если принять за единицу относительную вредность углекислого газа, то относительная вредность окислов азота составляет 20, а относительная вредность окислов серы – 12.
Оксиды азота обладают высокой токсичностью, но, реагируя с другими веществами, они способны образовывать еще более токсичные соединения, а также фотохимические туманы (смоги). Если переход на сжигание «чистых» с точки зрения загрязнения воздушного бассейна топлив (например, на природный газ) позволяет резко сократить, а иногда полностью устранить все прочие выбросы вредностей, то на сокращение окислов азота это не оказывает существенного влияния. Сказанное ставит этот газ в один ряд с такими мощными загрязнителями окружающей среды, как окислы серы и твердые частицы. Влияние NOx на организм человека показано в табл. 1.
Таблица 1
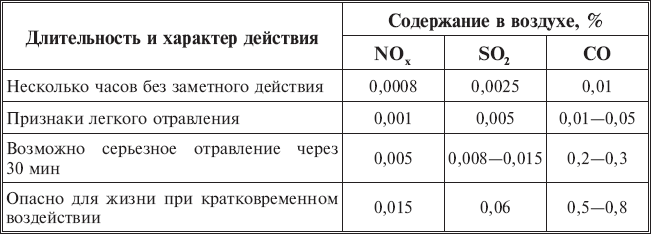
Раздражающее и обжигающее действие NOx на дыхательные пути приводит к раковым заболеваниям дыхательных органов человека. Уже при концентрации 15 мг/м3 отмечается раздражение глаз, а концентрация 200–300 мг/м3 даже при кратковременном воздействии может вызвать отек легкого.
Реагируя с атмосферной влагой, NOx образует азотную кислоту, которая вызывает интенсивную коррозию металлических сооружений и конструкций. NОх поглощает видимый свет и при концентрации около 0,5 мг/м3 приводит к уменьшению видимости, что может стать причиной аварий на автомобильном, морском и воздушном транспорте. При интенсивном выделении NOx уменьшается количество солнечных дней в году.
Двуокись азота – бурый газ с удушливым запахом является сильным окислителем. Концентрация окислов азота определяется в лаборатории с помощью калориметров, спектрофотометров или электрофотокалориметров. Однако для бытовых нужд для оценки концентрации NOx вполне приемлем экспресс-метод с использованием прибора УГ-2. Этот метод не такой точный, как упомянутые выше, но для того, чтобы обнаружить NОx в доме, его точности достаточно. Сам прибор представляет собой небольшую металлическую коробку с расположенными в ней мехами. Набрав пробу воздуха, меха сжимаются, и выходящий воздух с загрязнителем поступает в индикаторную трубку. По изменению окраски этой трубки судят о наличии NOx в воздухе.
Бороться с этим газом очень трудно, но все же кое-что экологи могут посоветовать; в частности, не открывать окна и двери на балкон в часы пик, когда на улице наиболее интенсивное движение автомашин и максимальная концентрация этого газа. Причем больше всего он выделяется при работе двигателей автомобилей на холостом ходу, а также в пробках и на перекрестках со светофорами или без них. Кроме того, защиту вашего организма от NOх (так же как и от SO2) обеспечит употребление в пищу йодистых соединений.
Если Вы живете у автотрассы, или возле котельных, или ТЭЦ, то летом необходимо вывозить за город детей и по возможности уезжать самим для прочистки ваших легких. Человек, правда, обладает удивительным свойством адаптации к окружающей среде, и бывает, что, выехав за город, вы первое время неважно себя чувствуете, но это быстро проходит. У Аркадия Райкина была шутка о том, что у выхлопной трубы автомобиля человек за городом лучше себя чувствует; в этой шутке есть доля правды.

