7.2. Галогены
7.2.1. Хлор. Хлороводород
Хлор – элемент 3-го периода и VII А-группы Периодической системы, порядковый номер 17. Электронная формула атома [10Ne]3s23p5, характерные степени окисления 0, -I, +I, +V и +VII. Наиболее устойчиво состояние Cl-I. Шкала степеней окисления хлора:

Хлор обладает высокой электроотрицательностью (2,83), проявляет неметаллические свойства. Входит в состав многих веществ – оксидов, кислот, солей, бинарных соединений.
В природе – двенадцатый по химической распространенности элемент (пятый среди неметаллов). Встречается только в химически связанном виде. Третий по содержанию элемент в природных водах (после О и H), особенно много хлора в морской воде (до 2 % по массе). Жизненно важный элемент для всех организмов.
Хлор Cl2. Простое вещество. Желто-зеленый газ с резким удушливым запахом. Молекула Cl2 неполярна, содержит σ-связь CI–Cl. Термически устойчив, негорюч на воздухе; смесь с водородом взрывается на свету (водород сгорает в хлоре):
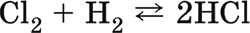
Хорошо растворим в воде, подвергается в ней дисмутации на 50 % и полностью – в щелочном растворе:
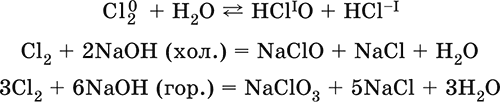
Раствор хлора в воде называют хлорной водой, на свету кислота НClO разлагается на НCl и атомарный кислород О0, поэтому «хлорную воду» надо хранить в темной склянке. Наличием в «хлорной воде» кислоты НСlO и образованием атомарного кислорода объясняются ее сильные окислительные свойства: например, во влажном хлоре обесцвечиваются многие красители.
Хлор очень сильный окислитель по отношению к металлам и неметаллам:
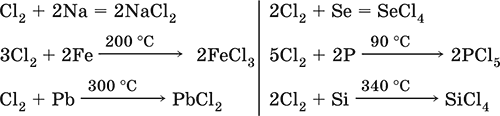
Реакции с соединениями других галогенов:
а) Cl2 + 2KBr(p) = 2КCl + Br2↑ (кипячение)
б) Cl2 (нед.) + 2KI(p) = 2КCl + I2↓
3Cl2 (изб.) + ЗН2O + KI = 6НCl + КIO3 (80 °C)
Качественная реакция – взаимодействие недостатка Cl2 с KI (см. выше) и обнаружение иода по синему окрашиванию после добавления раствора крахмала.
Получение хлора в промышленности:
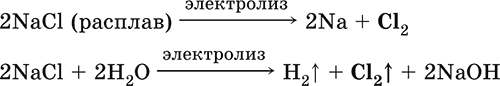
и в лаборатории:
4НCl (конц.) + MnO2 = Cl2↑ + MnCl2 + 2Н2O
(аналогично с участием других окислителей; подробнее см. реакции для НCl и NaCl).
Хлор относится к продуктам основного химического производства, используется для получения брома и иода, хлоридов и кислородсодержащих производных, для отбеливания бумаги, как дезинфицирующее средство для питьевой воды. Ядовит.
Хлороводород НCl. Бескислородная кислота. Бесцветный газ с резким запахом, тяжелее воздуха. Молекула содержит ковалентную σ-связь Н – Cl. Термически устойчив. Очень хорошо растворим в воде; разбавленные растворы называются хлороводородной кислотой, а дымящий концентрированный раствор (35–38 %) – соляной кислотой (название дано еще алхимиками). Сильная кислота в растворе, нейтрализуется щелочами и гидратом аммиака. Сильный восстановитель в концентрированном растворе (за счет Cl-I), слабый окислитель в разбавленном растворе (за счет НI). Составная часть «царской водки».
Качественная реакция на ион Cl- – образование белых осадков AgCl и Hg2Cl2, которые не переводятся в раствор действием разбавленной азотной кислоты.
Хлороводород служит сырьем в производстве хлоридов, хлорорганических продуктов, используется (в виде раствора) при травлении металлов, разложении минералов и руд.
Уравнения важнейших реакций:
НCl (разб.) + NaOH (разб.) = NaCl + Н2O
HCl (разб.) + NH3 H2O = NH4Cl + Н2O
4HCl (конц., гор.) + МО2 = МCl2 + Cl2↑ + 2H2O (М = Mn, Pb)
16HCl (конц., гор.) + 2КMnO4(т) = 2MnCl2 + 5Cl2↑ + 8H2O + 2КCl
14HCl (конц.) + К2Cr2O7(т) = 2CrCl3 + ЗCl2↑ + 7H2O + 2КCl
6HCl (конц.) + КClO3(т) = КCl + ЗCl2↑ + 3H2O (50–80 °C)
4HCl (конц.) + Са(ClO)2(т) = СаCl2 + 2Cl2| + 2Н2O
2HCl (разб.) + М = МCl2 + H2↑ (М = Fe, Zn)
2HCl (разб.) + МСO3 = МCl2 + СO2↑ + H2O (М = Са, Ва)
HCl (разб.) + AgNO3 = HNO3 + AgCl↓
Получение НCl в промышленности – сжигание Н2 в Cl2 (см.), в лаборатории – вытеснение из хлоридов серной кислотой:
NaCl(т) + H2SO4 (конц.) = NaHSO4 + НCl↑ (50 °C)
2NaCl(т) + H2SO4 (конц.) = Na2SO4 + 2НCl↑ (120 °C)
7.2.2. Хлориды
Хлорид натрия NaCl. Бескислородная соль. Бытовое название поваренная соль. Белый, слабогигроскопичный. Плавится и кипит без разложения. Умеренно растворим в воде, растворимость мало зависит от температуры, раствор имеет характерный соленый вкус. Гидролизу не подвергается. Слабый восстановитель. Вступает в реакции ионного обмена. Подвергается электролизу в расплаве и растворе.
Применяется для получения водорода, натрия и хлора, соды, едкого натра и хлороводорода, как компонент охлаждающих смесей, пищевой продукт и консервирующее средство.
В природе – основная часть залежей каменной соли, или галита, и сильвинита (вместе с КCl), рапы соляных озер, минеральных примесей морской воды (содержание NaCl = 2,7 %). В промышленности получают выпариванием природных рассолов.
Уравнения важнейших реакций:
2NaCl(т) + 2H2SO4 (конц.) + MnO2(т) = Cl2↑ + MnSO4 + 2Н2O + Na2SO4 (100 °C)
10NaCl(т) + 8H2SO4 (конц.) + 2КMnO4(т) = 5Cl2↑ + 2MnSO4 + 8Н2O + 5Na2SO4 + K2SO4 (100 °C)
6NaCl(т) + 7H2SO4 (конц.) + К2Cr2O7(т) = ЗCl2 + Cr2(SO4)3 + 7Н2O + 3Na2SO4 + K2SO4 (100 °C)
2NaCl(т) + 4H2SO4 (конц.) + РЬO2(т) = Cl2↑ + Pb(HSO4)2 + 2Н2O + 2NaHSO4 (50 °C)
NaCl (разб.) + AgNO3 = NaNO3 + AgCl↓
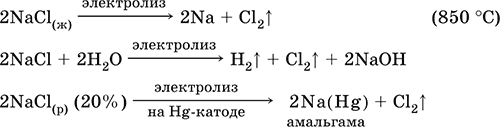
Хлорид калия KCl. Бескислородная соль. Белый, негигроскопичный. Плавится и кипит без разложения. Умеренно растворим в воде, раствор имеет горький вкус, гидролиза нет. Вступает в реакции ионного обмена. Применяется как калийное удобрение, для получения К, КОН и Cl2. В природе основная составная часть (наравне с NaCl) залежей сильвинита.
Уравнения важнейших реакций одинаковы с таковыми для NaCl.
Хлорид кальция СаCl2. Бескислородная соль. Белый, плавится без разложения. Расплывается на воздухе за счет энергичного поглощения влаги. Образует кристаллогидрат СаCl2 6Н2O с температурой обезвоживания 260 °C. Хорошо растворим в воде, гидролиза нет. Вступает в реакции ионного обмена. Применяется для осушения газов и жидкостей, приготовления охлаждающих смесей. Компонент природных вод, составная часть их «постоянной» жесткости.
Уравнения важнейших реакций:
СаCl2(т) + 2H2SO4 (конц.) = Ca(HSO4)2 + 2НCl↑ (50 °C)
СаCl2(т) + H2SO4 (конц.) = CaSO4↓ + 2НCl↑ (100 °C)
СаCl2 + 2NaOH (конц.) = Ca(OH)2↓ + 2NaCl↑
ЗСаCl2 + 2Na3PO4 = Са3(РO4)2↓ + 6NaCl
СаCl2 + К2СO3 = СаСO3↓ + 2КCl
СаCl2 + 2NaF = CaF2↓ + 2NaCl
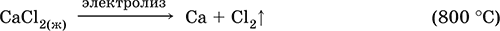
Получение:
СаСO3 + 2HCl = СаCl2 + СO3↑ + Н2O
Хлорид алюминия AlCl3. Бескислородная соль. Белый, легкоплавкий, сильнолетучий. В паре состоит из ковалентных мономеров AlCl3 (треугольное строение, sр2-гибридизация, преобладают при 440–800 °C) и димеров Al2Cl6 (точнее, Cl2AlCl2AlCl2, строение – два тетраэдра с общим ребром, sр3-гибридизация, преобладают при 183–440 °C). Гигроскопичен, на воздухе «дымит». Образует кристаллогидрат, разлагающийся при нагревании. Хорошо растворим в воде (с сильным экзо-эффектом), полностью диссоциирует на ионы, создает в растворе сильнокислотную среду вследствие гидролиза. Реагирует со щелочами, гидратом аммиака. Восстанавливается при электролизе расплава. Вступает в реакции ионного обмена.
Качественная реакция на ион Al3+ – образование осадка AlРO4, который переводится в раствор концентрированной серной кислотой.
Применяется как сырье в производстве алюминия, катализатор в органическом синтезе и при крекинге нефти, переносчик хлора в органических реакциях. Уравнения важнейших реакций:
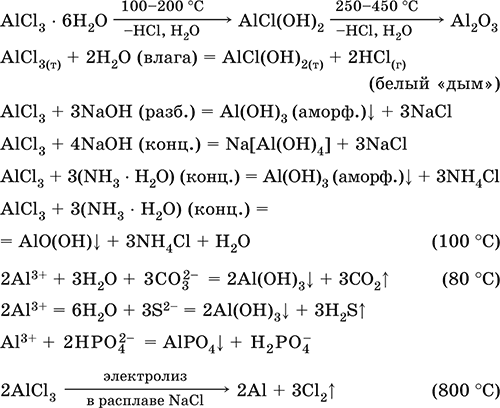
Получение AlCl3 в промышленности – хлорирование каолина, глинозёма или боксита в присутствии кокса:
Al2O3 + ЗС (кокс) + ЗCl2 = 2AlCl3 + ЗСО (900 °C)
Хлорид железа(Н) FeCl2. Бескислородная соль. Белый (гидрат голубовато-зеленый), гигроскопичный. Плавится и кипит без разложения. При сильном нагревании летуч в потоке HCl. Связи Fe – Cl преимущественно ковалентные, пар состоит из мономеров FeCl2 (линейное строение, sp-гибридизация) и димеров Fe2Cl4. Чувствителен к кислороду воздуха (темнеет). Хорошо растворим в воде (с сильным экзо-эффектом), полностью диссоциирует на ионы, слабо гидролизуется по катиону. При кипячении раствора разлагается. Реагирует с кислотами, щелочами, гидратом аммиака. Типичный восстановитель. Вступает в реакции ионного обмена и комплексообразования.
Применяется для синтеза FeCl3 и Fe2O3, как катализатор в органическом синтезе, компонент лекарственных средств против анемии.
Уравнения важнейших реакций:
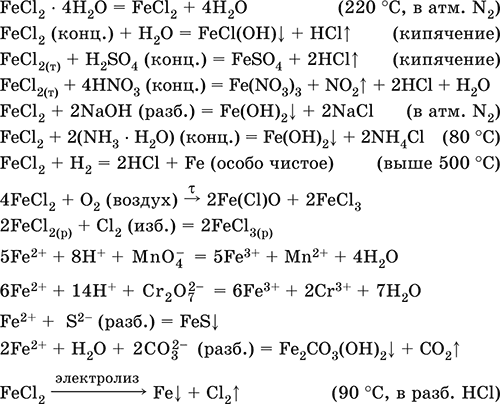
Получение: взаимодействие Fe с соляной кислотой:
Fe + 2НCl = FeCl2 + Н2↑
(в промышленности используют хлороводород и ведут процесс при 500 °C).
Хлорид железа(III) FeCl3. Бескислородная соль. Черно-коричневый (темно-красный в проходящем свете, зеленый в отраженном), гидрат темно-желтый. При плавлении переходит в красную жидкость. Весьма летуч, при сильном нагревании разлагается. Связи Fe – Cl преимущественно ковалентные. Пар состоит из мономеров FeCl3 (треугольное строение, sр2-гибридизация, преобладают выше 750 °C) и димеров Fe2Cl6 (точнее, Cl2FeCl2FeCl2, строение – два тетраэдра с общим ребром, sр3-гибридизация, преобладают при 316–750 °C). Кристаллогидрат FeCl3 6Н2O имеет строение [Fe(H2O)4Cl2]Cl • 2Н2O. Хорошо растворим в воде, раствор окрашен в желтый цвет; сильно гидролизован по катиону. Разлагается в горячей воде, реагирует со щелочами. Слабый окислитель и восстановитель.
Применяется как хлорагент, катализатор в органическом синтезе, протрава при крашении тканей, коагулянт при очистке питьевой воды, травитель медных пластин в гальванопластике, компонент кровоостанавливающих препаратов.
Уравнения важнейших реакций:
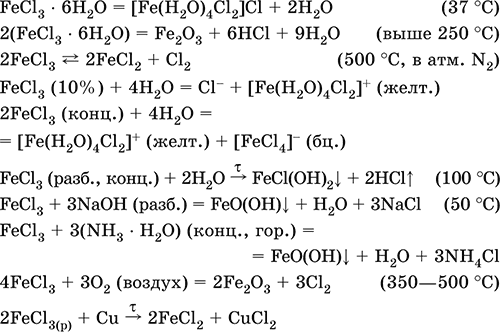
Хлорид аммония NH4Cl. Бескислородная соль, техническое название нашатырь. Белый, летучий, термически неустойчивый. Хорошо растворим в воде (с заметным эндо-эффектом, Q = -16 кДж), гидролизуется по катиону. Разлагается щелочами при кипячении раствора, переводит в раствор магний и гидроксид магния. Вступает в реакцию конмутации с нитратами.
Качественная реакция на ион NH4+ – выделение NH3 при кипячении со щелочами или при нагревании с гашёной известью.
Применяется в неорганическом синтезе, в частности для создания слабокислотной среды, как компонент азотных удобрений, сухих гальванических элементов, при пайке медных и лужении стальных изделий.
Уравнения важнейших реакций:
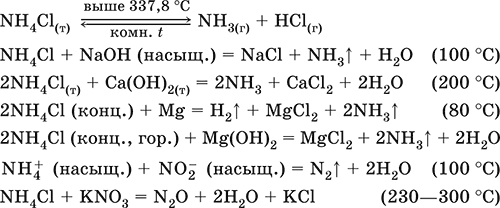
Получение: взаимодействие NH3 с HCl в газовой фазе или NH3 Н2O с HCl в растворе.
7.2.3. Гипохлориты. Хлораты
Гипохлорит кальция Са(СlO)2. Соль хлорноватистой кислоты HClO. Белый, при нагревании разлагается без плавления. Хорошо растворим в холодной воде (образуется бесцветный раствор), гидролизуется по аниону. Реакционноспособный, полностью разлагается горячей водой, кислотами. Сильный окислитель. При стоянии раствор поглощает углекислый газ из воздуха. Является активной составной частью хлорной (белильной) извести – смеси неопределенного состава с СаCl2 и Са(ОН)2. Уравнения важнейших реакций:
Са(ClO)2 = СаCl2 + O2 (180 °C)
Са(ClO)2(т) + 4НCl (конц.) = СаCl2 + 2Cl2↑ + 2Н2O (80 °C)
Са(ClO)2 + Н2O + СO2 = СаСO3↓ + 2НClO (на холоду)
Са(ClO)2 + 2Н2O2 (разб.) = СаCl2 + 2Н2O + 2O2↑
Получение:
2Са(ОН)2 (суспензия) + 2Cl2(г) = Са(ClO)2 + СаCl2 + 2Н2O
Хлорат калия КСlO3. Соль хлорноватой кислоты НСlO3, наиболее известная соль кислородсодержащих кислот хлора. Техническое название — бертоллетова соль (по имени ее первооткрывателя К.-Л. Бертолле, 1786). Белый, плавится без разложения, при дальнейшем нагревании разлагается. Хорошо растворим в воде (образуется бесцветный раствор), гидролиза нет. Разлагается концентрированными кислотами. Сильный окислитель при сплавлении.
Применяется как компонент взрывчатых и пиротехнических смесей, головок спичек, в лаборатории – твердый источник кислорода.
Уравнения важнейших реакций:
4КClO3 = ЗКClO4 + КCl (400 °C)
2КClO3 = 2КCl + 3O2 (150–300 °C, кат. MnO2)
КClO3(т) + 6НCl (конц.) = КCl + ЗCl2| + ЗН2O (50–80 °C)
ЗКClO3(т) + 2H2SO4 (конц., гор.) = 2ClO2| + КClO4 + Н2O + 2KHSO4
(диоксид хлора на свету взрывается: 2ClO2(г) = Cl2 + 2O2)
2КClO3 + Е2(изб.) = 2КЕO3 + Cl2↑ (в разб. HNO3, Е = Br, I)
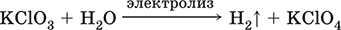
Получение КClO3 в промышленности – электролиз горячего раствора КCl (продукт КClO3 выделяется на аноде):
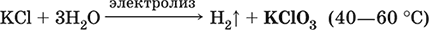
7.2.4. Бромиды. Иодиды
Бромид калия КBr. Бескислородная соль. Белый, негигроскопичный, плавится без разложения. Хорошо растворим в воде, гидролиза нет. Восстановитель (более слабый, чем KI).
Качественная реакция на ион Br – вытеснение брома из раствора КBr хлором и экстракция брома в органический растворитель, например СCl4 (в результате водный слой обесцвечивается, органический слой окрашивается в бурый цвет).
Применяется как компонент травителей при гравировке по металлам, составная часть фотоэмульсий, лекарственное средство.
Уравнения важнейших реакций:
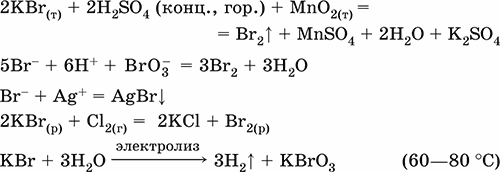
Получение:
K2CO3 + 2HBr = 2KBr + CO2↑ + H2O
Иодид калия KI. Бескислородная соль. Белый, негигроскопичный. При хранении на свету желтеет. Хорошо растворим в воде, гидролиза нет. Типичный восстановитель. Водный раствор KI хорошо растворяет I2 за счет комплексообразования.
Качественная реакция на ион I – вытеснение иода из раствора KI недостатком хлора и экстракция иода в органический растворитель, например СCl4 (в результате водный слой обесцвечивается, органический слой окрашивается в фиолетовый цвет).
Уравнения важнейших реакций:
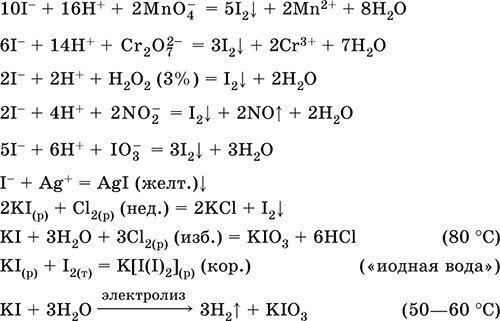
Получение:
K2CO3 + 2HI = 2KI + СO2↑ + Н2O
Назад: 7.1. Водород
Дальше: 7.3. Халькогены

