Книга: Лаборатория химических историй. От электрона до молекулярных машин
Назад: Традиция, логика, расчет
Дальше: Глава 2 Биохимия тоже химия
Создать новую науку
В ХХ в. полимеры уверенно входят в повседневную жизнь. В первое десятилетие были получены патенты на производство полистирола, поливинилхлорида, бакелита (пластмассы на основе фенольных смол). Искусственные волокна на основе целлюлозы, о которых рассказано в разделе «Лидер среди природных полимеров», были уже хорошо известны. К началу 1920-х гг. промышленность уже производит определенный набор полимеров. Интересно то, что науки о полимерах и самого термина «полимеры» в то время не существовало, – употребляли название «смола» (resin). Химики-органики, работавшие в научных лабораториях, рассматривали получение смолообразных продуктов как результат неудачного синтеза и не проявляли к ним интереса. Большинство считало, что полимеры – это определенный вид коллоидных систем. Поясним, что коллоидными называются системы, в которых в равновесии существуют – не разделяясь, но и не смешиваясь в одну, – две различные фазы: жидкость – жидкость (эмульсии), жидкость – твердое тело (суспензии), газ – твердое тело (дымы), газ – жидкость (туманы). Но были и ученые, которые считали, что полимеры представляют собой небольшие молекулы, объединенные в агрегаты клубкообразной формы, которые называли мицеллами (лат. mica – «частица», «крупинка»). Таким образом, полимеры были чем-то непонятным, зато хорошим и полезным.
История знает много примеров, когда свежая интересная теория предлагается сразу несколькими учеными, причем независимо друг от друга. Про это говорят: "Идея висела в воздухе". В случае с полимерами, что удивительно, это был всего лишь один (!) ученый. Новые идеи всегда пробиваются с трудом, что и произошло с наукой о полимерах. Расскажем о ее основоположнике подробнее.
Немецкий ученый-химик Г. Штаудингер (1881–1965) получил степень доктора наук в возрасте всего 22 лет, он продолжил свои исследования в органической химии под руководством Д. Тиле (его имя уже упоминалось в разделе "Лидер среди природных полимеров") в Страсбургском университете. В ходе исследований он открыл новый класс соединений R2C=C=O, названных кетенами. Во время Первой мировой войны Штаудингер подключился к решению хозяйственных задач страны: создал ароматизаторы – заменители натуральных продуктов (кофе, перца), которые во время войны были в дефиците. Кроме того, он не остался в стороне от политических вопросов, выходящих за рамки академической науки, и в 1917 г. опубликовал статью «Техника и война» (Technik und Krieg), где привел аккуратный подсчет промышленных потенциалов воюющих сторон. В обращении к немецкому имперскому Генеральному штабу он утверждал, что по результатам его расчета война уже фактически проиграна Германией и должна быть немедленно закончена, дальнейшее кровопролитие бессмысленно. Согласитесь, научный подход к подобным проблемам вызывает большее уважение, нежели политические лозунги о войне до победного конца? Такое смелое заявление противоречило имперскому духу Германии. Штаудингер был уволен с основного места работы и допрошен органами безопасности, позже увольнение отменили, поставив условие, что он не станет публично осуждать новую власть. Выезд из страны для участия в научных конференциях ему был запрещен.
Настоящий бойцовский характер Штаудингера проявился в 1920 г., когда он опубликовал статью "О полимеризации" (Über Polymerisation), где сформулировал сенсационное утверждение: полимеры – это длинные молекулы с очень большой молекулярной массой, он назвал их "макромолекулами", а реакцию, приводящую к их образованию, – "полимеризацией". С этого момента началась многолетняя вражда с классическими химиками-органиками, а также со специалистами по коллоидной химии. Они утверждали, что измеренные высокие молекулярные массы являются только кажущимися и представляют собой результат агрегации небольших молекул в коллоиды. Большинство коллег Штаудингера отказывались допустить, что маленькие молекулы могут объединяться друг с другом ковалентными связями с образованием высокомолекулярных соединений. Утверждение Штаудингера, что каучук, целлюлоза и многие другие подобные соединения представляют собой длинные цепочки из повторяющихся низкомолекулярных фрагментов, химики никак принять не могли.
Для доказательства своего утверждения Штаудингер привел результаты экспериментов. Например, натуральный каучук (о нем рассказано в разделе "Когда упорство выше знаний"), по мнению специалистов, представлял собой агрегат-мицеллу из отдельных молекул изопрена СН2=С(СН3) – СН=СН3, которые удерживаются вместе за счет притяжения между двойными связями. Логика Штаудингера была проста: если удалить двойные связи, удерживающие молекулы изопрена вместе, то каучук должен превратиться в жидкость, состоящую из одиночных молекул. Штаудингер гидрировал каучук, атомы водорода присоединились к двойным связям, которые после этого исчезли, но полученное вещество оставалось твердым продуктом, похожим по свойствам на натуральный каучук (рис. 1.57).
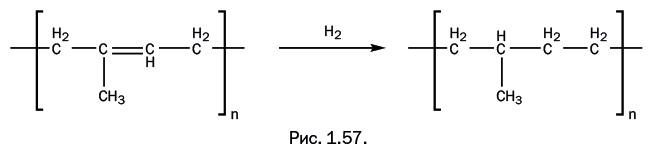
Аналогичное превращение он провел с полистиролом, получив подобный результат (рис. 1.58).
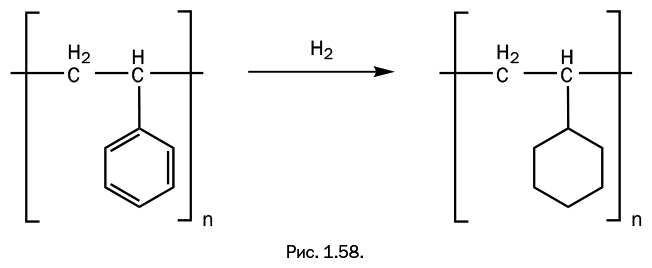
Штаудингер ввел в практику контроль молекулярной массы полимера с помощью вискозиметрии – измерение вязкости раствора полимера в органическом растворителе. Именно такой метод исследования показал, что полимеры – уникальные объекты. В случае если цепь полимера жесткая, вязкость раствора с концентрацией всего лишь 0,1–0,2 % может в 4–5 раз (!) превышать вязкость растворителя. Подобное не наблюдается ни для каких других веществ. Проводя химическую модификацию некоторых полимеров, ученый с помощью этого метода показал, что молекулярная масса практически не меняется.
Штаудингер заметно расширил представления о вариантах строения полимеров: он показал, что существуют разветвленные макромолекулы и полимерные сетки, которые образуются при трехмерной полимеризации. Таким образом, он смог предложить совершенно новый взгляд на крупную группу известных соединений.
В своей автобиографии Штаудингер писал: "Мои коллеги были очень скептически настроены по отношению к моей теории, и все, кто встречал мои прежние публикации в области низкомолекулярной химии (например, химия кетенов), спрашивали меня, почему я пренебрегаю этой интересной областью и продолжаю работать с плохо изученными и неинтересными соединениями вроде резины и синтетических полимеров". В то время химию этих соединений, благодаря их свойствам, часто называли химией смазок.
С середины 1930-х гг. макромолекулярная теория Штаудингера стала постепенно признаваться научным сообществом. В 1932 г. вышла классическая монография Г. Штаудингера "Высокомолекулярные органические соединения, каучук и целлюлоза", в которой была подробно описана его новая теория и результаты экспериментов. В 1940-е гг. при Фрайбургском университете был создан научно-исследовательский институт макромолекулярной химии, руководимый Штаудингером. За свои заслуги он получил многочисленные награды: медаль Эмиля Фишера Германского химического общества (1930), медаль Леблана Французского химического общества (1931), премию Станислава Канниццаро Итальянской национальной академии наук (1933) и другие.
Тем не менее сложности с продвижением новой науки не закончились, причем это было результатом упорства самого Штаудингера, который уже, вероятно, не представлял себя вне привычной обстановки "сражений". Он утверждал, что полимеры – прямые гигантские молекулы, которые не гнутся и не сворачиваются (по современной терминологии – жесткоцепные), однако эксперименты показывали, что существуют и гибкоцепные – сворачивающиеся в клубки. Видимо, они напоминали Штаудингеру "ненавистные" мицеллы, и он категорически отвергал такие взгляды. В результате в лагере "полимерщиков" разгорелись споры, что, естественно, затормозило принятие новой науки широкой ученой общественностью. Косвенным результатом этих событий было следующее: Штаудингер многократно был номинирован на Нобелевскую премию, но получил ее только в 1953 г., то есть спустя более чем тридцать лет после появления этой новой области химии.
Среди заслуг Штаудингера, основавшего новую науку, почти незаметным осталось одно его достижение: в 1920-х гг. он создал полимер, который в то время не получил промышленного развития. Но в наши дни это один из широко применяемых пластиков – речь идет о полимеризации формальдегида H2C=O (рис. 1.59).
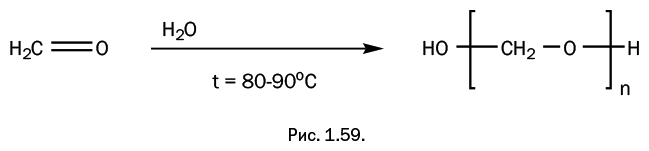
Полиформальдегид (его второе название полиоксиметилен), полученный Штаудингером, имел молекулярную массу в пределах 100 000 и представлял собой полимер с высокой механической прочностью. Однако при температуре свыше 120 оС он начинал разлагаться. Причиной этого были концевые гидроксильные группы, которые при нагревании начинали «откусывать» фрагменты полимерной цепи в виде низкомолекулярных продуктов (рис. 1.60).
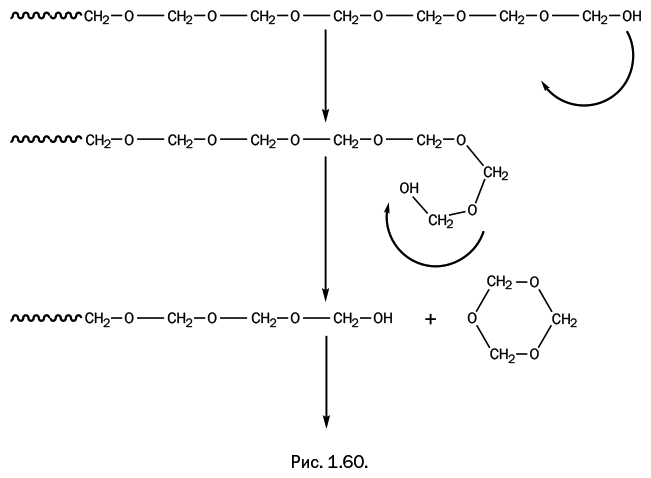
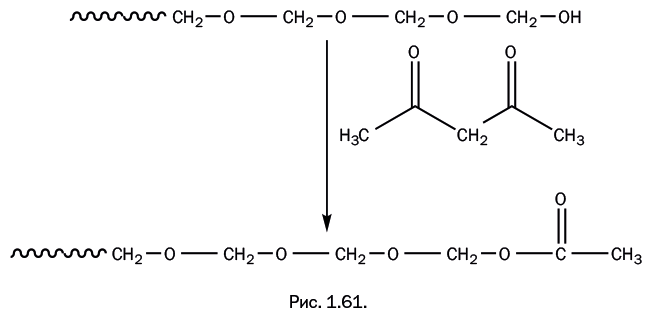
Во времена Штаудингера подобные процессы не изучались, но позже был найден простой способ предотвратить подобный распад полимерной цепи. Концевые гидроксильные группы заблокировали, переведя их в ацетатные действием уксусного ангидрида (рис. 1.61).
В настоящее время полиформальдегид используется как заменитель цветных металлов при изготовлении редукторов с зубчатыми передачами, в качестве вкладышей в подшипниках скольжения, а также деталей автомобилей, корпусов бытовой техники и электротехнических изделий. Кроме того, полиформальдегид физиологически безвреден, устойчив к дезинфекции, стерилизации и потому применим в пищевом и медицинском оборудовании.
Завершая главу о полимерах, подведем итоги. Существует основной признак, который всегда указывают при определении того, что такое полимер. Это вещество, молекулы которого собраны в цепь из повторяющихся звеньев и имеют большую молекулярную массу. Именно эту особенность строения Штаудингер положил в основу новой науки о полимерах. Кроме того, он установил, что полимерные цепи могут быть линейными, разветвленными или сшитыми.
Итак, для решения вопроса необходимо экспериментально определить молекулярную массу, но с какой величины начинаются полимеры? Обычно от десятков тысяч до нескольких миллионов. Однако граница очень размыта – ведь у каждого типа полимеров может быть своя величина. Если молекулярная масса невелика, то вещество называют олигомером (греч. ὀλίγος – "незначительный"). Например, вазелиновое масло содержит до двадцати звеньев -СН2-, оно имеет тот же состав, что и полиэтилен, но из вазелинового масла не удастся получить пленку или волокно.
Самое интересное, что для того, чтобы определить, относится ли конкретное вещество к полимерам, совсем не обязательно определять молекулярную массу. Полимеры имеют набор свойств, заметно их отличающих от остальных материальных объектов.
В отличие от низкомолекулярных веществ, имеющих четко выраженную температуру плавления, полимеры при нагревании постепенно размягчаются.
Полимеры способны образовывать волокна, нити и пленки. "А металлические нити?" – возразит читатель. Действительно, многие металлы пластичны: например, из 1 г серебра можно вытянуть проволоку длиной более 100 м, но ткань из металлических волокон очень заметно отличается от обычных тканей, так что сходство это просто формальное.
Высокоэластичность – способность некоторых полимеров растягиваться на 500–600 % от первоначальной длины и после снятия нагрузки возвращаться в исходное состояние. Но ведь то же самое делают стальные пружины? Но если сравнить полоску резины и металлическую полоску, то различие будет очевидно.
У растворов полимеров весьма низкой концентрации (0,1–0,2 %) вязкость в несколько раз превосходит вязкость чистого растворителя.
При набухании сшитого полимера (например, вулканизованного каучука) в органическом растворителе объем "впитавшегося" растворителя может в десять раз превышать объем самого полимера.
Не все из перечисленных свойств присущи каждому полимеру: обычно у конкретного образца два-три определяющих свойства. И если таковые обнаружены, есть основания рассматривать вещество как полимерное. Фактически мы упомянули некоторые экспериментальные приемы, используемые при изучении полимеров.
Термин "полимер" иногда употребляется слишком вольно: например, кристаллы кварца SiO2 при желании можно назвать трехмерным сшитым полимером. Однако химики-полимерщики прекрасно знают об отличительных особенностях полимеров, ориентируясь на перечисленные выше основные свойства.
Воздадим должное Штаудингеру – он первым выделил полимеры в особый, самостоятельный класс веществ и указал методы их изучения.
Назад: Традиция, логика, расчет
Дальше: Глава 2 Биохимия тоже химия

