Книга: Пять литров красного. Что необходимо знать о крови, ее болезнях и лечении
Назад: Глава 21 «Доктор, почему я заболел?» Причины возникновения рака: реальность и мифы
Дальше: Глава 23 Заболевания лимфатической системы. Кто такой Томас Ходжкин?
Глава 22
«Доктор, я умру?» Острые лейкозы
У медицинских работников есть расхожая фраза: «Все когда-то умрут от рака, просто не все до него доживают». За последние десятилетия медицина действительно шагнула далеко вперед и, как следствие, средняя продолжительность жизни значительно увеличилась, а вслед за этим наблюдается увеличение заболеваемости злокачественными заболеваниями. И, несмотря на все достижения современной медицины, по данным ВОЗ, злокачественные заболевания являются второй по частоте причиной смертности на Земле. Каждая шестая смерть связана с онкологическим заболеванием.
У многих из нас при упоминании гематологических болезней (рака крови, хотя мы уже разобрались, что так говорить неграмотно) всплывает образ из кино, где показано, как лысеющий и худой пациент отчаянно борется со своим заболеванием и в конце обязательно умирает («Умереть молодым», 1991; «Сладкий ноябрь», 2001; «Спеши любить», 2002; «Сейчас самое время», 2012; «Я, Эрл и умирающая девушка», 2015).
На самом деле каждый случай индивидуален и все может закончиться иначе. Я намеренно буду избегать приводить статистические данные по выживаемости при каждом заболевании, потому что, во-первых, эти данные устареют сразу после выхода книги, во-вторых, при различных методах терапии и в разных стадиях болезней выживаемость кардинально отличается и, в-третьих, не хотелось бы, чтобы книга превратилась в многотомный труд по гематологии. Моя основная задача – познакомить вас с основными симптомами каждой болезни, необходимыми обследованиями и существующими методами терапии.
Как уже было сказано, все гемобластозы можно разделить на лейкозы и лимфомы. Лейкозы, в свою очередь, делятся на хронические и острые, а лимфомы – на индолентные (вялотекущие) и агрессивные формы. Еще есть разделение по принадлежности к отделу кроветворения: миелоидные и лимфоидные.
Лейкоз – это опухоль кроветворной ткани с первичным поражением или опухолевым ростом в костном мозге. А острые лейкозы представляют собой опухолевые заболевания кроветворной ткани, связанные с мутацией в клетке-предшественнице гемопоэза, следствием которой становятся блокировка процессов дальнейшей дифференцировки и бесконтрольное деление незрелых миелоидных клеток (бластов),.
Термин «острый лейкоз» введен в 1889 году немецким врачом Вильгельмом Эбштайном (1836‒1912), чтобы разделить быстро развивающиеся лейкозы со смертельным исходом и относительно медленно текущие хронические лейкозы. Замечу, кстати, что в англоязычной литературе до сих пор используется термин leukemia, а вот в отечественной медицинской литературе закрепился термин «лейкоз».
Острые лейкозы считаются редкими заболеваниями. Как говорилось выше, есть два основных типа таких заболеваний. Первым – острым миелоидным лейкозом – заболевают в среднем 3–5 человек на 100 тысяч населения в год. При этом заболеваемость резко возрастает в возрастных группах старше 60 лет и составляет 12–13 случаев на 100 тысяч населения у лиц в возрасте старше 80 лет. Пик заболеваемости приходится на 65‒67 лет. Исходя из расчетного показателя заболеваемости (по данным европейских и американских исследователей), при численности населения России 146,2 миллиона человек число заболевающих в год должно составлять примерно 6000,.
Второй тип – острый лимфобластный лейкоз (ОЛЛ) – напротив, самая распространенная опухоль кроветворной ткани у детей, на ее долю приходится до 30 % всех злокачественных опухолей в детском возрасте. У пациентов моложе 15 лет ОЛЛ диагностируется в 75 % случаев всех острых лейкозов. Пик заболеваемости ОЛЛ приходится на возраст 3–4 года, затем частота его снижается, и второй подъем, хотя не столь существенный, отмечается в возрасте 50–60 лет. Заболеваемость в среднем составляет 1–2 случая на 100 тысяч населения,.
Можно сказать, что миелоидные лейкозы – это болезнь пожилых, а лимфобластные, наоборот, детей.
Классификация острых лейкозов не ограничивается разделением на миело– и лимфобластные; согласно общепринятой классификации ВОЗ 2016 года, выделяют более 30 их разновидностей. Виды лейкозов сильно отличаются друг от друга происхождением, тактикой лечения и прогнозом.
Клинические проявления острого лейкоза
Острый лейкоз характеризуется недостаточностью костномозгового кроветворения и признаками опухолевого роста в организме.
Нормальная кроветворная ткань в костном мозге замещается опухолевыми клетками, состоящими из стволовых клеток опухоли и «зрелых» опухолевых клеток, которые завершили созревание на уровне бластов.
Костный мозг перестает создавать клетки крови, а значит, возникают анемия, нейтропения и тромбоцитопения различных степеней тяжести. Они, как правило, и служат поводом для обращения за медицинской помощью.
Соответственно, симптомы острого лейкоза будут такими же, как при перечисленных ранее «-пениях»: слабость, спонтанное появление синяков, лихорадка и потеря веса без повода, частые инфекции, безболезненные уплотнения в шее, подмышках, животе или паху – все те же неявные недомогания, на которые люди, как правило, долго не обращают внимания.
Абсолютный критерий острого лейкоза – наличие более 20 % бластных клеток в крови или костном мозге.
Кроме поражения костного мозга, при остром лейкозе можно обнаружить внекостномозговые очаги поражения: увеличение лимфатических узлов, селезенки, печени, а также любых других органов и тканей.
Бластные клетки делятся очень быстро, и их число увеличивается буквально ежеминутно в геометрической прогрессии. Если вчера, например, у пациента было 10 тысяч лейкоцитов на 1 мкл, сегодня – 20 тысяч на 1 мкл, завтра – уже 40 тысяч на 1 мкл. Если не предпринять меры, наступает такое угрожающее жизни состояние, как лейкостаз или лимфостаз: количество лейкоцитов превышает 200–300 тысяч на 1 мкл (при верхней границе 9000 на 1 мкл), они застаиваются в сосудах и не дают нормально двигаться другим клеткам крови.
Без лечения острый лейкоз быстро приводит к летальному исходу. Такой большой объем опухолевых клеток может сочетаться с наличием симптомов опухолевой интоксикации: потерей массы тела, повышенной потливостью, подъемом температуры (лихорадкой), поэтому в случае подозрения на эту группу заболеваний необходимо как можно раньше начать специфическое лечение, ситуация может поменяться за считаные часы.
По современным нормативам мы должны начать лечение пациентов с острым лейкозом в течение 72 часов после постановки диагноза. В нашей клинике, когда возникает такая ситуация, мы сразу же госпитализируем человека или, если у нас нет мест, вызываем скорую и отправляем в другой стационар. Иногда мы сталкиваемся с так называемыми отказниками – людьми, которые не понимают всю серьезность ситуации. К счастью, это случается очень редко, но все-таки бывает: человек, например, говорит, что не может сейчас лечиться, потому что у него кредиты, работа, завтра экзамен у ребенка или что-то аналогичное. Заканчивается это промедление, конечно же, плачевно, потому что действовать при остром лейкозе надо так же оперативно, как, например, при острой инфекции.
Диагностика острого лейкоза
Итак, мы разобрались, что чаще всего становится причиной для обращения к гематологу, и дальше необходимо определиться с диагностикой острого лейкоза. Эти же методы применяются в дальнейшем для оценки эффективности терапии и контроля ремиссии заболевания.
И здесь нам пригодятся знания, полученные в ходе прочтения предыдущих глав:
1. В первую очередь необходимо выполнить клинический анализ крови для определения степени анемии, нейтропении и тромбоцитопении, а также для подсчета количества бластов.
2. При обнаружении бластных клеток в крови следующим шагом будет аспирационная биопсия костного мозга, которая проводится в первую очередь для подсчета всех типов клеток – миелограммы.
3. Следующим исследованием образца костного мозга будет цитохимический тест – с помощью специальных красителей выясняют, к какому типу (миелоидный или лимфоидный) относятся обнаруженные бластные клетки.
4. Затем выполняется стандартное цитогенетическое исследование.
5. После этого проводится иммунофенотипирование посредством проточной цитофлуорометрии. Эта методика позволяет получить комплексную информацию о множестве клеток зараз. С ее помощью можно узнать размер клетки, содержание ДНК или РНК и многие другие параметры. В гематологии подобный вид диагностики применяется для определения типа опухолей, лейкозов, лимфом. Сопоставляя данные иммунофенотипирования и других исследований, мы можем сделать заключение о происхождении опухоли. Это крайне важно для определения тактики лечения и дальнейшего наблюдения.
6. И последнее – проведение тестов FISH или ПЦР в реальном времени (клеток костного мозга или периферической крови) для идентификации предполагаемых генетических аномалий, ассоциированных с данным вариантом острого лейкоза.
После проведенных анализов приступают к оценке объема опухолевых клеток в организме. С помощью уже знакомых вам УЗИ, КТ и МРТ мы разыскиваем симптом «плюс ткань», то есть опухолевые образования, в различных органах; исследуем, как работают органы и системы тела, и обязательно делаем спинномозговую (люмбальную) пункцию с исследованием ликвора (спинномозговой жидкости) на предмет наличия в нем бластных клеток. Если мы обнаруживаем их присутствие в ликворе, то есть убеждаемся, что поражена центральная нервная система, это значит, что вводить химиопрепараты нужно будет интратекально – под оболочку спинного мозга, иначе убить опасные клетки в ликворе практически невозможно.
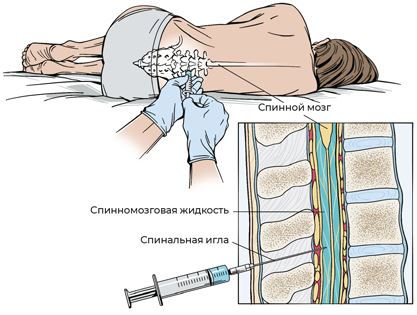
Рис. 24. Выполнение люмбальной пункции
И только после полноценного обследования и определения тактики можно переходить к лечению, которое заключается в максимальном подавлении опухолевого клона и достижении ремиссии.
Общепринятой системы стадирования в широком понимании (как в общей онкологии) для острых лейкозов не существует. Вместо стадий можно выделить три состояния для этого заболевания: впервые установленный острый лейкоз, ремиссия и рецидив.
Со впервые обнаруженным лейкозом все понятно: он диагностирован – раньше не было, теперь есть. А что такое ремиссия? Давайте будем использовать этот термин в отношении большинства онкологических заболеваний. Ремиссия – это такое состояние, при котором мы не можем современными методами диагностики поймать даже минимальное количество опухолевых клеток. Оно может называться другим, модным термином – «минимальная остаточная болезнь» (МОБ). Полностью удалить опухолевые клетки из организма, к сожалению, пока невозможно. И мы знаем, что они прячутся где-то в глубине лимфатических узлов или костного мозга. Находиться в спящем режиме они могут годами, и при каких-то неблагоприятных условиях возможна их повторная активация. Это называется рецидив. Тогда лечение придется повторить – вернее, назначить новое, потому что при каждом новом рецидиве оно может отличаться.
В основном лечение острого лейкоза заключается в применении высоких доз химиопрепаратов. Честно говоря, протоколы химиотерапии при острых лейкозах мало изменились за последние 30‒40 лет, за исключением некоторых случаев, когда возможно применение таргетных (узконаправленных, «прицельных») препаратов: ингибиторов (подавителей активности) протеинкиназ, моноклональных антител – о них мы поговорим позже.
Объем и характер противоопухолевой химиотерапии определяют на основании типа и варианта острого лейкоза и общего состояния пациента (учитывается состояние всех систем организма, в особенности наличие прочих болезней).
Радикальная химиотерапия предполагает лечение для полного уничтожения опухоли. Причем задача терапии не только достичь ремиссии, но и закрепить ее, поддерживая как можно более долгое время.
Давайте на примере миелобластного острого лейкоза рассмотрим, как может проходить лечение.
 Индукция – первая часть лечения: с помощью высоких доз химиопрепарата мы добиваемся полной ремиссии.
Индукция – первая часть лечения: с помощью высоких доз химиопрепарата мы добиваемся полной ремиссии. Консолидация – курс закрепления результатов, в рамках которого также вводятся массивные дозы химиопрепаратов.
Консолидация – курс закрепления результатов, в рамках которого также вводятся массивные дозы химиопрепаратов. Режим мониторинга – как правило, после первых двух этапов мы переходим к режиму контроля состояния организма. Это значит, что или человек регулярно сдает анализы крови, или, помимо этого, периодически проводится аспирационная биопсия костного мозга. Хотя пациенту обычно рекомендуется пить поддерживающие химиопрепараты, иногда в особо благоприятных случаях удается отказаться от их продолжительного приема. Мы стремимся именно к такому результату: чтобы пациент по возможности избежал продолжительного приема «химии», потому что препараты, как вы помните, дают побочные эффекты и могут снижать качество жизни.
Режим мониторинга – как правило, после первых двух этапов мы переходим к режиму контроля состояния организма. Это значит, что или человек регулярно сдает анализы крови, или, помимо этого, периодически проводится аспирационная биопсия костного мозга. Хотя пациенту обычно рекомендуется пить поддерживающие химиопрепараты, иногда в особо благоприятных случаях удается отказаться от их продолжительного приема. Мы стремимся именно к такому результату: чтобы пациент по возможности избежал продолжительного приема «химии», потому что препараты, как вы помните, дают побочные эффекты и могут снижать качество жизни.При миелобластных же лейкозах пациенты пожизненно должны принимать таргетные препараты, чтобы болезнь не вернулась (к счастью, этот вид препаратов на качество жизни не влияет – они не дают значимых побочных эффектов).
Также крайне важно определиться на ранних этапах с возможностью проведения аллогенной трансплантации костного мозга (то есть пересадки от стороннего донора). Желательно найти такого донора и вырабатывать дальнейшую стратегию в зависимости от наличия этой опции. Казалось бы, если есть вариант трансплантации, зачем «травиться» химиопрепаратами? Мы позже подробнее поговорим о процедуре трансплантации: это непростая операция, которая имеет ряд побочных эффектов. Обычно в случае с острыми лейкозами, если все складывается хорошо (химиотерапия эффективна, донор найден, человек активно движется к выздоровлению), мы закрепляем результаты химиотерапии аллогенной пересадкой, то есть сначала заболевание вводится в ремиссию с помощью препаратов, потом проводится пересадка.
В чем же состоит прогресс в лечении острых лейкозов? В основном в применении более современных методов сопроводительной терапии: заместительной, антибактериальной, противорвотной и других. И вот именно здесь важен опыт врача и оснащенность медицинского центра, потому что в лечении острых лейкозов важен процесс выхаживания после проведенной высокодозной химиотерапии, когда пациент находится в аплазии (полное отсутствие клеток костного мозга: анемия, нейтропения, тромбоцитопения).
У таких пациентов, грубо говоря, нет иммунитета – они беззащитны перед инфекциями. Поэтому раньше, когда в распоряжении врачей была лишь одна комбинация антибиотиков (пенициллин+стрептомицин), человек мог подхватить инфекцию и погибнуть от нее, потому что у болезнетворных бактерий выработалась к этим лекарствам резистентность. Сейчас каждый год появляются новые антибиотики, которые борются со все более и более «умными» и сильными бактериями. Также раньше не было противовирусных и мощных противогрибковых препаратов, которые сегодня помогают пройти через процесс восстановления после «химии» и пересадки костного мозга.
Еще один фактор прогресса – противорвотные препараты. Коллеги, которые старше меня на 20‒30 лет, рассказывают, какие ужасные побочные эффекты давала химиотерапия раньше. Они заранее предупреждали пациентов, что тех будет безостановочно рвать в течение недели и это неизбежно. Сейчас разработаны современные противорвотные препараты, благодаря которым у человека остается только чувство тошноты, но не бывает неукротимой рвоты, которая выматывала бы и его самого, и его родственников, и медицинский персонал.
Как я уже сказал, прогноз и выживаемость сугубо индивидуальны и зависят от слишком большого количества факторов, поэтому каждый случай необходимо обсуждать отдельно. Важно понимать, что острый лейкоз – это жизнеугрожающее состояние, которое без лечения очень быстро приводит к смерти.
Основные моментыОстрый лейкоз – это быстро прогрессирующее злокачественное заболевание крови, при котором происходит поражение костного мозга бластными клетками.
Лейкоз может приводить к развитию анемии, тромбоцитопении и нейтропении.
Существует большое количество видов лейкозов.
Основные симптомы заболевания проявляются в виде слабости, лихорадки, образования синячков и кровотечений, возможно увеличение лимфатических узлов и поражение других органов.
Для подтверждения диагноза «острый лейкоз» обязательно исследование крови и костного мозга.
На прогноз (шанс выздоровления) и тактику лечения влияет большое количество факторов.
Назад: Глава 21 «Доктор, почему я заболел?» Причины возникновения рака: реальность и мифы
Дальше: Глава 23 Заболевания лимфатической системы. Кто такой Томас Ходжкин?

