Лекция IV
Водород в свече. Водород сгорает и превращается в воду. Другая составная часть воды – кислород
Я вижу, вам еще не надоела свеча, иначе вы бы не стали проявлять столько интереса к этой теме. Когда наша свеча горела, мы убедились, что она дает в точности такую же воду, к какой мы привыкли в повседневной жизни. При дальнейшем исследовании этой воды мы нашли в ней интересное вещество – водород. Это легкое вещество у нас сейчас вот здесь, в банке. Затем мы убедились в горючести водорода, а также в том, что он дает воду. Помнится также, что я познакомил вас вкратце с одним аппаратом, который я охарактеризовал как некий химический источник энергии или силы, устроенный так, чтобы по этим проводам передавать нам свою энергию. Тогда же я сказал, что употреблю эту энергию для того, чтобы разложить воду на части, так сказать, разорвать ее на куски, с целью узнать, что же, кроме водорода, содержится в воде. Ведь вы помните, когда мы пропускали водяной пар сквозь железную трубку, мы получали очень значительное количество газа, но отнюдь не столько по массе, сколько мы туда впускали воды в виде пара. Теперь нам предстоит выяснить, каково то, другое вещество, которое там имеется.
Давайте проделаем несколько опытов, чтобы вы могли разобраться, что собой представляет этот прибор, т. е. батарея, и для чего она употребляется, Прежде всего давайте приведем в соприкосновение некоторые известные нам вещества, а затем посмотрим, какое воздействие на них окажет батарея. Вот медь (обратите внимание на различные видоизменения, в которых она может существовать), а вот азотная кислота; вы увидите, что она, обладая вообще очень сильным химическим действием, будет весьма энергично действовать на медь. Вот она испускает красивые рыжие пары, но так как эти пары нам будут только мешать, мистер Андерсон некоторое время подержит колбу около вытяжной трубы, чтобы нам досталась польза и красота этого опыта без его неприятной стороны. Медь, которую я положил в эту колбу, растворится и при этом превратит кислоту с водой в голубую жидкость, содержащую медь и другие вещества; затем я покажу вам, какое действие окажет электрическая батарея на эту жидкость.
А пока мы проведем другой опыт, чтобы вы могли увидеть, каковы возможности этой батареи. Вот здесь вещество, которое для вас неотличимо от воды. Подобно воде, оно содержит какие-то еще не известные нам вещества. Этим раствором некоей соли я могу пропитать бумажку, а затем подвергну ее действию нашей батареи, и мы посмотрим, что получится. Произойдет несколько существенных явлений, которыми мы и воспользуемся для дальнейших рассуждений.
Бумажку, пропитанную раствором, я кладу на лист станиоля, во-первых, чтобы она не испачкалась, а во-вторых, чтобы удобнее было подводить электрическую энергию. Как вы видите, этот раствор не претерпевает никаких изменений ни от того, что мы его поместили на станиоль, ни от чего бы то ни было другого, с чем я до сих пор приводил его в соприкосновение; таким образом, он вполне пригоден для испытания действия батареи. Но сперва проверим, в порядке ли наша батарея, продолжает ли она находиться в том же состоянии, как прошлый раз. Это легко можно выяснить. Вот провода; я сближаю их концы, но пока еще энергии нет, потому что отключены те пути для электричества, которые мы называем электродами. (На концах проводов происходит внезапная вспышка.)
Ага! Вот мистер Андерсон подал мне сигнал, что все готово. Прежде чем мы приступим к нашему опыту со смоченной бумажкой, я попрошу его снова разомкнуть цепь батареи, а здесь мы соединим полюса платиновой проволочкой. Если теперь окажется, что нам удастся раскалить током эту довольно длинную проволочку, мы сможем спокойно приступить к своему опыту со смоченной бумажкой. Сейчас вы увидите, какова энергия нашей батареи. (Ассистент включает цепь, и соединительная проволочка раскаляется докрасна.) Смотрите, как прекрасно передается энергия через эту проволочку, причем я нарочно взял тонкую, чтобы показать вам, с какой мощной силой мы имеем дело. Теперь, располагая этой энергией, мы ее применим к исследованию воды.
Вот два кусочка платины; если я их положу на эту бумажку (смачивает бумажку раствором), то никакой реакции, как видите, не произойдет; и если я их опять сниму, все останется, как было, без малейших изменений. Теперь следите за тем, что будет происходить: если я прикоснусь каким-нибудь из этих двух полюсов к платиновой пластинке, то по отдельности ни тот, ни другой не окажут ровно никакого действия. Однако если я сделаю так, чтобы они одновременно оба касались платины, смотрите, что получается, (под обоими полюсами появилось по бурому пятну.) Видите, какой результат; вы можете убедиться, что я из белого вещества выделил что-то бурое.
Теперь я все это расположу несколько иначе… вот так… и один из полюсов приложу снизу к станиолю, подстилающему бумагу, ну, теперь получается такое чудесное действие тока на бумагу, что надо попробовать, не удастся ли мне что-нибудь написать таким способом своего рода телеграмму. (Лектор вывел на бумаге концом одного из проводов слово «молодежь».) Вот какие интересные результаты у нас получаются!
Вы видите, что из этого раствора мы извлекли нечто такое, о чем раньше и не подозревали. Теперь возьмем вот эту колбу у мистера Андерсона и посмотрим, что мы можем получить отсюда. Это ведь та жидкость, которую мы сегодня приготовили из меди и азотной кислоты за то время, пока занимались другими опытами. И хотя получена она в спешке и, может быть, опыт с ней у меня не вполне удастся, но я предпочитаю приготовлять ее не заранее, а у вас на глазах, чтобы вы могли видеть, что я делаю.
Теперь смотрите, что будет происходить. Пусть эти две платиновые пластинки служат полюсами батареи, я потом соединю их с проводами. Я собираюсь привести их в соприкосновение с раствором, как мы это только что делали на бумаге. Для нас все равно, находится ли раствор на бумаге или в банке, лишь бы мы подвели к нему полюса батареи. Если я погружу в раствор эти платиновые пластинки сами по себе (лектор погружает их в жидкость, не соединяя с батареей), то выну их такими же чистыми и белыми, какими их туда опустил. Однако когда мы привлечем к делу энергию батареи (соединяет платиновые пластинки с батареей и вновь опускает их в раствор), смотрите, вот эта пластинка (показывает пластинку) сразу как будто превращается из платины в медь. Видите, она стала как медная, а вот та (показывает другую) совсем чистая, как была. Если же я возьму и поменяю полюса батареи, налет меди переместится с одной пластинки на другую: та пластинка, которая только что была покрыта медью, окажется чистой, а чистая покроется налетом меди. Итак, вы видите что ту самую медь, которую мы ввели в этот раствор, мы можем и извлечь из него при помощи батареи.
Отставим этот раствор и посмотрим, какое действие батарея будет оказывать на воду. Вот две платиновые пластинки, которые я сделаю полюсами батареи, а это сосуд. Я могу разобрать его на части и показать вам его устройство. В эти две чашечки (А и В) я наливаю ртуть, так что она будет находиться в контакте с концами проводов, соединенных с платиновыми пластинками. В сосуд С я наливаю слегка подкисленную воду (кислота прибавляется только для облегчения реакции, и сама она при этом не претерпевает никаких изменений). В пробку сосуда С вставлена изогнутая стеклянная трубка D, она подведена под банку F и она. может быть, напомнит вам отводную трубку, присоединенную к трубке с железными стружками в том опыте с печью, который мы проделывали в прошлый раз. Вот я собрал прибор, и мы теперь попытаемся так или иначе воздействовать на воду.
Прошлый раз я пропускал водяной пар сквозь трубку, раскаленную докрасна; теперь же я буду пропускать электрический ток сквозь содержимое этого сосуда. Может статься, я при этом вскипячу воду; в таком случае я получу пар, а вы знаете, что пар при остывании сгущается, и, таким образом, вы сможете судить, вскипятил я воду или нет. Но может статься, что, пропуская электрический ток сквозь воду, я не вскипячу ее, а получу какой-нибудь другой результат. Об этом вы сможете судить на основании опыта.
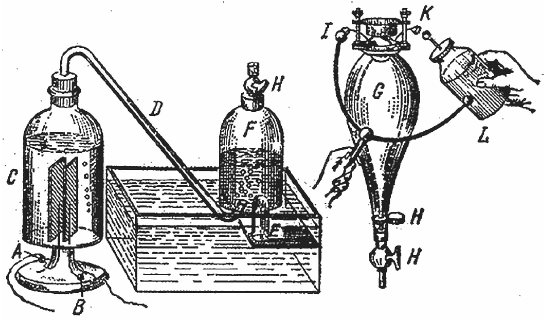
Две платиновые пластинки, которые служат полюсами батареи. При погружении их в раствор происходит реакция в зависимости от того, используется ли их энергия
Один провод я присоединю к А, другой к В, и вы скоро увидите, останется ли вода спокойной. Кажется, что вода вовсю кипит; но кипит ли она на самом деле? Давайте проверим, что оттуда выходит водяной пар или нет? Я думаю, вы скоро увидите, что банка наполнится парами, если то, что поднимается пузырьками из воды, представляет собой пар. Но пар ли это? Ну, конечно, нет. Ведь вы же видите, что это нечто остается неизменным. Оно не превращается в воду, и потому это никак не может быть паром; это, очевидно, какой-то устойчивый газ. Так что же он собой представляет? Водород? Или что-нибудь другое?
Что ж, испытаем его. Если это водород, он должен гореть. (Тут лектор зажигает некоторое количество собравшегося газа, который сгорает со взрывом.) Несомненно, это что-то горючее, но горит оно не так, как водород. Тот бы не дал такого шума; однако свет при горении этого газа был по цвету похож на водородное пламя.
Впрочем, этот газ способен гореть и без доступа воздуха. Вот почему я собрал еще один прибор, приспособленный для того, чтобы сделать опыт более тщательно. Вместо открытого сосуда я взял закрытый. Я хочу показать вам, что этот газ, каков бы он ни оказался, может гореть без воздуха; в этом отношении он отличается от свечи, которая без воздуха гореть не может. Проделаем мы это следующим образом. Вот стеклянный сосуд (G), в который впаяны две платиновые проволочки (I и К), к ним я могу подвести электрический ток. Мы можем соединить этот сосуд с воздушным насосом и выкачать из него воздух, а затем поставить его на банку, соединить с ней и впустить в него тот газ, который образовался в результате воздействия батареи на воду; можно сказать, что мы получили его, превратив в него воду, я вправе употребить такое выражение и сказать, что мы действительно, по ходу нашего опыта, превратили воду в этот газ.
Мы не только изменили ее состояние, но по-настоящему превратили воду в это газообразное вещество; и вся вода, которая была при этом опыте разложена, находится тут, в банке. Вот я привинчиваю к банке F сосуд О, тщательно соединяю их трубки кранами Н, Н, Н, и если вы будете следить за уровнем воды в банке F, вы заметите, что он повысится, когда я открою краны (Н, Н, Н), т. е. газ из этой банки поднимется в верхний сосуд. Теперь я закрою эти краны, так как сосуд О уже наполнился газом. Перенеся его для безопасности в эту камеру, я пропущу через него электрическую искру от лейденской банки L. Сосуд сейчас совершенно прозрачный, а после взрыва он затуманится. Стенки его настолько толсты, что звука слышно не будет. (Через сосуд пропускается электрическая искра, поджигающая взрывчатую смесь.) Вы видели этот яркий свет?
Я снова привинчу сосуд О к банке F, открою краны, и вы убедитесь, что уровень воды в банке вторично повысится. (Краны открываются.) Как видите, эти газы исчезли. (Лектор имеет в виду газы, первоначально собранные в банке и только что зажженные электрической искрой.) В сосуде их место освободилось, и в сосуд вошла новая порция газа. Из вспыхнувших газов образовалась вода. Если мы все повторим (делает опыт снова), у нас опять получится пустота, в чем вы убедитесь по подъему воды в банке F. После взрыва у меня всегда оказывается пустой сосуд, потому что тот пар или газ, в который мы при помощи батареи превратили воду в банке С, взрываясь от искры, превращается в воду. И действительно, через некоторое время вы увидите, как капельки воды будут понемногу стекать по стенкам этого верхнего сосуда и собираться на дне.
Здесь мы имели дело с водой совершенно безотносительно к атмосфере. Вода; содержащаяся в свече, образовалась в свое время при участии атмосферы. А таким путем, как сейчас, воду можно получать независимо от воздуха. Значит, в воде должно содержаться также и то другое вещество, которое горящая свеча берет из воздуха и которое, соединяясь с водородом, дает воду.
Вы только что видели, как один из полюсов нашей батареи с помощью вот этого провода притягивал к себе медь, извлекая ее из сосуда с голубым раствором. И, конечно, мы вправе задать себе такой вопрос: если батарея имеет такую власть над раствором металла, который мы сами можем приготовить и разложить, то не окажется ли возможным разложить воду на составные части и отделить их друг от друга? Посмотрим, что произойдет с водой вот в этом приборе, где металлические концы батареи далеко разнесены. Один провод я присоединяю тут, у А, другой там, у В. На каждый полюс можно надеть по маленькой подставке с отверстием, для того чтобы надежно разделить газы, выделяющиеся на полюсах (ведь вы убедились, что из воды у нас получается не водяной пар, а газы).
Ну, вот, теперь провода присоединены надлежащим образом к сосуду с водой, и вы видите, как пузырьки идут вверх. Давайте соберем эти пузырьки и выясним, из чего они состоят. Вот стеклянный цилиндр О; я наполняю его водой, опрокидываю и ставлю его над полюсом А, другой цилиндр, Н, я таким же образом помещаю над полюсом В. Теперь у нас сдвоенный прибор для получения газа на обоих полюсах. Оба эти цилиндра будут наполняться газом. Вот, пошло дело! Правый цилиндр Н наполняется очень быстро, а левый, О, не так быстро.
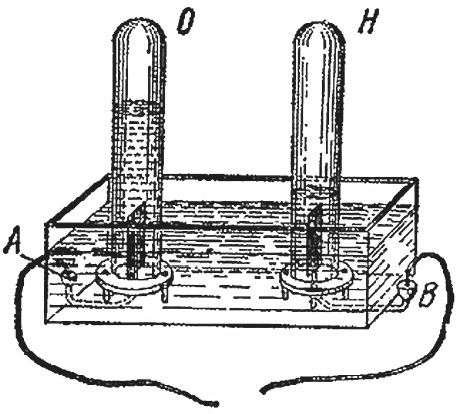
Один из полюсов батареи с помощью провода притягивает к себе медь, извлекая ее из сосуда с раствором
Хотя я и упустил несколько пузырьков, но видно, что реакция протекает равномерно; и если бы не то обстоятельство, что цилиндры не совсем одинаковые, вам было бы видно, что здесь в цилиндре Н, газа вдвое больше, чем там, в цилиндре О. Оба эти газа бесцветны; они находятся над водой, не конденсируясь; они одинаковы по всем признакам я хочу сказать, по всем видимым признакам; однако мы должны исследовать эти вещества и выяснить, что они собой представляют. Каждого газа у нас помногу, и нам легко делать с ними опыты.
Начнем с цилиндра H, я надеюсь, вы скоро поймете, что в нем содержится водород. Вспомните все свойства водорода: это легкий газ, хорошо сохраняющийся в опрокинутых сосудах, горящий бледным пламенем у края банки. Проверьте, удовлетворяет ли наш газ всем этим условиям. Если это водород, он останется здесь, в цилиндре, который я держу опрокинутым. (Лектор подносит к цилиндру горящую лучинку, и водород загорается.)
Ну, а что же находится в другом цилиндре? Вы знаете, что оба газа вместе дают взрывчатую смесь. Но что же представляет собой вторая составная часть воды и благодаря которой, следовательно, горит водород? Мы знаем, что вода, налитая нами в сосуд, состояла из совокупности этих двух веществ. Мы убедились, что одно из них водород; но что же представляет собой второе вещество, которое до опыта находилось в воде, а теперь есть у нас в изолированном виде? Я введу в этот газ зажженную лучинку. Сам газ не будет гореть, но он заставит гореть лучинку (вносит в газ зажженную лучинку). Вот видите, как он усиливает горение дерева, как он заставляет лучинку гореть несравненно ярче, чем на воздухе. Итак, у нас здесь в чистом виде то второе вещество, которое содержится в воде и которое, когда вода образовалась при горении свечи, было, очевидно, взято из окружающего воздуха. Как же мы его назовем? А, В или С? Давайте назовем его О, назовем его кислородом. Имя очень хорошее, характерно звучащее. Итак, значит, это кислород присутствовал в воде и составлял такую значительную часть ее.
Теперь мы сможем яснее понимать наши опыты и исследования: ведь когда мы все это хорошенько продумаем, мы сразу сообразим, почему свеча горит в воздухе. Разделив воду на составные части при помощи электричества, мы получаем два объема водорода и один объем вещества, сжигающего водород. Это соотношение объемов представлено на следующей схеме, где указаны также и массы этих составных частей. Отсюда видно, что кислород второй составной элемент воды вещество очень тяжелое по сравнению с водородом.
Пожалуй, теперь, после того как мы выделили кислород из воды, мне пора вам рассказать, как он получается в больших количествах. Кислород, как вы сразу же сообразите, есть и в атмосфере, иначе как же могла бы свеча давать при сгорании воду? Без кислорода это было бы совершенно невозможно. А можем ли мы добывать кислород из воздуха? Что же, есть такие способы, очень сложные и трудные, посредством которых можно получить кислород из воздуха, но мы воспользуемся другим, более простым способом.
Вот это вещество называется перекисью марганца. Минерал этот очень невзрачный, но очень полезный; если его раскалить докрасна, он выделяет кислород.
Вот чугунная бутыль, в которую заложено некоторое количество этого вещества; в горлышко вставлена трубка. Мистер Андерсон поместит этот сосуд в огонь: ведь сосуд чугунный и может выдержать жар. А вот так называемый хлорат калия. Это вещество в больших количествах производится для отбеливания пряжи и тканей, для использования в химии и медицине, для фейерверков и других целей. Я смешиваю его с перекисью марганца (кстати, окислы меди и железа дали бы такие же результаты). Для получения кислорода из такой смеси достаточно будет нагреть сосуд до температуры гораздо более низкой, чем красное каление. Я не собираюсь добывать много кислорода, нам он нужен только для опытов. Однако вы сейчас убедитесь, что если я помещу в сосуд слишком мало смеси, то первая порция газа будет непригодна к употреблению, потому что она смешается с тем воздухом, который уже находится в сосуде. Как видите, нагревание на обычной спиртовке оказывается совершенно достаточным, чтобы получить кислород из смеси бертолетовой соли с перекисью марганца, так что у нас пойдут одновременно два процесса добывания кислорода. Смотрите, как обильно выделяется газ из этой маленькой порции смеси!
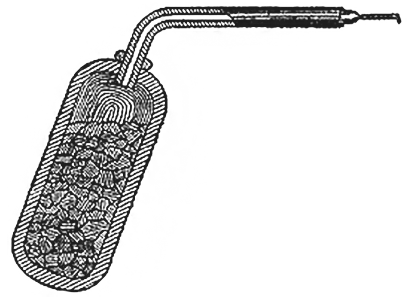
Чугунная бутыль с перекисью перекиси марганца
Исследуем этот газ и выясним, каковы его свойства. Вы видите, что здесь получается в точности такой же газ, как тот, который у нас получался в опыте с батареей: газ бесцветен, в воде не растворяется и по видимым свойствам похож на обычный атмосферный воздух. (Эту первую банку, содержащую смесь воздуха с первыми порциями выделяющегося кислорода, мы отставим подальше и приготовимся к проведению опытов надлежащим образом.)
У кислорода, который мы добывали из воды при помощи электрической батареи, была ярко выражена способность заставлять гореть дерево, воск и т. п.; очевидно, мы можем рассчитывать и здесь найти то же самое свойство. Испытаем газ. Посмотрите, вот как горит лучинка в воздухе, а вот как она горит в этом газе. (Лектор опускает лучинку в кислород.) Видите, как она ярко и хорошо горит!
Вы также можете наблюдать еще вот что: этот газ тяжелый; водород же поднялся бы вверх подобно воздушному шару или даже еще быстрее: ему не мешал бы вес оболочки. Нетрудно убедиться, что, хотя мы получили из воды вдвое больше по объему водорода, чем кислорода, отсюда еще не следует, чтобы у нас его было вдвое больше и по массе: ведь один газ тяжелый, а другой очень легкий. Мы располагаем методами определения массы газов или воздуха, но я не буду здесь заниматься этим, а просто сообщу вам, какова масса водорода и кислорода. Пинта водорода имеет массу всего три четверти грана, а тот же объем кислорода около двенадцати гран. Это очень большая разница. Масса кубического фута водорода 1/12 унции, а масса кубического фута кислорода 1 1/3 унции. Продолжая таким образом, мы могли бы дойти до таких масс вещества, которые можно определить с помощью весов, и таких, которые мы можем исчислять на центнеры и тонны, в чем вы очень скоро убедитесь.
Так вот, вернемся к этой способности кислорода поддерживать горение, по которой мы можем его сравнивать с воздухом. Я возьму огарок свечи и на нем покажу вам это свойство. Вот наша свечка горит в воздухе, а как же она будет гореть в кислороде? У меня тут есть банка с кислородом, и я накрою ею свечку, чтобы вы могли сравнить действие этого газа с действием воздуха. Ну, смотрите, Это похоже на тот яркий свет, который вы видели у полюсов электрической батареи. Подумайте, до чего здесь сильна реакция! И тем не менее, по ходу всей этой реакции не возникает ничего такого, что бы не получалось при сгорании свечи в воздухе. В кислороде наблюдается такое же выделение воды и точно такие же явления, какие происходят, когда свеча горит в воздухе.
Теперь, познакомившись с этим новым веществом, мы можем исследовать его несколько подробнее, чтобы иметь уверенность в том, что мы в общем хорошо поняли, что собой представляет эта составная часть продуктов сгорания свечи. Способность этого вещества поддерживать горение изумительно велика. Возьмем, например, эту простейшую лампочку, являющуюся своего рода прототипом всякого рода ламп, применяемых для самых различных целей, для маяков, для освещения предметов, рассматриваемых в микроскоп, и т. д. Если бы понадобилось заставить ее гореть очень ярко, вы бы сказали: «Раз свеча лучше горела в кислороде, то почему бы и лампе не гореть ярче!» Конечно, она будет лучше гореть.
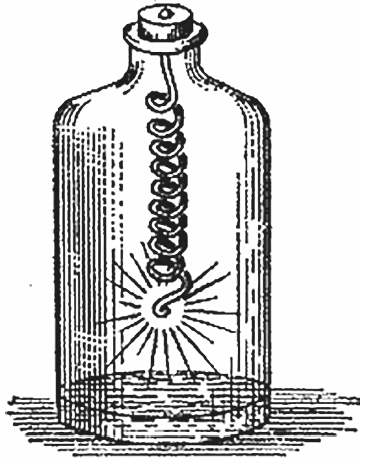
Лампочка, помещенная в банку: в зависимости от подачи кислорода пламя горит тускло или ярко
Сейчас я нарочно устрою так, чтобы эта лампочка у нас горело тускло, а затем мистер Андерсон передаст мне трубку, подводящую сюда кислород из банки, где он у нас накопился, и я поднесу ее к пламени лампочки… Вот пошел кислород! И какое получилось пламя! Ну а что будет с лампой, если я прекращу подачу кислорода? (Закрывается кран, и лампа опять становится тусклой.) Поразительно, до чего мы усиливаем горение при помощи кислорода! Он влияет на горение не только водорода, углерода или свечи он усиливает все виды горения вообще.
Банка с кислородом и с железной проволокой
Посмотрим, например, как будет гореть в кислороде железо. Ведь вы уже видели, как слабо горит железо в воздухе. Вот банка с кислородом, а вот железная проволока; но даже если бы это был брус толщиной в руку, и то он горел бы совершенно так же, как проволока. К концу проволоки я сперва прикрепляю кусочек дерева и зажигаю его, а затем опускаю все вместе в банку. Смотрите! Дерево горит так, как оно и должно гореть в кислороде. А сейчас горение передастся железу… Вот загорелось и железо. Как ярко оно горит. Так оно и будет гореть долгое время. Если мы обеспечим подачу кислорода, железо будет продолжать гореть, пока не сгорит дотла.
Оставим теперь железо и обратимся к какому-нибудь другому веществу. Однако нам придется ограничиться немногими опытами, так как у нас не хватит времени для всех тех иллюстраций, которые вы могли бы посмотреть, будь у нас больше времени. Возьмем кусочек серы, вы знаете, как сера горит на воздухе. Так вот, поместим ее в кислород, и вы убедитесь, что все, что может гореть в воздухе, может гореть и в кислороде, и притом гораздо интенсивнее. Это наведет вас на мысль, что, пожалуй, сам атмосферный воздух обязан именно этому газу своей способностью поддерживать горение. Сера очень спокойно горит в кислороде, но вы же видите, что реакция здесь несравненно сильнее и интенсивнее, чем при горении серы в обыкновенном воздухе.
Теперь я покажу вам горение еще одного вещества – фосфора. Здесь условия более подходящие для этого опыта, чем у вас дома. Фосфор вещество весьма горючее; а если так обстоит дело в воздухе, то что вы можете ожидать от горения фосфора в кислороде? Показывать вам его в полной силе я не собираюсь, так как есть риск, что при этом взорвется весь прибор. Даже и так банка может треснуть, несмотря на все мои предосторожности. Видите, как горит фосфор на воздухе. Но какой изумительный свет он испускает при горении в кислороде! (Лектор опускает зажженный фосфор в банку с кислородом.) Вот вы тут видите, как отскакивают твердые частицы, благодаря которым это горение и оказывается таким ослепительно ярким.
До сих пор это свойство кислорода и вызываемое им яркое горение мы испытывали при помощи таких веществ, которые не содержатся в воде и в свече. Теперь нам надо еще рассмотреть это свойство в отношении к водороду. Помните, у нас произошел небольшой взрыв, когда мы дали возможность кислороду и водороду смешаться и гореть вместе. Вы помните также, что когда я сжигал кислород и водород вместе в одной струе, у нас получалось очень мало света, но очень много тепла. Теперь я собираюсь поджечь смесь кислорода и водорода в той же пропорции, в какой они содержатся в воде. Вот сосуд, в котором смешан один объем кислорода с двумя объемами водорода. Таким образом, эта смесь по своей природе не отличается от того газа, который мы сегодня получали при помощи электрической батареи.
Здесь у нас чересчур много газа, чтобы сжечь его одновременно, поэтому я устроил приспособление, чтобы надувать этой смесью газов мыльные пузыри, а затем их поджигать и таким образом на опыте убедиться, как кислород поддерживает горение водорода. Прежде всего проверим, удастся ли нам надуть пузырь. Вот пошел газ. (Через курительную трубку, присоединенную к банке со смесью, лектор пропускает газ в мыльную воду.) Вот и пузырь. Я ловлю его на ладонь. Пожалуй, мои действия в этом опыте покажутся вам странными, но я просто хочу вам доказать, что не всегда можно доверяться шуму и звукам, а лучше держаться подлинных фактов. (Лектор поджигает на своей ладони мыльный пузырь; происходит взрыв.) Я боюсь поджечь пузырь прямо у трубки, потому что взрыв может проникнуть в банку тогда она разлетелась бы на куски. По всем этим видимым явлениям и по звуку вы можете судить, что кислород с чрезвычайной готовностью и стремительностью соединяется с водородом.
Я надеюсь, что из всего сказанного выше вы теперь можете составить себе понятие о том, что представляет собой вода по отношению к кислороду и к воздуху. Почему кусочек калия разлагает воду на составные части? Потому, что в воде он находит кислород. Я сейчас повторю этот опыт. Что выделяется в свободном состоянии, когда я кладу в воду калий? Выделяется водород, и он-то и горит, а кислород соединяется с калием. Так этот кусочек калия, разлагая всякую воду, в том числе хотя бы воду, полученную при горении свечи, забирает из нее кислород, в свое время забранный свечой из воздуха, и тем самым высвобождает водород. Даже если положить кусочек калия на лед, то, как это ни странно, лед подожжет калий. Я это вам покажу для того, чтобы расширить ваше представление обо всем этом и чтобы вы могли убедиться, до какой степени внешние обстоятельства влияют на результаты опыта. Ведь калий на льду, а получается какое-то подобие вулканического извержения!
Ну, теперь мы познакомились с этими необычайными и удивительными реакциями. На следующей лекции я покажу вам, что такие странные и опасные явления не угрожают нам не только при горении свечи, но и при горении светильного газа в уличных фонарях и топлива в наших каминах, если только мы будем соблюдать соответствующие правила, подсказанные нам природой.

