Почва – коварная среда
Рассмотрим кратко процессы, происходящие при коррозии металлических предметов. В результате атмосферной коррозии медные сплавы покрываются тонкой пленкой оксидов: красного оксида меди Cu2O и черного оксида CuO. Со временем пленка приобретает коричневый цвет, это так называемая естественная патина – темный прозрачный слой, придающий изделиям налет благородной старины, однако такое можно наблюдать при не очень длительном хранении предмета.
В отличие от атмосферной коррозии, при почвенной коррозии (именно с ней приходится иметь дело археологу) дело обстоит намного хуже. На предмете образуются коррозионные слои, наружный состоит из основных карбонатов меди (в зависимости от состава зеленого или синего цвета), покрытых остатками почвы и органических наслоений. Там же часто содержится основной хлорид меди СuCl(OH), а под ним – плотный красно-коричневый оксид меди Cu2O, содержащий включения черного оксида CuO. Еще глубже расположены чешуйки восстановленной меди, это результат электрохимической коррозии, протекающей в почве.
Между слоем восстановленной меди и оксидным слоем находится самая опасная коррозионная составляющая – хлорид меди CuCl2, чаще всего это соединение образуется при повышенной влажности от присутствия ионов хлора в засоленных почвах. Хлорид меди при взаимодействии с влагой гидролизуется, переходя в основной хлорид СuCl(OH). При этом образуется хлороводород HCl, который в присутствии кислорода и влаги начинает разрушать не затронутый коррозией слой металлической меди. На поверхности предмета появляются небольшие ярко-зеленые пятна рыхлого гигроскопичного вещества, постепенно очаги разрастаются, разрушение также идет вглубь металла, образуются каверны, поверхность становится изъязвленной. Этот процесс называют «бронзовой болезнью» – термин, используемый реставраторами.
Теперь перейдем к железным сплавам, они заметно менее коррозионностойки в сравнении с медными сплавами. При почвенной коррозии железных сплавов под действием кислорода и влаги образуются оксиды и гидроксиды железа Fe2O3·nH2O желтовато-коричневого цвета, синеватый фосфат железа Fe3(PO4)2·8H2O, желтовато-серый карбонат FeCO3.
Для предмета, находящегося в почве, сохраняется определенное равновесие между металлом и окружающей средой, но при извлечении его из археологического слоя это равновесие нарушается: меняется влажность и облегчается доступ кислорода, в результате увеличивается скорость коррозии. Ионы хлора, попавшие в объект из почвенной влаги, реагируя с металлом, образуют хлориды железа, которые, в свою очередь, при гидролизе выделяют хлороводород HCl, который взаимодействует с металлической поверхностью. Место коррозии все время перемещается, затрагивая новые участки сохранившегося металла, что приводит к активному разрушению предмета. Таким образом, реставрацию извлеченного предмета нельзя отложить на неопределенное время, необходимо как можно раньше приступить к обработке.
Не только восстановить, но и уберечь
Состав металла в археологических предметах в настоящее время подробно изучен с помощью микроскопического исследования участков протравленной поверхности, а также с использованием современных спектральных методов, которые позволяют провести анализ без взятия пробы. Эти сведения помогают провести более точную датировку таких предметов, кроме того, по содержанию примесных металлов можно определить состав использовавшихся в то время рудных месторождений. Широко известный радиоуглеродный метод, используемый для датировки остатков органического происхождения, в этом случае малоприменим, так как он «работает» только при наличии атомов углерода, и иногда он может быть полезен при определении возраста органических наслоений.
Если вопросы, касающиеся состава археологических предметов, в настоящее время успешно решают с помощью современных физических методов, то во всем, что относится к процедуре их восстановления после коррозии, протекавшей в течение столетий, еще существует много проблем.
Наука реставрации накопила громадное количество разнообразных приемов, позволяющих вернуть корродированным предметам вид, близкий к первоначальному. В большинстве случаев используют реагенты, широко применяемые для очистки и консервации металлов. Отдельные оригинальные методики удалось создать некоторым талантливым реставраторам, сочетавшим знание химии с искусством экспериментатора. Тем не менее многие из разработанных приемов хотя и позволяют на какое-то время достичь нужного результата, но сохраняют этот эффект ненадолго.
Первый этап работы с археологическим предметом – очистка от загрязнений, представляющих собой жировые наслоения, смешанные с частицами органических веществ и остатками почвы. Далее следует химическая очистка от продуктов коррозии.
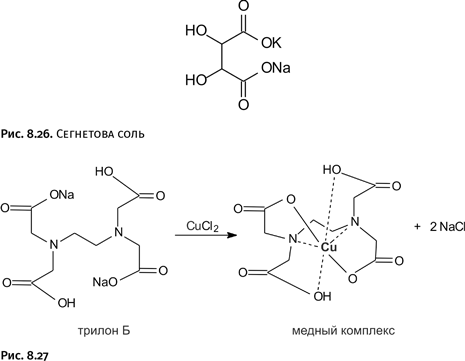
А теперь рассмотрим некоторые устоявшиеся методики. Для очистки медных изделий испробовали много различных реагентов: щелочной раствор сегнетовой соли NaKC4H4O6•4H2O (рис. 8.26), фосфат натрия (он входит в состав бытового средства калгон для смягчения воды), сульфамидную кислоту HOS(O)2NH2. Все эти средства не удаляют красно-коричневый куприт Cu2O. Широко используют препарат трилон Б – динатриевую соль этилендиаминтетрауксусной кислоты, при этом ион металла «укрывается» во внутренней полости молекулы, а металлическая поверхность не затрагивается (рис. 8.27).
Этот реагент растворяет практически все нерастворимые в воде продукты коррозии – оксиды, гидроксиды и карбонаты. Однако он заметно ослабляет сам металл, это так называемое «растравливание».
При электрохимических методах очистки существует опасность того, что поверхность покроется тонким слоем свежевосстановленной меди, имеющим яркую красноватую окраску. В результате старинный предмет приобретет вид недавно изготовленной поделки.
Пожалуй, самое важное, что все найденные методики не решали проблему стабилизации – сохранения на долгое время результатов реставрации.
При реставрации бронзовых предметов основная проблема та же: чтобы сохранить полученные результаты, необходимо удалить следы хлорида меди CuCl2, приводящие к появлению «бронзовой болезни». Часто используют длительную многократную промывку водой (иногда в течение нескольких месяцев) для извлечения ионов хлора Cl– из пор, трещин и полостей.
При обработке водным раствором сесквикарбоната натрия (смесь кислого и среднего карбоната натрия NaHCO3 + Na2CO3) галогениды переходят в труднорастворимые карбонаты, которые «запечатывают» хлориды меди в порах и трещинах, предохраняя их от контакта с влагой. Процесс длится несколько месяцев (при этом необходима ежедневная замена реагента), кроме того, диффузия (проникновение) новых порций реагента в мелкие полости заметно затруднена.
При коррозии предметов из железных сплавов наиболее агрессивные продуты коррозии – хлориды железа (так же, как и в случае с хлоридами меди). Эффективна обработка бензтриазолом. Этот препарат широко используют в замкнутых системах водонагрева для предотвращения коррозии аппаратуры. Бензтриазол блокирует металлическую поверхность, препятствуя доступу влаги к активным продуктам коррозии. Применяют также трилон Б.
Результативно использование танина (более известен как дубильное вещество): он не удаляет продукты коррозии, а образует с ними на какое-то время прочные нерастворимые комплексы, предохраняющие железо от дальнейшего разрушения. Идея такого применения танина возникла после археологических раскопок в Англии, где были найдены хорошо сохранившиеся железные предметы, несмотря на то что почвы в этом районе были весьма агрессивны. Оказалось, что на месте раскопок прежде находились мастерские по дублению кож и в землю выливали отработанные растворы, содержащие танин. Опыт работы с танином показал, что он не предотвращает рецидивную (повторно возникающую) коррозию, кроме того, поверхность предмета приобретает черный цвет.
Классический способ консервации железных сплавов, называемый в быту преобразованием ржавчины, состоит в обработке поверхности ортофосфорной кислотой, содержащей ингибитор (например, уротропин), который препятствует взаимодействию кислоты с металлическим слоем. Оксиды железа при такой обработке превращаются в фосфат железа, прочно соединяющийся с поверхностью металла.
Здесь уместно отметить, что проблемы реставрации тесно связаны с чисто эстетическими вопросами. Стараясь сохранить археологический вид предмета, реставратор должен выявить его форму, показать детали украшения или конструктивные особенности, раскрыть гравировку или надпись, при этом, естественно, следует уберечь налет старины. Весьма желательно, чтобы работа реставратора была минимально заметна. Точно так же музыкант-исполнитель не должен стараться «блеснуть» мастерством, его задача – показать красоту самого произведения. Все эти эстетические принципы, определяющие границы допустимого вмешательства реставратора, сформулированы в Международной хартии по консервации и реставрации памятников и достопримечательных мест (Венецианская хартия), которая была принята в Венеции в 1964 г. на II Международном конгрессе архитекторов и технических специалистов по историческим памятникам. Рекомендациями Венецианской хартии руководствуются многие реставраторы, сочетающие искусство химического эксперимента с уважительным отношением к археологическим объектам. Например, крайне нежелательно использовать различные защитные лаковые покрытия, поскольку они отличаются от металла блеском и фактурой, что нарушает эстетическое восприятие древнего предмета (экспонат начинает напоминать лакированную безделушку), кроме того, защитные свойства многих таких покрытий незначительны.
Внушительное обилие рассмотренных реагентов для реставрации не случайно – каждый из них обладает нежелательным побочным эффектом: методика очень длительна и трудоемка или технически трудноосуществима. Некоторые способы были найдены путем экспериментальных поисков, основанных не на детальном анализе химических процессов, а скорее на интуитивно полученном удачном результате. Опыт работы с такими препаратами показал, что при их использовании сохранялась высокая вероятность появления рецидивной (повторной) коррозии после реставрации (в случае медных сплавов – это «бронзовая болезнь»). Все это привело к поиску новых методов реставрации и стабилизации.

