Книга: Из чего это сделано? Удивительные материалы, из которых построена современная цивилизация
Назад: 7. Прозрачность
Дальше: 9. Утонченность
8. Постоянство

На первом уроке учитель рисования мистер Баррингтон рассказал нам, что все вокруг состоит из атомов. Абсолютно все. И если мы это поймем, то можем попробовать стать художниками. Класс затих. Мистер Баррингтон поинтересовался, есть ли у нас вопросы, но мы онемели от неожиданности, думая про себя, не ошиблись ли мы дверью. Учитель тем временем продолжил вводный урок. Взял карандаш и нарисовал идеальный круг на листе бумаги, приколотом к стене. Все оживились, по рядам пронесся вздох облегчения – значит, мы все-таки будем заниматься рисованием.
– Сейчас я перенес атомы карандашного грифеля на бумагу, – заметил учитель и произнес целую речь о замечательных свойствах графита как материала для художественного творчества. – Важно иметь в виду, – сказал он, – что, хотя алмаз считается высшей формой углерода, ему не дано выразить самую суть и, в отличие от графита, для настоящего искусства он не годится.
Остается лишь догадываться, что бы он подумал об инкрустированном бриллиантами черепе «За любовь Господа» стоимостью 50 миллионов фунтов стерлингов, произведении известного британского художника Дэмиена Херста.
Но, описывая отношения между двумя формами углерода, алмазом и графитом, как соперничество, он был совершенно прав. Борьба между темным, выразительным, практичным графитом и чистым, холодным, твердым, сверкающим алмазом идет с древнейших времен. Если говорить о культурной ценности, то алмаз давно победил, но все еще может измениться. Новое понимание структуры графита сделало из него сокровище.
Через тридцать лет после того, как я благодаря учителю рисования узнал, что такое графит, мы встретились с профессором Андреем Геймом, одним из крупнейших мировых специалистов по углероду, в его кабинете на третьем этаже на кафедре физики Манчестерского университета. Жаль, про него нельзя сказать, что он, подобно Баррингтону, выражал себя только с помощью графита. Когда он открыл ящик письменного стола, я увидел великое множество шариковых ручек и маркеров для белой лекторской доски. С сильным русским акцентом Андрей сказал:
– Идеального круга не существует, Марк.
Его слова привели меня в замешательство – понял ли он, о чем я только что рассказывал? Порывшись в ящике, он достал небольшой подарочный футляр из красной кожи и сказал:
– Взгляни на эту штуку, а я пока сварю кофе.
В футляре оказался диск из чистого золота размером с печенье, украшенный рельефным портретом какого-то мужчины. Взвесив тяжелый диск на ладони, я убедился, что он из металла. Металлический до безобразия. Ведь золото – это самый что ни на есть металл, всем металлам металл. Мужчиной, изображенным на медали, был Альфред Нобель; надпись гласила, что Андрей Гейм на пару с коллегой в 2010 году получил Нобелевскую премию в области физики за новаторскую работу о графене, двумерной версии графита, удивительном явлении в мире материалов. В ожидании Андрея и кофе я размышлял над его загадочным ответом. Возможно, он хотел сказать, что последние десять лет в своих исследованиях углерода ходил по кругу, но финиш все-таки не совпал со стартом.
Углерод – это легкий атом с шестью протонами и, как правило, шестью нейтронами в ядре. Иногда ядро содержит восемь нейтронов, но в такой форме, известной как углерод-14, атомное ядро нестабильно, и данный изотоп подвержен радиоактивному распаду. Поскольку скорость распада остается постоянной в течение долгого времени и эта форма углерода присутствует во многих материалах, измерение его относительного количества позволяет вычислить возраст материала. Метод, известный как радиоуглеродная датировка, осветил наше прошлое как никакой другой. С помощью этой формы углерода был определен настоящий возраст Стоунхенджа, Туринской плащаницы и свитков Мертвого моря.
Ядро в углероде играет второстепенную роль, если только речь не идет о радиоактивности. Что касается прочих свойств, то за них отвечают шесть электронов, защищающих ядро. Два из них спрятаны в глубине, рядом с ядром, и не участвуют в химической жизни атома – в его взаимодействиях с прочими элементами. Оставшиеся четыре образуют слой, максимально удаленный от центра, и являются активными. Именно эти четыре электрона отличают грифель в карандаше (графит) от бриллианта (алмаза) на обручальном кольце.
Самое простое, что делает атом углерода, – обменивается четырьмя активными электронами c другим атомом углерода. Образуются четыре химические связи, что решает проблему активных электронов: каждый из них находит пару в виде такого же электрона, но принадлежащего другому атому. Получившаяся кристаллическая структура обладает необычайной твердостью. Это и есть алмаз.
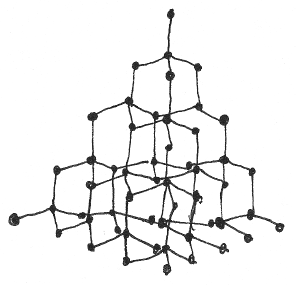
Кристаллическая структура алмаза
Самый крупный алмаз, известный на данный момент, находится в галактике Млечный Путь, в созвездии Змеи (в Хвосте Змеи), где он вращается вокруг пульсара PSR J1719–1438. Это целая планета в пять раз больше Земли. По сравнению с ней земные алмазы кажутся малюсенькими. Даже «Куллинан» – алмаз размером с футбольный мяч, самый крупный из когдалибо найденных. Он был добыт в Южной Африке и в 1907 году подарен королю Эдуарду VII ко дню его рождения. Ныне его части украшают королевские корону и скипетр. «Куллинан» созревал под землей на глубине примерно 300 км – миллиарды лет высокая температура и давление превращали большой кусок углеродной породы в огромный алмаз. Затем, вероятнее всего, извержением вулкана его вынесло к поверхности, там он спокойно лежал еще миллионы лет, пока его не нашли на глубине всего в милю под землей.
В детстве меня без конца водили по всяким национальным музеям, и во всех без исключения мне было скучно. Я старался делать то же, что и взрослые: ходить в задумчивом молчании или стоять в размышлении перед картиной или скульптурой, но все это никак на меня не действовало. Из этих посещений я ровным счетом ничего не вынес, как мне тогда казалось. Все изменилось, когда я попал в королевскую сокровищницу в лондонском Тауэре. Я был сражен, едва переступив порог этой пещеры Аладдина. Золото и драгоценности, казалось, говорили со мной на языке гораздо более глубинном и первобытном, нежели искусство. Меня охватило чувство, схожее с религиозным экстазом. Сейчас я не думаю, что упивался тогда видом богатства, – на самом деле так подействовала на меня встреча с чистой материальностью. Перед «Большой Звездой Африки» (так назвали самый крупный из бриллиантов, полученных после того, как «Куллинан» раскололи на несколько частей и огранили их) теснилась толпа. Мне хватило одного взгляда на этот бриллиант, чтобы не забыть его уже никогда, хоть я и видел его из-под руки великана в потной клетчатой рубашке, стоя за спиной у индианки, которая цокала от удивления языком. Присутствие дамы из Индии было очень кстати, потому что, как я узнал потом из отцовской энциклопедии, эта страна была единственным поставщиком алмазов вплоть до середины XVIII века, когда открыли месторождения в других частях света, самые крупные – в Южной Африке.
Практически любой алмаз – это монокристалл. В одном алмазе в среднем содержится миллион миллиардов миллиардов атомов (1 000 000 000 000 000 000 000 000), собранных в идеальную пирамиду. Благодаря такой структуре алмаз обладает замечательными свойствами. Электроны сидят в ней как влитые, что придает алмазу его легендарную твердость. Алмаз, кроме того, прозрачен, однако у него чрезвычайно высокая оптическая дисперсия, то есть он расщепляет световой пучок на отдельные цвета, вспыхивая радугой.
Сочетание необычайной твердости и блеска делает алмаз почти безупречным драгоценным камнем. Практически невозможно поцарапать его поверхность, поэтому он сохраняет совершенство огранки и искрящийся блеск в течение всей жизни своего владельца, да и жизни целой цивилизации: под дождем и под солнцем, продираясь вместе с хозяином сквозь джунгли или стирая белье вместе с хозяйкой. Уже в древности алмаз был известен как самый твердый материал на земле. Само слово «алмаз» происходит от греческого adamas, что значит «неизменный» или «несокрушимый».
Транспортировка «Куллинана» в Англию представляла немало трудностей, связанных с его охраной, поскольку газеты уже раструбили об открытии самого крупного необработанного алмаза. Владельцы не на шутку опасались знаменитых преступников вроде Адама Ворта, успевшего уже похитить целую партию алмазов, – прототипа заклятого врага Шерлока Холмса профессора Мориарти. Втайне был составлен и приведен в исполнение план, достойный самого Шерлока Холмса. Фальшивый алмаз отбыл в Британию пароходом под строжайшей охраной, между тем настоящий камень был отправлен почтой в ничем не примечательной коричневой картонной коробке. Уловка удалась еще по одной причине, точнее, из-за еще одного замечательного свойства алмаза: он очень легок, поскольку состоит из углерода. Едва ли «Куллинан» весил более полукилограмма.
Адам Ворт был такой не один. Пока богатые наперебой скупали крупные бриллианты, родилась новая преступная специализация – алмазный вор. Кража даже небольшого бриллианта, почти невесомого, но дорогого, обеспечивала безбедную жизнь, к тому же украденные бриллианты было практически невозможно отследить. (Чего никак нельзя сказать о золотой медали Андрея Гейма, будь она мной украдена. Переплавив ее в слиток, я бы заработал самое большее несколько тысяч фунтов.) Этот новый вид кражи драгоценностей перенял достоинства самого бриллианта – элегантность, изысканность и чистоту. В фильмах «Поймать вора» и «Розовая пантера» бриллианты играют роль принцессы, томящейся в жестоком плену. Честные граждане днем, ночью их спасители в исполнении таких кинозвезд, как Кэри Грант и Дэвид Нивен, превращаются в алмазных воров. В этих фильмах кража бриллиантов изображается благородным поступком. У похитителя бриллиантов легкая пружинистая походка; все, что ему нужно, – это облегающий черный костюм и хорошее знание старинных особняков с их запутанными коридорами, а также кодовых замков к сейфам, спрятанным за картинами. Ограбление банка или почтового поезда ради получения золота или наличных денег, напротив, предстает грязным преступлением, зачастую совершаемым жадными и жестокими людьми.
В отличие от золота, бриллианты, несмотря на их коммерческую ценность, никогда не были частью всемирной денежной системы. Они не представляют собой ликвидный финансовый инструмент, то есть их не так-то легко превратить в деньги. Крупные бриллианты не имеют иного применения, кроме как вызывать интерес, восхищение и, самое главное, демонстрировать статус хозяина. Вплоть до XX века бриллианты могли позволить себе только по-настоящему богатые люди. Однако растущее благосостояние европейского среднего класса привело к появлению нового привлекательного рынка для алмазодобытчиков. Компания «Де Бирс», которой в 1902 году принадлежало 90 % мирового производства бриллиантов, очутилась перед дилеммой: как удовлетворить большой спрос и при этом не обесценить драгоценный товар. Решить ее помогла продуманная рекламная кампания. Слоган «Бриллианты навсегда» внушал обществу идею того, что истинным выражением вечной любви может служить лишь обручальное кольцо с бриллиантом. Каждый, кто хотел убедить возлюбленную в подлинности своих чувств, должен был купить кольцо с бриллиантом – тем дороже, чем подлиннее чувства. Кампания эффектно стартовала, и в миллионах домов появились бриллианты. Ее кульминацией стал одноименный фильм о Джеймсе Бонде, в котором композитор Джон Барри и певица Ширли Бэсси воспели новую социальную роль бриллиантов – символа романтической любви.
Впрочем, бриллианты все же не вечны, во всяком случае на нашей планете. Есть более стабильная форма углерода – это родной брат алмаза графит. Поэтому все алмазы, включая «Большую Звезду Африки» в лондонском Тауэре, на самом деле медленно превращаются в графит. Удручающая новость для владельцев бриллиантов. Впрочем, их можно утешить: до появления первых признаков вырождения камня пройдут миллиарды лет.
Структура графита радикально отличается от алмазной. Слои атомов углерода в ней расположены шестиугольником. Каждый слой представляет собой чрезвычайно прочное и устойчивое образование с более крепкими, чем в алмазе, межатомными связями. Факт весьма удивительный, если вспомнить, что из рыхлого графита делают смазку и карандашные грифели.
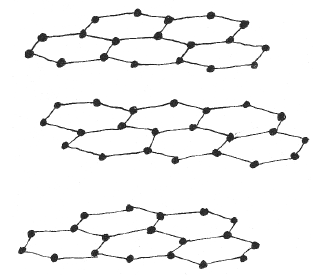
Кристаллическая структура графита
Парадокс, возможно, объясняется тем, что у каждого атома углерода внутри графитового слоя имеется три соседа, с которыми он делит четыре своих электрона. В алмазной же структуре каждый атом углерода делит свои четыре электрона с четырьмя атомами. Отсюда иная электронная структура и более сильные химические связи внутри слоев графита по сравнению с алмазными. В то же время у атомов графита не остается электронов, чтобы образовать прочные связи между слоями. Слои скрепляет универсальный клей, совокупность слабых взаимодействий, вызванных флуктуациями в электрическом поле молекул, – силы Ван-дер-Ваальса. Это те самые силы, которые делают липким офисный пластилин (Blu-Tack). Поэтому, когда графит подвергается механическому давлению, первыми рвутся слабые связи Ван-дер-Ваальса, и графит становится очень мягким. Именно так «работает» карандаш: прижимая его к бумаге, вы разрываете эти связи, и слои графита соскальзывают на бумагу. Если бы не слабые связи между слоями, графит был бы прочнее алмаза. Этот факт послужил одной из отправных точек для Андрея Гейма и его команды.
Взгляните на темно-серый, с металлическим отливом, карандашный грифель. Тысячелетиями этот материал ошибочно принимали за разновидность свинца и называли плюмбаго, или черным свинцом. Путаница была вполне понятной, поскольку и графит, и свинец – это мягкие металлы (впрочем, графит сегодня считается полуметаллом). Рудники плюмбаго приобретали все большую ценность по мере того, как графиту находили новые сферы применения. Оказалось, например, что из него выходят отличные пушечные ядра и мушкетные пули. В XVII–XVIII веках в Англии материал так сильно вырос в цене, что воры приноровились рыть тайные ходы в рудники или же нанимались рабочими и скрытно выносили плюмбаго под одеждой. Дороговизна подстегивала этот промысел, пока в 1752 году парламент не принял закон, объявлявший кражу графита из рудников тяжким уголовным преступлением, наказуемым годом каторжных работ или семилетней ссылкой в Австралию. К 1800 году добыча графита стала настолько прибыльным предприятием, что повсюду у ворот рудников стояла вооруженная охрана.
Причина того, что у графита, в отличие от алмаза, металлическая природа, кроется все в той же шестиугольной атомной структуре. Как мы уже знаем, в структуре алмаза все четыре электрона каждого атома углерода связаны с такими же электронами других атомов. Таким образом, все атомы пространственной решетки крепко взаимосвязаны, и «свободных» электронов нет. Вот почему алмазы не проводят электричество, ведь в их структуре отсутствуют электроны, которые могли бы свободно перемещаться, производя электрический ток. В то же время в структуре графита внешние электроны не просто связаны с парными электронами соседнего атома, скорее они образуют море электронов внутри материала. Одним из последствий этого является электропроводность графита – ведь электроны в нем могут перемещаться подобно жидкости. Нить накаливания в электрических лампочках Эдисона была из графита: за счет высокой температуры плавления он под действием тока раскаляется добела, но не плавится, излучая сильный свет. И кроме того, бесчисленные электроны служат чем-то вроде электромагнитного батута для света – именно отраженный свет придает графиту свойственный металлам блеск. Впрочем, команда Андрея Гейма получила Нобелевскую премию не за это лаконичное объяснение металлических свойств графита, это было для нее лишь отправной точкой.
Углерод – основа жизни на Земле, любой ее формы, и хотя различные углеродные соединения на первый взгляд совсем не похожи на графит, им легко придать шестиугольную структуру путем сжигания. При сильном нагреве дерево превращается в уголь, кусок хлеба – в сгоревший тост; да и мы сами почернеем и обуглимся, если подвергнуть нас воздействию пламени. Ни один из этих процессов не приводит к образованию чистого блестящего графита, поскольку шестиугольные слои углерода перемешаны, а не плотно уложены в аккуратном порядке. Тем не менее существует огромное разнообразие черных сажистых материалов с общим свойством: все они содержат углерод в его наиболее стабильной форме – в форме шестиугольных слоев. Каменный уголь, очередная разновидность черного сажистого углерода, стал широко применяться в XIX веке. Шестиугольные пласты атомов в угле образуются не за счет нагрева, как в случае с подгоревшим тостом, но вследствие геологических процессов, миллионы лет воздействовавших на останки растительных организмов. Первоначально уголь – это форма торфа, которая под воздействием высокой температуры и давления трансформируется в лигнит (бурый уголь), потом в битуминозный уголь, в антрацит и, наконец, в графит. В процессе этих трансформаций уголь теряет летучие соединения азота, серы и кислорода, присутствующие в первоначальном растительном материале, постепенно превращаясь в почти чистый углерод. По мере формирования гексагональных слоев материал приобретает все более выраженный металлический блеск, особенно заметный на зеркальных черных гранях некоторых углей, например антрацита. Однако уголь редко является чистой формой углерода. Вот почему при горении он довольно неприятно пахнет.
Среди всех сортов наиболее ценится за внешний вид уголь из ископаемых остатков чилийской араукарии. Это твердая порода (ее можно резать и полировать до зеркального блеска) насыщенного черного цвета с чудесным глянцем. Иногда этот уголь называют черным янтарем, поскольку он обладает похожими трибоэлектрическими свойствами: рождает при трении статический заряд и топорщит волоски на теле. Чаще он встречается под именем «гагат». В Англии он вошел в моду в XIX веке благодаря королеве Виктории, которая в знак траура по супругу принцу Альберту всю жизнь носила черную одежду и гагатовые украшения. По всей империи спрос на гагаты был так велик, что население йоркширского городка Уитби, в котором Брэм Стоукер позднее написал свой готический шедевр, роман «Дракула», внезапно бросило топить печи местным гагатом и перешло на производство знаменитых траурных украшений. Мысль о том, что у алмаза есть нечто общее с углем или графитом, была чистой фантазией, пока химики его не нагрели. В 1772 году это сделал Антуан Лавуазье и обнаружил, что раскаленный докрасна алмаз горит и сгорает дотла. После него совсем ничего не остается, как если бы он растворился в воздухе. Удивительный эксперимент. Прочие драгоценные камни, такие как рубин и сапфир, оказались невосприимчивы к нагреву. Их нельзя было довести не то что до красного, но даже до белого каления. Они не горели. У алмаза же, короля драгоценных камней, обнаружилась ахиллесова пята. Душа поет, когда я думаю про следующий опыт Лавуазье, настолько это было красиво. Химик нагрел алмаз в вакууме, чтобы там, в отсутствие необходимого для реакции горения воздуха, достичь более высокой температуры. Это один из тех экспериментов, которые легче предложить, чем выполнить, что особенно верно для XVIII столетия, когда создать вакуум само по себе было нелегкой задачей. Результат поразил Антуана Лавуазье. Как и в прошлый раз, камень раскалился докрасна, однако в ходе начавшейся реакции превратился в чистейший графит. Так было доказано, что оба материала состоят из одного и того же вещества – углерода.
Вооруженный этим знанием Лавуазье и многие его коллеги в Европе задумались о том, как осуществить обратную реакцию – превращение графита в алмаз. Того, кто сделал бы это, ждало сказочное богатство. Гонка началась. Но цель оказалась труднодостижимой. Все материалы склонны меняться от менее устойчивых структур к более устойчивым, и, поскольку структура алмаза менее устойчива, чем у графита, необходимы запредельно высокие температура и давление, чтобы «уговорить» графит пойти в обратную сторону, то есть превратиться в алмаз. Такие условия существуют в глубинах земной коры, но даже в этом случае потребуются миллиарды лет, чтобы вырастить большой алмазный кристалл. Воспроизвести подобные условия в лаборатории чрезвычайно сложно. Попытки химиков одна за другой кончались провалом. Никто из этих ученых не разбогател в одночасье, что лишний раз подтверждало их неудачливость в лаборатории. Впрочем, подозревали, что кое-кто все же совершил подвиг и преобразовал графит в алмаз, а теперь втихомолку наживает состояние.
Как бы там ни было, но в 1953 году появилось достоверное документальное свидетельство подобной трансформации. Ныне производство искусственных алмазов стало по-настоящему крупным бизнесом, и все же настоящие, природные алмазы вне конкуренции. Причин тому несколько. Во-первых, несмотря на то, что изготовление небольших искусственных алмазов обходится дешевле, чем добыча соразмерных им природных камней, все же первые, как правило, имеют изъяны, в частности непрозрачные включения: ускоренный промышленный цикл приводит к дефектам, которые в свою очередь вызывают пигментацию. На деле искусственно выращивают по большей части не ювелирные, а технические алмазы: алмазной пылью покрывают буры и другие режущие инструменты – не ради красоты, но чтобы резать и обрабатывать гранит и прочие твердые материалы. Во-вторых, подлинность составляет большую долю в общей ценности алмаза. Когда вы предлагаете руку и сердце, важно, чтобы в обручальном кольце сиял бриллиант, рожденный в глубинах Земли миллиарды лет назад, пусть даже по физическим свойствам искусственный камень ни в чем ему не уступает. Наконец, в-третьих, если вы сверхрациональный субъект, которого не трогает природная история камня, то для вас искусственный бриллиант слишком дорогой способ украсить возлюбленную. Есть немало гораздо более дешевых суррогатов, которые своим ослепительным блеском обманут кого угодно, кроме разве настоящих знатоков бриллиантов. К таким суррогатам относятся кубические кристаллы циркония и даже стекло. Впрочем, природные алмазы потерпели новое поражение: выяснилось, что алмаз больше не является самым твердым из известных материалов. В 1967 году открыли третий способ организации атомов углерода, который позволял получить еще более твердое вещество. Основу его строения также составляют гексагональные слои графита, но в трехмерной модификации. Считается, что эта структура, под названием лонсдейлит, на 58 % тверже алмаза, хотя в природе она существует в столь малых количествах, что это трудно проверить. Первый образец нашли в метеорите Каньон-Дьябло – сильный жар и повышенное давление, возникшие при ударе о Землю, вызвали превращения графита. В мире не существует ни одного обручального кольца из лонсдейлита, поскольку падения метеоритов этого типа происходят чрезвычайно редко и производят на свет лишь крошечные кристаллы, но открытие третьей структуры углерода неизбежно подводило к вопросу о возможной четвертой структуре – в дополнение к уже известным кубической (алмаз), шестиугольной (каменный и древесный уголь, гагат, графит) и трехмерной шестиугольной (лонсдейлит). Вскоре, благодаря авиационной промышленности, список пополнился еще одной синтетической структурой.
Первые летательные аппараты делали из дерева, легкого и крепкого. Одним из самых быстрых самолетов Второй мировой войны был почти полностью деревянный истребитель-бомбардировщик «Москито». Однако деревянная конструкция, как правило, страдает недостатками, так что построить из дерева корпус летательного аппарата весьма сложно. А поскольку авиастроители не думали отказываться от своих честолюбивых планов, конструкторы переключились на легкий металл алюминий. Последний, однако, нельзя назвать сверхлегким, и в глубине души инженеры надеялись обрести еще более прочный и легкий материал. Казалось, в природе ничего подобного не существует, поэтому в 1963 году инженеры из британского Королевского авиационного управления в Фарнборо решили его изобрести.
Углеродное волокно, как назвали они свое детище, было получено из графита, сплетенного в тонкие нити, при этом ученые максимально использовали огромную прочность и жесткость шестиугольных слоев. Как всегда в случае с чистым графитом, структурная зависимость от сил Ван-дер-Ваальса делала его уязвимым. Впрочем, покрытие волокон эпоксидным клеем решило проблему. Так родился углепластик, новый композиционный материал на основе углеродного волокна.
Хотя в авиастроении он в конце концов вытеснил алюминий (новейший «Боинг-Дримлайнер» на 70 % состоит из углепластика), понадобилось немало времени, чтобы доказать полную пригодность этого материала для авиационной промышленности. Впрочем, производителям спортивного оборудования углепластик сразу понравился. Он настолько изменил эксплуатационные качества спортивных ракеток, что поклонники традиционных материалов вроде дерева и алюминия быстро оказались в проигрыше. Живо помню тот день, когда мой друг Джеймс появился на теннисном корте, размахивая углепластиковой ракеткой с характерным черным плетением из углеродного волокна. Перед игрой он дал мне пару раз испробовать ее невероятную легкость и в то же время силу, а потом забрал ее и одержал надо мной сокрушительную победу. Есть что-то обескураживающее в том, что противник играет ракеткой вдвое легче и вдвое мощнее твоей. «Ну, углепластик, держись!» – воскликнул я перед началом игры, но это не помогло. С новым материалом серьезные перемены пришли в те виды спорта, где требуются легкость и высокая мощность, – то есть практически во все. Круто изменился в 1990-е годы велосипедный спорт: появились велосипеды с более обтекаемыми контурами, в которых применялись конструкции из углеродного волокна. Пределом совершенства таких велосипедов стали, вероятно, те, на которых Крис Бордман и Грэм Обри пытались побить часовой рекорд в своем классическом поединке. В 1990 годы оба британских велосипедиста установили мировые рекорды, а потом обгоняли друг друга на все более навороченных велосипедах из углеволокна. В 1996 году Крис Бордман проехал за час 56,375 км – и навлек на себя гнев Международного союза велосипедистов, который немедленно запретил к использованию новые конструкции из углеволокна, опасаясь, что они изменят традиционный спорт раз и навсегда.
«Формула-1», напротив, совсем иначе отнеслась к новинке и постоянно вносила изменения в правила, способствуя дальнейшему усовершенствованию материала. Действительно, передовые технологии – неотъемлемая составляющая этого спорта, и успех достигается как мастерством гонщика, так и новаторскими решениями конструкторов. Даже в беге не обошлось без углеволокна. Все больше спортсменов-инвалидов пользуются транстибиальными протезами. В 2008 году Международная ассоциация легкоатлетических федераций пыталась помешать этим спортсменам выступать против здоровых на том основании, что углепластиковые протезы нижних конечностей дают им преимущество и это якобы несправедливо. Однако Спортивный арбитражный суд отменил запрет, и в 2011 году безногий южноафриканец Оскар Писториус участвовал вместе с обычными спортсменами в эстафете 4 400 м мирового чемпионата в ЮАР, и его команда завоевала серебро. Углеродное волокно может сыграть весомую роль в легкой атлетике, если только легкоатлетические федерации не выступят против, по примеру велосипедных.
Успех композитов на основе углеволокна окрылил инженеров, которые вынашивают теперь идею грандиознейшего из проектов. Достаточно ли новый материал прочен, чтобы осуществить давнюю мечту человечества – построить лифт в космос? Космический лифт, или, как его еще называют, небесная праща, лестница в небо, космический фуникулер, – это сооружение, которое должно связать точку на земном экваторе с расположенным прямо над ней спутником на геостационарной орбите. С таким лифтом космические путешествия в кратчайший срок стали бы доступны самым широким массам. Людей и грузы можно было бы с легкостью отправлять в космос при минимальных энергетических затратах. Идею лифта разработал в 1960 году советский инженер Юрий Арцутанов. Чтобы ее осуществить, понадобится трос длиной 36 000 км, который соединит спутник с кораблем, находящимся в океане в зоне экватора. Все исследования показывают, что идея технически осуществима, при условии, что трос выполнен из материала с чрезвычайно высоким отношением прочности к весу. Почему речь идет именно о весе? Дело в том, что трос должен в первую очередь выдерживать собственный вес, чтобы не лопнуть. При длине в 36 000 км понадобится материал настолько прочный, что сделанная из него нить сможет удержать слона. На практике, однако, даже самая прочная нить из углеволокна способна удержать лишь кота. Впрочем, это из-за того, что в ней полно дефектов. Теоретические расчеты убедительно доказывают, что прочность углеволокна, совершенно свободного от дефектов, была бы гораздо выше и даже превосходила бы прочность алмаза. Ученые начали изучать возможность создания такого материала.
Ключ к решению был найден с открытием четвертой углеродной структуры, которая, в свою очередь, обнаружилась в самом, казалось бы, неподходящем месте – в пламени свечи. В 1985 году профессор Харольд Крото и его научный коллектив пришли к выводу, что внутри пламени свечи атомы углерода волшебным образом самоорганизуются в группы ровно по шестьдесят штук, образуя макромолекулы углерода. Эти молекулы выглядели словно гигантские футбольные мячи и были названы бакиболами (или фуллеренами) в честь архитектора Бакминстера Фуллера, изобретателя геодезического купола тоже гексагональной структуры. За это открытие научный коллектив профессора Крото получил в 1996 году Нобелевскую премию в области химии, а также привлек всеобщее внимание к тому факту, что микроскопический мир может содержать большое разнообразие неизвестных нам до поры до времени углеродных структур.
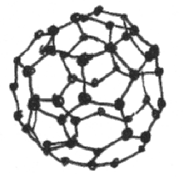
Молекулярная структура фуллеренов
В считаные дни углерод стал одной из самых горячих тем в материаловедении, и вскоре появился новый вид углерода, из которого можно было сделать трубочки диаметром всего в несколько нанометров. При всей сложности молекулярной архитектуры эти углеродные нанотрубки обладали редкой способностью к самоорганизации. Без всякой посторонней помощи и высокотехнологичного оборудования они принимали самые замысловатые формы в свечном дыму. Это новое знание было сродни открытию бактерий: мир неожиданно оказался куда более непростым и причудливым местом, чем мы думали раньше. Не только живые организмы, как выяснилось, умеют самоорганизовываться в сложные структуры, но и неживые тоже! Всех охватило страстное желание творить и исследовать наномолекулы. Нанотехнология вошла в моду.
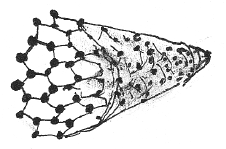
Молекулярная структура углеродных трубок
Углеродные нанотрубки похожи на миниатюрные углеродные волокна, только без слабых связей Ван-дер-Ваальса. Выяснилось, что у них самое высокое отношение прочности к весу среди материалов планеты. Значит, потенциально они достаточно прочны, чтобы построить из них космический лифт. Проблема решена? Не совсем. В длину углеродные нанотрубки имеют самое большее несколько сотен нанометров, в то время как их практическое применение требует длины в несколько метров. В настоящее время сотни исследовательских коллективов по всему миру работают над решением этой задачи. Но команда Андрея Гейма не принадлежит к их числу.
Андрей и его коллеги задались вопросом попроще: если все эти новые формы углерода основаны на гексагональной структуре графита, а графит заполняет слои гексагонального углерода, почему не считать сам графит чудесным материалом? Ответ: потому что эти слои слишком неплотно прилегают друг к другу, и это ослабляет материал. Тогда что будет, если взять лишь один слой гексагонального углерода? Какой выйдет материал?
…Когда Андрей Гейм вернулся с кофе на подносе, я все еще держал на ладони его золотую нобелевскую медаль, чувствуя себя слегка виноватым, хотя он сам дал мне ее посмотреть. Поставив поднос на стол, он забрал у меня медаль и протянул вместо нее кусок чистого графита из рудников графства Камбрия. Гейм сказал, что взял его прямо из шахты, расположенной, выражаясь географически, к северу от его кабинета в Манчестерском университете. Потом он показал, как его научно-исследовательская группа изготовила одинарный слой гексагонального углерода.
Андрей отрезал кусок липкой ленты, прижал к графиту, отдернул – на пленке остался тончайший блестящий металлический отпечаток. Он взял еще один отрезок ленты, прижал его к блестящему отпечатку на первом отрезке и отдернул. Теперь отпечаток разделился надвое. Повторив процедуру пять-шесть раз, Гейм получал все более тонкие слои графита. Наконец он объявил, что получил слой графита толщиной всего в один атом. Я посмотрел на отрезок скотча у него в руках. На нем было несколько темных смазанных пятнышек. Боясь упустить что-то важное, я присмотрелся внимательнее. «Разумеется, – улыбнулся Андрей, – его нельзя увидеть. Он слишком мал и поэтому невидим».
Я усиленно закивал, когда Гейм предложил пройти к микроскопу в соседнюю комнату, где можно было бы увидеть эти одноатомные слои графита.
Андрей и его коллега получили Нобелевскую премию не за то, что создали одинарный слой графита, а за то, что продемонстрировали исключительные, даже по меркам нанотехнологий, свойства этих слоев, которые заслужили собственное наименование – графен.
Начнем с того, что графен – это самый тонкий, прочный и жесткий материал в мире. Он проводит тепло быстрее, чем любой другой известный материал, и он проводит больше электроэнергии, быстрее и с меньшим сопротивлением, чем любой другой материал.
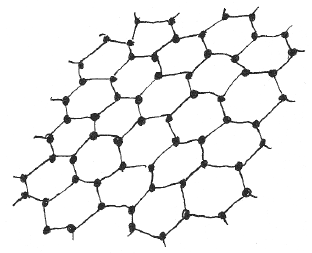
Молекулярная структура графена
Графен допускает туннельный эффект Клейна – необычное явление квантовой природы, при котором электроны внутри материала проходят сквозь барьеры, словно их вовсе нет. В общем, графен потенциально может стать электронной электростанцией и даже заменить кремниевые микросхемы – «сердце» компьютеров и устройств связи. Его необычайная тонкость, прозрачность, прочность и электронные характеристики могут пригодиться в сенсорных интерфейсах будущего, и не только экранах, к которым мы уже привыкли. Возможно, предметы целиком и даже здания будут чувствительны к прикосновениям. Но, вероятно, самый интригующий повод для похвалы графену – его двумерность. Это вовсе не означает, что у него нет толщины. Просто его нельзя сделать ни тоньше, ни толще, не изменив при этом его свойств, – это будет уже другой материал. Что и продемонстрировала команда Андрея: добавьте к графену еще один слой углерода, и он снова станет графитом; снимите один слой, и графен вовсе перестанет существовать.
Учитель рисования Баррингтон не знал этого, когда называл графит более высокой формой углерода, чем алмаз. В техническом смысле, однако, он был кругом прав. Также он был прав, говоря о важности атомной природы графита. Графен – это кирпичик толщиной в один атом, из которого построен графит. Это то, что вы оставляете на бумаге, когда рисуете карандашом. Графит можно использовать лишь как средство художественной выразительности, но его значение гораздо шире – этот материал и его скрученный вариант в виде нанотрубок станут важной частью нашего будущего мира на всех масштабных уровнях: от самого мелкого до самого крупного, от электроники до автомобилей, самолетов, ракет и даже (кто знает?) космических лифтов.
Померк ли алмаз перед графитом, породившим из себя графен? Победил ли графит, неожиданно для всех, в вековом поединке? Говорить окончательно еще рано, но для меня это факт сомнительный. Похоже, и вправду графен даст начало целой эпохе в строительстве. Ученые с инженерами уже сейчас влюблены в новый материал. Но это еще не гарантирует всеобщего признания. Возможно, алмазы уже не самые твердые и нерушимые в мире, и, как нам хорошо известно, они не вечны, однако для большинства людей они символизируют именно эти качества. Алмаз по-прежнему соединяет любящие сердца. Связь между бриллиантом и настоящей любовью, вероятно, возникла из-за рекламной кампании, но теперь она для нас совершенно реальна.
От графена, возможно, больше пользы, чем от алмаза, но он не сверкает, по сути он вообще невидим, неимоверно тонок и лишен объема. Кому захочется сравнивать свою любовь с таким материалом? Я думаю, пока рекламщики не освоят графен, кубические кристаллы углерода останутся лучшими друзьями девушек.
Назад: 7. Прозрачность
Дальше: 9. Утонченность

