Книга: Власть Рода. Родовые программы и жизненные сценарии
Назад: Введение
Дальше: Глава 2 Генетическая форма памяти
Глава 1
Энергия в биологических системах
1.1. Примеры бифуркации в системах
Огромное количество молекул, атомов в природе обычно находится в объединениях-коллективах, которые принято называть системами. Так, атмосфера Земли объединена в систему благодаря наличию в ней взаимодействующих гравитационных, температурных, электромагнитных полей.
Человек являет собой систему атомов и молекул, в которой взаимодействуют все виды энергетических полей, известных сегодня науке: гравитационное, температурное, химическое, ядерное, электромагнитное И т. д.
Представляют интерес две модели систем: закрытые (замкнутые, консервативные) и открытые. Закрытая система взаимодействует только сама с собой внутри себя, допуская интегративно-нулевое взаимодействие с другими системами. Открытая система взаимодействует с другими системами.
Деление достаточно условно. Так, например, атмосферу Земли можно рассматривать в первом приближении как закрытую систему, так как силы её взаимодействия с энергетическими полями Земли значительно больше, чем силы взаимодействия с другими планетами, с отдельным человеком и т. д.
Согласно второму закону термодинамики, равновесное состояние закрытой системы – хаос. Иными словами, это такое динамическое состояние, в котором энергия распределена в среднем поровну между частицами системы.
Если рассмотреть как образец закрытой системы атмосферу Земли, мы увидим, что химический состав её в естественном состоянии равномерен. В случае повышения концентрации какого-то химического элемента или температуры в данном локальном месте сразу же начинаются процессы, которые ведут к выравниванию.
Чистых закрытых систем в природе нет, ибо любая система в какой-то мере всегда взаимосвязана с другими системами. Так, атмосферу Земли, например, пронзают различные виды космических излучений. Они взаимодействуют с химическими элементами атмосферы, оставляя при этом часть своей энергии в атмосфере. Кроме того, атмосфера не может выровнять концентрацию химических элементов, температуру по радиусу (по высоте) от Земли и т. д.
Итак, любая закрытая система находится в равновесном состоянии. Давайте посмотрим, что произойдёт, если на закрытую систему воздействовать извне, тем самым превратив её в открытую систему.
Несколько примеров.
1. Привычный для нас воздух в комнате. Воздух, газ, представляет собой закрытую систему. При температуре +20 °C атомы, молекулы, составляющие воздух, мечутся – хаос торжествует. Вмешаемся в закрытую систему извне – начнём понижать температуру. С воздухом что-то стало происходить. Он перестал быть прозрачным, и вдруг прямо из воздуха начали появляться объекты, которые мы видим своими глазами. Приглядитесь – они же симметричные. Это не хаос, это же элегантные снежинки с великолепной симметрией.
Что произошло? При переходе закрытой системы в открытую хаос родил симметрию! Да такую симметрию, что сам И. Кеплер не обошёл вниманием такую красоту [2]. При понижении температуры в системе запустился процесс бифуркации [3]. В системе возникло два агрегатных состояния: хаос – газ и порядок – снег.
2. Выйдем в тёплое море, куда-нибудь южнее Японии. Огромные зеркала воды, острова. Взошло солнце. Воздушный океан подвергся вмешательству извне – солнце нещадно палит. Какие-то участки поверхности, особенно неоднородные, разогреваются неравномерно: мели, рифы, острова, поверхность воды. Воздух, соприкасаясь с этими поверхностями, разогревается тоже неравномерно. Та воздушная среда, которая получила больше солнечной энергии, начинает раскручиваться. Раскрутка захватывает целые воздушные зоны. Наконец, масса воздуха срывается в закрутку. Запустился процесс бифуркации. В воздушном океане возникло два энергетических состояния: вихрь, который вобрал в себя избытки энергии Солнца, и огромное пространство относительно холодного воздуха, окружающего вихрь.
3. А вот неожиданный ракурс локализации энергии. Просто кипарис и кипарис Ван Гога. Посмотрите, какие вихри нарисовал Ван Гог, и сколько тревоги и энергетической ёмкости добавилось на полотне! Когда оказались совмещёнными на одном полотне два энергетических состояния: покой и вихри.
4. Рассмотрим хорошо знакомую нам в обиходе воду. В определённых температурных условиях резервуар воды можно рассматривать как закрытую систему. Это привычная для нас с вами вода, например, при температуре +20 °C. Молекула воды – Н2O. Как мы с вами уже знаем, можно резервуар воды сделать открытой системой, если начать менять температурный режим. В результате вмешательства извне вода становится открытой системой и начинает вести себя очень интересно: Н2O как функция температуры Т.
На температурной шкале возникает несколько замечательных точек (температурных зон), в которых запускается процесс бифуркации – вода разделяется на разные агрегатные состояния.
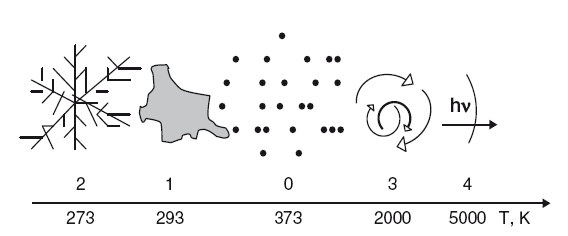
Рис. 18. Геометрическая форма упаковки Н2O как функция температуры Т
При повышении температуры за точкой 0 встречаем зону динамического равновесия 3, где молекулы Н2O начинают раскручиваться. Достаточно незначительных неоднородностей, как начинают возникать локальные вихри. В кручении вихрей принимает участие много молекул.
В точке 4 приток энергии столь велик, что внутри каждой молекулы возникают сложные отношения между атомами. Химические связи с трудом удерживают атомы водорода и кислорода в химическом соединении Н2O. Атомы начинают ходить – колебаться друг относительно друга, будто на пружинках. В этой температурной зоне возникает совершенно удивительное преобразование хаоса в порядок периодики: из молекул начинает рождаться электромагнитное излучение строго определённых частот.
При понижении температуры за точкой 0 запускается процесс бифуркации: в зоне 1 из пара появляется вода в известном нам жидком виде.
При переходе через температурную точку 2 запускается процесс бифуркации: из достаточно подвижной, пластичной воды с ближним порядком симметрии начинает выстраиваться кристаллическая структура с дальним порядком симметрии. Все атомы выстраиваются, как солдаты на плацу во время парада.
Позвольте ещё раз напомнить, что человек в основном состоит из воды.
1.2. Кросс-катализ
Получается, что для природы характерно:
✓ наличие точек бифуркации по определённым параметрам при переходе закрытой системы в открытую систему (мы рассмотрели только один параметр – температуру);
✓ запасать энергию в определённом диапазоне температур в виде вращательного движения.
Отметим, что для человеческого организма не чужд класс каталитических реакций – так называемый кросскатализ (перекрёстный катализ). Он играет существенную роль в метаболических (от греч. μεταβολή – перемена, превращение) функциях [4]. Приведём пример такой реакции, описанной в [1].
Идёт удивительная реакция, характерная для работающего биологического объекта. По параметру концентрации в определённой химической среде запускается процесс бифуркации, в результате которого в среде возникает устойчивое кольцо локализации энергии – вихрь.
При этом из вещества У получается вещество X, и одновременно из X получается У. Процесс устойчив. Такой реакцией, например, может быть описана взаимосвязь между нуклеиновыми кислотами и протеином: нуклеиновые кислоты являются носителями информации, необходимой для синтеза протеинов, а протеины в свою очередь синтезируют нуклеиновые кислоты.
Позвольте! Этот процесс напоминает те процессы, которые мы наблюдали в приведённых ранее (1.1. Примеры бифуркации в системах) примерах. Может быть, приведённый процесс кросс-катализа – весточка. Одна из многих весточек о том, что человека не следует вырывать из природы, как мы теперь говорим – из окружающей среды. Приятно сознавать, что человек органично вписан в природу и проявляет собой одну из её ипостасей.
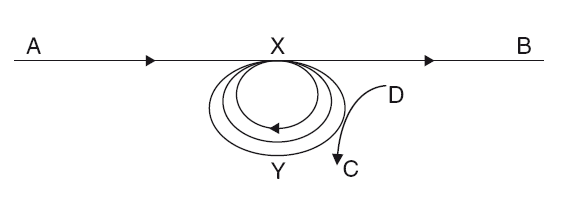
Рис. 19. Реакция перекрёстного катализа
В таком случае законы, которые учёные открыли, изучая неорганическую природу, распространяются и на человека. Можно сказать так: человек представляет собой закрытую систему огромного количества атомов и молекул. При переходе этой системы в открытую систему могут возникать процессы бифуркации, сопровождаемые различными формами локализации энергии, в том числе и в виде устойчивых колец-вихрей.
Назад: Введение
Дальше: Глава 2 Генетическая форма памяти

