Книга: Прямоходящие мыслители. Путь человека от обитания на деревьях до постижения миро устройства
Назад: Глава 10 Пределы человеческого опыта
Дальше: Глава 12 Квантовая революция
Глава 11
Царство незримого
Заработав себе докторскую степень, я получил место младшего научного сотрудника в Калтехе и взялся искать себе тему для дальнейших трудов, чтобы не вылететь из науки и не занять более доходную позицию официанта в факультетском клубе. Как-то раз после одного семинара я разговорился с физиком Ричардом Фейнманом о теории под названием струнная. Фейнман, которому в те поры перевалило за шестьдесят, среди своих коллег-физиков был, вероятно, самым почитаемым на свете. Ныне многие (хотя отнюдь не все) считают теорию струн главным кандидатом на единую теорию всех сил природы, святой грааль теоретической физики. Но в те времена о ней мало кто слышал, а из них, в свою очередь, ею мало кто увлекался – включая Фейнмана. Он как раз брюзжал по поводу теории струн, когда в разговор вмешался гость нашего факультета, прибывший из университета в Монреале: «Мне кажется, не стоит отвращать молодых людей от исследования новых теорий лишь потому, что они не приняты светилами физики», – сказал он Фейнману.
Отвергал ли Фейнман теорию струн, потому что она казалась ему слишком большим отрывом от его устоявшейся системы верований, и он не мог пересмотреть свои взгляды? Или он сделал бы те же выводы о недостатках этой теории, даже если б она не размежевывалась с предыдущими теориями столь категорически? Этого мы не знаем, но Фейнман ответил гостю, что он не отсоветовал мне работать над чем бы то ни было новым, а просто мне следует быть осторожным, иначе, если дело не выгорит, я впустую потрачу уйму времени. Гость возразил: «Ну, я со своей теорией возился двадцать лет», – и пустился объяснять ее, в изнурительнейших подробностях. Когда он договорил, Фейнман повернулся ко мне и заметил, прямо в присутствии человека, который только что с гордостью изложил свою теорию: «Именно это я и имел в виду под впустую потраченным временем».
Передний край научных исследований укрыт туманом, и любой деятельный ученый неизбежно приложит зряшные усилия, следуя неинтересным тупиковым путям. Но одна черта, отличающая успешного физика, – чутье (или удача) при выборе задач, которые окажутся одновременно и познавательными, и решаемыми.
Я сравнивал страсть физиков с пылом художников, но мне всегда казалось, что у художников перед физиками есть большое преимущество: в искусстве, сколько бы ваши коллеги и критики ни говорили, что ваша работа – фуфло, никто не сможет этого доказать. Но не в физике. В физике утешать может лишь то, что вам пришла в голову «красивая мысль», пусть она и оказалась ошибочной. И потому в физике, как и в любом поле новаторства, приходится блюсти непростое равновесие: выбирать задачи с осторожностью, но с ней не перебарщивать, иначе никогда не родится ничего нового. Именно поэтому так ценна в науке система пожизненных ставок – она обеспечивает безопасность падения, а это необходимо для поддержки творчества.
Если вглядеться в прошлое, может показаться, что Эйнштейнова увлекательная теория фотонов – световых квантов, – должна была немедленно подпитать уйму новых исследований юной квантовой теории. Но современникам Эйнштейна еще предстояло познакомиться со множеством доказательств существования фотона, хватало им и поводов для скептицизма, а работа над фотонной теорией требовала большого интеллектуального авантюризма и смелости.
Даже юные физики, обычно самые неудержимые, пусть речь идет о задаче, которая может не выгореть или, более того, вызвать насмешки, и чье мировоззрение все еще пластично, проходили мимо и темами своих докторских диссертаций и дальнейших трудов выбирали что угодно, только не Эйнштенову чокнутую фотонную теорию.
Без всякого развития прошло почти десять лет. Эйнштейну перевалило за тридцать, он стал довольно взрослым теоретиком-новатором и много времени посвящал другой революционной теме: расширению, или обобщению, своей специальной теории относительности, предъявленной в 1905 году, – чтобы она охватывала и силу тяготения. (Специальная теория относительности – модификация Ньютоновых законов движения, общая теория относительности заместила Ньютонов закон всемирного тяготения, однако потребовала от Эйнштейна скорректировать специальную теорию относительности.) Невнимание Эйнштейна к фотонной теории подтолкнуло Роберта Милликена написать: «Вопреки… с виду полному успеху Эйнштейнова уравнения [для фотоэлектрического эффекта], физическая теория [фотона], кою это уравнение и описывает, до того непригодна, что даже сам Эйнштейн, насколько я понимаю, за нее не держится».
Милликен заблуждался. Эйнштейн не отказался от фотона, однако, поскольку внимание ученого было занято другим, вполне понятно, почему Милликену так показалось. И все же ни фотон, ни квантовая теория, которую он породил, не умерли. Напротив, они вскоре станут звездами – благодаря Нильсу Бору (1885–1962), двадцати-с-чем-то-летнему молодому человеку, который ни укоренился в убеждениях, ни имел достаточно опыта, чтобы отказаться от риска потратить время и бросить вызов нашим представлениям о законах, правящих миром.
* * *
Когда Нильс Бор учился в школе, ему рассказывали, как греки придумали натурфилософию, и что уравнения Исаака Ньютона, описывавшие отклик физических тел на воздействие силы тяготения, – первый громадный шаг к пониманию устройства мира, поскольку благодаря им ученые могут производить количественные оценки движения падающих и движущихся по орбите тел. Бора учили и тому, что незадолго до его рождения Максвелл добавил к трудам Ньютона теорию, как предметы взаимодействуют с электрическими и магнитными полями и генерируют их, – и таким образом довел мировоззрение Ньютона до его вершины.
Физики во времена юности Бора, казалось, располагали теорией и сил, и движения, включавшей в себя все взаимодействия, какие есть в природе и известные на ту пору. Бор, однако, не ведал вот чего: на рубеже веков, когда сам он поступил в Университет Копенгагена и принялся за свою научную работу, почти через двести лет все более поразительных успехов мировоззрение Ньютона готово было того и гляди рухнуть.
Как мы уже убедились, ньютонианство оказалось под сомнением, поскольку новая теория Максвелла хоть поначалу и позволила расширить Ньютоновы законы движения на множество других явлений, позднее оказалось, что излучение абсолютно черного тела и фотоэлектрический эффект, например, не укладываются в предсказания Ньютоновой (классической) физики. Однако прорывы в развитии теории, осуществленные Эйнштейном и Планком, стали возможны лишь благодаря техническим нововведениям, позволившим экспериментаторам исследовать физические процессы с участием атома. И именно этот поворот событий вдохновил Бора, поскольку он питал большое почтение – и располагал изрядным даром – к экспериментальной работе.
Годы, посвященные Бором его диссертации, несомненно, увлекательны – особенно тем, кому интересна экспериментальная физика. В те годы технические новшества вроде вакуумированных стеклянных трубок со встроенным в них источником тока – предшественников электронно-лучевых трубок, сиречь экранов старых телевизоров, привели ко множеству важных открытий. Например: открытие Вильгельмом Рентгеном [Вильхельмом Рёнтгеном] лучей, названных его именем (1895); открытие Томсоном электрона (1897); осознание физиком новозеландского происхождения Эрнестом Резерфордом [Разерфордом], что атомы некоторых химических элементов вроде урана или тория испускают загадочное излучение (1899–1903). Резерфорд (1871–1937) описал даже не одного, а целых трех обитателей этого зверинца загадочных лучей – альфа-, бета– и гамма-излучение. По его рассуждению, эти три излучения – ошметки, образующиеся после того, как атомы одного элемента самопроизвольно распадаются и образуют атомы другого элемента.
Открытия Томсона и Резерфорда оказались особенно сродни откровению, поскольку описывали атом и его составляющие, кои, как выяснилось, при помощи законов Ньютона ни описать, ни даже вместить в систему классической физики не получается. И потому эти новые наблюдения, как впоследствии станет ясно, потребовали совершенно нового подхода к физике.
И все же, пусть и теоретические, и экспериментальные успехи того времени кружили голову, первоначальный отклик физического сообщества на бо́льшую часть этих успехов свелся к следующему: примем охолонин и сделаем вид, что ничего этого на самом деле не происходит. И потому отмахнулись не только от кванта Планка и фотона Эйнштейна, но и от этих революционных экспериментов.

Эрнест Резерфорд
До 1905 года считавшие атом метафизической чепухой относились к разговорам об электронах, предполагаемых составляющих атома, примерно так же серьезно, как атеист относится к дискуссиям о том, мужчина Бог или женщина. Удивительнее же вот что: тем, кто все-таки верил в существование атомов, электроны не понравились – потому что электрон считался «частью» атома, а атом, по определению, – штука неделимая. До того фантасмагорическим казался электрон Томсона, что один знаменитый физик сказал ему, что принял все это за «розыгрыш».
Так же и с предположением Резерфорда о том, что атом одного элемента может распасться до атома другого, – все решили, что оно исходит от человека, отрастившего себе длинную бороду и облачившегося в мантию алхимика. В 1941 году ученые узнали, как превратить ртуть в золото – прямо-таки мечта алхимика, – бомбардируя ртуть нейтронами в ядерном реакторе. Но в 1903-м коллегам Резерфорда принять смелые заявления о трансмутации не хватило авантюрности. (При этом, как ни странно, на возню со светящимися радиоактивными цацками, которые им выдал Резерфорд, им авантюрности достало, и они тем самым получили дозу облучения от процесса, который, как они считали, и не происходит вовсе.)
Шквал диковинных статей с результатами исследований и в теоретической, и в экспериментальной физике казался многим, вероятно, примерно тем же, чем нам ныне – обилие литературы по социопсихологии, в которых исследователи регулярно объявляют об открытиях вроде: «Люди, которые едят виноград, чаще попадают в аварии на дороге». Но на самом деле, хоть выводы физиков и выглядели несусветными, они оказались верны. И постепенно накопленные экспериментальные данные, подкрепленные теоретическими доводами Эйнштейна, вынудили физиков принять существование и атома, и его составных частей.
За работу, приведшую к открытию электрона, Томсон получил Нобелевскую премию по физике 1906 года, а Резерфорд – по химии, в 1908 году, за работы, благодаря которым стало ясно, что алхимики в мантиях все же кое-что смекали.
Вот какова была сцена физических исследований 1909 года, на которую взошел Нильс Бор. Он был на пять лет младше Эйнштейна, однако этот разрыв оказался достаточно велик, чтобы Бор попал в другое поколение – в то, которое выходило на поле физики, уже приняв и атом, и электрон, хотя на фотон это доверие все еще не распространялось.
Темой докторской диссертации Бор выбрал анализ и критику теоретических выкладок Томсона. Завершив работу, Бор успешно обратился за грантом, который позволил бы ему трудиться в Кембридже и получать отзывы великого ученого. Обсуждение идей – ключевое свойство науки, и потому обращение Бора к Томсону с критикой, конечно, не равносильно замечанию студента, адресованному Пикассо, дескать, у лиц на ваших картинах перебор углов, – но все же что-то близкое к тому. И Томсон, разумеется, не рвался одарять критика-выскочку вниманием. Бор пробыл рядом почти год, но Томсон так и не обсудил с ним его диссертацию – он ее даже не читал.
Невнимание Томсона оказалось тем самым несчастьем, что помогло счастью: маясь в Кембридже из-за провалившегося плана задействовать Томсона, Бор встретил Резерфорда, заехавшего с визитом. Резерфорд сам работал под началом Томсона в свои молодые годы, но ко времени встречи с Бором уже был ведущим физиком-экспериментатором и директором центра изучения радиации в Университете Манчестера. Резерфорду, в отличие от Томсона, соображения Бора понравились, и он пригласил его к себе в лабораторию на работу.
Резерфорд с Бором составляли странный тандем. Резерфорд – человек-гора, энергичный, широкий и высокий, с сильным лицом и до того раскатистым, громовым голосом, что насылал помехи на чувствительное оборудование. Бор – утонченный и гораздо более мягкий, и на вид, и по натуре, с вислыми щеками, тихим голосом и легким дефектом речи. Резерфорд говорил с густым новозеландским акцентом, Бор – на бедном датском английском. Резерфорд, когда ему перечили, выслушивал с интересом, после чего завершал разговор, не удостаивая собеседника отпором. Бор упивался интеллектуальными стычками и творчески мыслил, лишь когда мог постоянно обмениваться с кем-нибудь мнениями и спорить.
Работа в паре с Резерфордом стала для Бора счастливой передышкой: хотя Бор отправился в Манчестер, думая, что сможет проводить эксперименты с атомом, прибыв туда, он очертя голову набросился на теоретическую модель атома, основанную на Резерфордовых экспериментальных данных, с которой сам Резерфорд и возился. Именно благодаря теоретической работе, которую он проделал по «атому Резерфорда», Бор смог оживить дремавшую квантовую идею и завершить за Эйнштейна работу, посвященную фотону: это Бор поместил представление о фотоне на карту наших знаний – навсегда.
* * *
Когда Бор прибыл в Манчестер, Резерфорд занимался экспериментами, призванными изучить распределение заряда внутри атома. Он решил разобраться с этим вопросом, анализируя особенности воздействия заряженных частиц, если ими стрелять, как пулями, по атому. Он взял альфа-частицы, которые сам же и открыл; мы теперь знаем, что это просто положительно заряженные ядра гелия.
Резерфорд еще не составил свою модель атома, однако допускал, что атом довольно прилично описывается другой моделью – Томсоновой. Протон и атомное ядро еще пока не открыли, и в модели Томсона атом состоял из рассеянной жидкости положительного заряда, в которой плавало множество электронов, компенсирующих этот положительный заряд. Поскольку масса электронов очень мала, Резерфорд думал, что, подобно марблам на пути пушечного ядра, они в движении массивных альфа-частиц мало что изменят. А вот гораздо более тяжелую жидкость положительного заряда и то, как она распределена, имело смысл изучать.
Аппарат Резерфорда был прост. Луч альфа-частиц испускало радиоактивное вещество вроде радия, и этот луч направляли на тоненькую золотую фольгу. Позади фольги размещался маленький экран. Альфа-частицы проходили сквозь фольгу и ударялись в экран, от чего получались крошечные почти невидимые вспышки света. Сидя перед экраном с лупой можно, несколько напрягшись, засечь место вспышки и определить, насколько отклонилась альфа-частица при соударении с атомами фольги.
Хотя Резерфорд уже прославился на весь мир, его работа и рабочее пространство были далеки от шикарных. Лаборатория – сырой мрачный подвал, по полу и потолку проложены трубы. Потолок так низок, что цепляешься головой, а пол такой неровный, что можно было налететь на трубу в полу еще до того, как утихнет боль от удара головой. Самому Резерфорду для проведения замеров терпения не хватало, и как-то раз пару минут попытавшись половить вспышки, он выругался и бросил это дело. Его ассистент, немец Ганс Гейгер [Ханс Хайгер], напротив, был богом однообразной деятельности. Ирония истории: позднее он перечеркнет ценность этой своей добродетели, изобретя счетчик имени себя самого.
Резерфорд предполагал, что тяжелые, положительно заряженные альфа-частицы по большей части будут пролетать сквозь фольгу в зазорах между атомами золота слишком далеко от них, и потому искривление траектории будет незаметно. Однако некоторые, рассуждал он, все же пролетят сквозь один или даже несколько атомов и потому отклонятся – самую малость – от прямой, из-за отталкивания их рассеянного положительного заряда. Эксперимент в целом, несомненно, прояснит устройство атома, но скорее благодаря чистой удаче, нежели в соответствии с тем, как Резерфорд его замыслил.
Поначалу все данные, собранные Гейгером, соответствовали ожиданиям Резерфорда и совпадали с моделью Томсона. Но однажды в 1909 году Гейгер предложил «небольшое исследование» юному студенту Эрнесту Марсдену – просто чтоб пороху нюхнул. Резерфорд, сидя на занятиях по теории вероятностей на математическом факультете, подумал, что есть небольшая вероятность отклонения альфа-частиц на некий больший угол, нежели позволял зарегистрировать Резерфордов прибор. И он предложил Гейгеру поручить Марсдену провести модифицированный эксперимент и проверить эту возможность.
Марсден принялся искать частицы, отклонявшиеся в полете от прямой сильнее, чем до него искал Гейгер, – даже с таким большим углом отклонения, что, окажись это правдой, нарушило бы всё, что Резерфорд «знал» об устройстве атома. Задача, по мнению Резерфорда, почти точно равнялась колоссальной потере времени. Иными словами, отличная для студиозуса задачка.
Марсден прилежно следил, как альфа-частицы одна за другой пролетали сквозь фольгу в полном соответствии с ожиданиями, без всяких резких отклонений. И тут случилось нечто практически невообразимое: на экране, расположенном сильно в стороне, возникла вспышка. В конце концов из многих тысяч альфа-частиц, которые пронаблюдал Марсден, лишь горстка отклонилась под большими углами, а парочка отлетела назад, почти как бумеранг. Этого было достаточно.
Услыхав эти новости, Резерфорд сказал, что это «едва ли не самое невероятное событие в моей жизни. Это почти так же невероятно, как стрелять 15-дюймовыми снарядами по бумажной салфетке и получать их рикошетом назад». Такой отзыв объясняется вот чем: вся его математика говорила ему, что должно быть в золотой фольге нечто немыслимо крошечное и мощное, чтобы возникали, пусть и редко, столь сильные отклонения в траектории. Вот так Резерфорд не прояснил модель Томсона – он установил, что модель Томсона ошибочна.
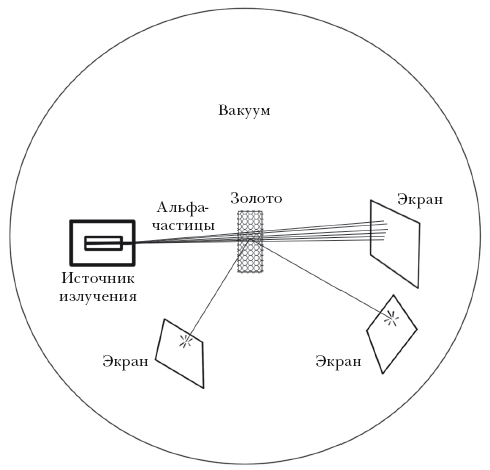
Эксперимент Резерфорда с золотой фольгой
Перед проведением эксперимента Марсденом весь этот проект казался несуразным – вроде той деятельности, от которой меня отговаривал Фейнман. Однако в течение века, последовавшего за этим экспериментом, его возносили как гениальный. И, разумеется, без него вряд ли возник бы «атом Бора», а это значит, что и непротиворечивая теория кванта возникла бы – если бы вообще возникла – на много лет позже. Что, в свою очередь, сильно повлияло бы на наш так называемый технический прогресс. Уж точно отсрочилась бы разработка атомной бомбы, а значит, ее не сбросили бы на Японию и тем спасли жизни многим-многим невинным японским гражданам, но, возможно, это стоило бы жизней многих-многих солдат, которые сгинули бы при вторжении союзников. Отложились бы многие другие изобретения – транзистор, например, а без него не началась бы компьютерная эра. Трудно в точности оценить все последствия, если бы тот единственный, с виду бессмысленный студенческий эксперимент не состоялся, но можно с уверенностью говорить, что мир сегодня выглядел бы несколько иначе. И вновь мы видим тонкую грань между странноватым чокнутым проектом и новаторской мыслью, которая меняет всё.
В дальнейшем Резерфорд курировал много других экспериментов, в которых Гейгер и Марсден пронаблюдали более миллиона вспышек. На собранных данных он составил свою теорию устройства атома, отличную от Томсоновой, но она все еще описывала электроны как обращающиеся по концентрическим орбитам тела, однако положительный заряд более не был рассеян, а наоборот – собран в крошечном центре атома. Гейгер с Марсденом, впрочем, вскоре каждый пошли своей дорогой. Во время Первой мировой войны они воевали на противоположных сторонах, а во Второй мировой применяли свои знания против друг друга: Марсден трудился над новой технологией радара, а Гейгер, поддерживая нацистов, участвовал в разработке немецкой атомной бомбы.
Атом Резерфорда – модель, которой нас учат в средней школе: электроны вращаются вокруг ядра, как планеты – вокруг Солнца. Как и многие научные представления, это, если свести его к повседневным похожим примерам вроде школьного, смотрится неприхотливо, однако подлинная гениальность этой модели – именно в «технических» затейливостях, утерянных при усушке и утруске, неизбежных при составлении простых схем. Интуитивная картинка – вещь полезная, однако любую мысль в физике делают жизненной математические следствия. И потому физик должен быть не просто мечтателем, но и техником.
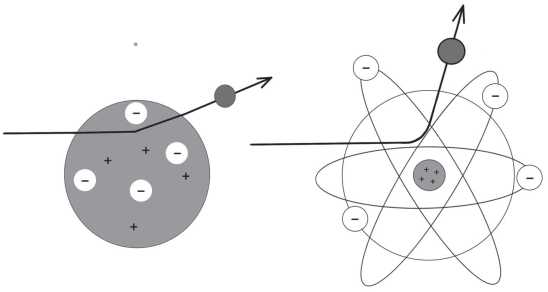
Предсказанное отклонение альфа-частиц: по Томсону (слева) и по Резерфорду (справа)
Резерфорду-мечтателю эксперимент подсказал, что львиная доля массы атома и весь его положительный заряд должны быть сосредоточены в центре его, в невероятно крошечном шарике заряженной материи, настолько плотной, что одна чашка ее будет весить в сто раз больше Эвереста. (То, что ни вы, ни я и близко не такие тяжелые, – подтверждение факта, что ядро есть малюсенькая точка в центре атома, который в основном – пустое пространство.) Позднее Резерфорд назовет эту центральную часть атома ядром.
Резерфорд-техник одолел сложные математические расчеты и обнаружил: если картина, которую он себе представляет, действительно верна, в экспериментах должно было получаться именно то, что наблюдала его команда. Большинство быстрых и тяжелых альфа-частиц пролетит сквозь золотую фольгу, мимо крохотных атомных центров, и в результате траектория их полета изменится лишь слегка. Меж тем некоторые, пролетающие вблизи ядер, столкнутся с сильным полем и претерпят значительное отклонение от прямого маршрута. Мощь этого силового поля – прямо-таки из научной фантастики, как для нас – силовые поля из фильмов. Но пусть мы не имеем возможности генерировать поля такой силы в макромире, они существуют внутри атома.
Важный нюанс открытия Резерфорда: положительный заряд ядра сосредоточен в его центре, а не распределен равномерно по объему. Его представление, будто электроны вращаются вокруг ядра подобно планетам вокруг Солнца, напротив, было совершенно ошибочным – и он это понимал.
Во-первых, аналогия с Солнечной системой не учитывает взаимодействия между планетами этой системы, – как не учитывает она и взаимодействия между разными электронами внутри атома. Эти взаимодействия совсем не одинаковы. Планеты, у которых солидная масса, но никакого общего электрического заряда, взаимодействуют гравитационно; электроны, у которых есть заряд, а масса мала, взаимодействуют электромагнитно. Сила тяготения чрезвычайно слаба, и потому притяжение планет друг к другу настолько мало, что для многих практических целей им можно пренебречь; электроны же воздействуют друг на друга мощнейшим электромагнитным отталкиванием, которое быстро нарушило бы аккуратненькие круговые орбиты.
Во-вторых – и это вопиющая нестыковка, – и планеты, и электроны, двигайся они по кругу, испускали бы волны энергии: планеты – гравитационной, электроны – электромагнитной. Опять-таки, сила тяготения очень слаба, и за миллиарды лет существования нашей Солнечной системы планеты потеряли ну, может, несколько процентов своей энергии. (На самом деле об этом эффекте и не догадывались, пока в 1916 году его не предсказала теория тяготения Эйнштейна.) Электронное же взаимодействие настолько сильно, что, согласно теории Максвелла, движущиеся по орбите электроны Резерфорда испустят всю свою энергию и плюхнутся на ядро примерно за одну стомиллионную секунды. Иными словами, если бы модель Резерфорда была верна, Вселенной в известном нам виде не существовало бы.
Вот она, расчетная оценка, какая запросто может потопить любую теорию: объявление о том, что Вселенной не существует. Так отчего же тогда относиться к такой теории серьезно?
Здесь возникает еще одна важная особенность развития науки: большинство теорий – не потрясающие новости планетарного масштаба, а, скорее, частные модели, нацеленные на описание конкретной ситуации. И потому, даже если в них есть недочеты, и сам автор модели знает, что не во всех случаях она работает, польза от нее все равно может быть.
В случае с атомом Резерфорда физики, занятые изучением атома, оценили, что эта модель дает точные прогнозы устройства ядра, и постановили, что дальнейшие эксперименты проявят, каких ключевых фактов не достает, чтобы разобраться, как во всё это встроены электроны и почему атом стабилен. Неочевидно было другое: атому требовалось не просто объяснение похитрее – нужно было революционное объяснение. Бледный и скромный Нильс Бор, однако, смотрел на все иначе. Юному Бору атом Резерфорда и его противоречия виделись стогом сена, в котором притаилась золотая иголка. И он был исполнен решимости ее найти.
* * *
Бор задался вопросом: если атом не испускает волн энергии, как того требует классическая теория (по крайней мере, согласно модели Резерфорда), может ли так быть, что атом не подчиняется классическим законам? Следуя этому рассуждению, Бор обратился к работе Эйнштейна о фотоэлектрическом эффекте. Он задумался, что может получиться, если включить атом в представление о кванте. То есть а что если атом, как световые кванты Эйнштейна, может иметь энергию лишь определенного значения? Эта мысль привела его к пересмотру модели Резерфорда и созданию того, что впоследствии станет называться Боровской моделью атома.
Бор применил этот подход к простейшему атому – атому водорода, состоящему из одного электрона, обращающегося вокруг ядра, которое представляет собой одинокий протон. Трудность этого предприятия1 можно проиллюстрировать фактом, что в те поры такое простое устройство атома водорода не было очевидным: из серии экспериментов, проведенных Томсоном, Бору пришлось сделать вывод, что у водорода всего один электрон.
Ньютонова физика дает расчетную оценку, что электрон может обращаться по орбите вокруг ядра (которое в случае водорода – просто протон) на любом расстоянии, если скорость и энергия его имеют подходящие значения, определяемые этим расстоянием. Чем меньше расстояние от электрона до протона, тем ниже должна быть энергия атома. Однако предположим, в духе Эйнштейна, что собираемся воспротивиться теории Ньютона, введя новый закон, повелевающий атому – по некой неведомой пока причине – иметь не какое попало значение энергии, а лишь взятое из дискретного набора возможностей. Поскольку радиус орбиты определяется энергией, это ограничение на допустимые значения энергии означает ограничение возможных значений радиусов орбит, по которым может перемещаться электрон. Сделав такое допущение, мы говорим, что энергия атома и радиусы электронных орбит квантуются.
Бор постановил: если свойства атома квантуются, электрон не может непрерывно съезжать по спирали к ядру и терять энергию, как велит классическая Ньютонова теория, – электрон может терять энергию только «порциями», переходя с одной разрешенной орбиты на другую. Боровская модель подразумевает, что электрон в атоме, возбуждающемся при поступлении энергии извне – например, от фотона, – переходит на одну из более удаленных от ядра и более энергетически насыщенных орбит. А всякий раз, когда происходит скачок на орбиту поближе к ядру, с энергией пониже, испускается квант света – фотон, а его частота соответствует разнице в энергиях между двумя орбитами.
Теперь предположим, что, опять-таки по доселе неведомой причине, есть самая близкая к ядру допустимая орбита – с самой низкой энергией, которую Бор назвал «основным уровнем». В этом случае, когда электрон достигает этого состояния, он более не может терять энергию и потому не падает на ядро, как предсказывала модель Резерфорда. Бор предположил, что похожая, но, быть может, более сложная схема применима и к другим химическим элементам, в чьих атомах много электронов: он считал квантование ключом к устойчивости Резерфордова атома, а следовательно – и всей материи во Вселенной.
Как работа Планка по излучению абсолютно черного тела, как объяснение Эйнштейном фотоэлектрического эффекта, так и соображения Бора не выводились из общей квантовой теории, а скорее были частными толкованиями одного определенного случая – например, устойчивости Резерфордова атома. Такова человеческая находчивость: невзирая на отсутствие «материнской» теории, модель Бора, как и модели Планка и Эйнштейна, по сути своей были верны.
Бор позднее скажет, что его размышления об атоме кристаллизовались лишь после случайного разговора с другом в феврале 1913 года. Тот друг напомнил ему о законах в спектроскопии – области науки, изучающей свет, испускаемый веществом в газовом состоянии при возбуждении, скажем, электрическим разрядом или сильным нагреванием. Было давно известно, что – по причинам, которые тогда еще предстояло понять, – каждое простое газообразное вещество испускает специфическую группу электромагнитных волн, характеризующихся конечным набором частот. Эти частоты именуются спектральными линиями и образуют своего рода отпечатки пальцев, по которым можно опознать, что это за химический элемент. Поговорив с другом, Бор понял, что с помощью своей модели атома может составить прогноз «отпечатков пальцев» водорода и так увязать свою теорию с проверкой опытными данными. Именно этот шаг в науке возносит мысль от многообещающего или «красивого» предположения к серьезной теории.
Доделав математику, Бор совершенно опешил: различия в энергии у «разрешенных» орбит воспроизводили в точности те самые частоты, чьи спектральные линии были получены в многочисленных экспериментах. Трудно вообразить себе воодушевление двадцатисемилетнего Бора в ту минуту: применив свою простенькую модель, он воспроизвел загадочные уравнения спектроскопистов и объяснил, откуда они берутся.
Бор опубликовал свой шедевр, посвященный атому, в июле 1913 года. Ради этой победы он изрядно потрудился. С лета 1912-го до того вдохновенного мига в феврале 1913-го он день и ночь возился со своими соображениями и выкладывался так, что даже прилежные его коллеги диву давались. Они даже думали, что он начнет падать от утомления. Одного примера будет достаточно: 1 августа 1912 года он собрался жениться – и женился, но медовый месяц в живописной Норвегии отменил и просидел в гостиничном номере в Кембридже, надиктовывая статью на тему своей работы новоиспеченной супруге.
Новая теория Бора, эдакий ералаш, очевидно была лишь началом. К примеру, он называл разрешенные орбиты «стационарными состояниями», поскольку электроны, когда ничего не излучают, должны, согласно классической теории, вести себя так, будто не движутся. При этом он часто говорил о «состоянии движения» электронов, изображая их обращающимися вокруг ядра по разрешенным орбитам, покуда они либо не слетали на орбиту с меньшей энергией, либо не поглощали внешнее излучение и не переходили в более высокоэнергетическое состояние. Я про это говорю, чтобы проиллюстрировать, что Бор применял противоречивые образы. Таков подход многих пионеров теоретической физики – в литературе предлагается не смешивать метафоры, а в физике, если мы знаем, что одна метафора не полностью подходит, вполне допустимо (осторожно) смешать ее с другой.
В данном случае Бор не выказывал пылкой приязни к классической «планетарной» модели атома, но с нее он начал и, чтобы создать новую теорию, применил уравнения классической физики, увязывавшие радиус и энергию электронных орбит, попутно добавив новые квантовые представления вроде принципа стационарных состояний, тем самым создав видоизмененную картину.
Боровскую модель поначалу встретили неоднозначно. В Университете Мюнхена влиятельный физик Арнольд Зоммерфельд (1868–1951) не только мгновенно распознал в этой работе веху науки, но и подключился к ней сам, взявшись исследовать ее связь с теорией относительности. Меж тем Эйнштейн сказал, что Бор сделал «одно из величайших открытий [в истории]». Но, вероятно, самое красноречивое свидетельство того, до чего потрясающей показалась модель Бора физикам его времени, – еще один комментарий Эйнштейна. Человек, которому хватило отваги выдвинуть предположение не только о существовании световых квантов, но и о взаимосвязи между пространством, временем и гравитацией, сказал, что ему приходило в голову нечто похожее на модель Бора, но из-за «чрезвычайной новизны» он не осмелился эти взгляды обнародовать.
Издание этой работы действительно потребовало смелости – об этом можно судить по другим откликам на работу Бора. К примеру, в Университете Гёттингена, ведущем немецком научном центре, все пришли к единодушному мнению, что «вся эта затея – ужасная чушь, граничащая с мошенничеством». Один гёттингенский ученый, эксперт в спектроскопии, изложил отношение Гёттингена письменно: «В высшей степени жаль, что литература оказывается засорена подобными жалкими данными, выдающими такое невежество». Один из зубров британской физики, лорд Рэлей [Рейли], сказал, что не смог заставить себя поверить, будто «Природа ведет себя вот так». Но все же прозорливо добавил, что «людям за семьдесят не стоит слишком поспешно выражать свое мнение о новых теориях». Другой ведущий британский ученый, Артур Эддингтон, тоже не пылал энтузиазмом, прежде отмахнувшись от квантовых представлений Планка и Эйнштейна как от «немецких измышлений».
Даже Резерфорд отозвался отрицательно. Ему уж точно не дорога была теоретическая физика. Но допекало его в работе Бора, которая, как ни крути, ревизовала его собственную модель атома, что его датский коллега не предложил никакого механизма, коим электрон осуществляет свои прыжки между объявленными энергетическими уровнями. К примеру, если электрон, перемещаясь на энергетический уровень, отвечающий меньшей орбите, «прыгает» на нее, а не непрерывно движется по спирали к ядру, каким именно маршрутом происходит этот «прыжок», и что его провоцирует?
Как позднее выяснится, возражения Резерфорда коснулись в точности сути. Не только такого механизма никогда не установят, но и квантовая теория дозреет до состояния теории природы, и из нее последует, что ответов у таких вопросов нет, а значит, им нет места в современной науке.
То, что в конце концов убедило мир физиков в правильности вид ения Бора, а значит – и ранних работ Планка и Эйнштейна, накопилось за десять лет, с 1913-го по 1923 год. Применяя свою теорию и воззрения других ученых к атомам разных химических элементов тяжелее водорода, Бор понял, что упорядочением элементов по атомному номеру, а не по массе атома, как это сделал Менделеев, можно устранить кое-какие ошибки в Периодической системе.
Атомная масса определяется числом протонов и нейтронов в ядре атома. Атомный номер же равен числу протонов, которое, поскольку атом в целом не имеет никакого заряда, равно числу электронов в этом атоме. Чем больше у атома протонов в ядре, тем больше там нейтронов, но их количества не обязательно совпадают, то есть порядок элементов по атомной массе и атомному номеру может разниться. Теория Бора показала, что атомный номер – подходящий параметр, на котором и следует выстраивать Периодическую таблицу, поскольку именно протоны и электроны, а не нейтроны, определяют химические свойства вещества. На этот вывод ушло более пятидесяти лет, но, благодаря Бору, наука наконец смогла объяснить, почему таинственная таблица Менделеева действенна.
С вызреванием квантовых представлений до общей структуры, которая заместит законы Ньютона, физики наконец смогли записать уравнения, из которых, в принципе, можно вывести поведение всех возможных атомов, хотя в большинстве случаев для этого требуется мощь суперкомпьютеров. Но чтобы проверить предположения Бора о важности атомного номера, никому ждать суперкомпьютеров не пришлось: в традиции Менделеева Бор предсказал свойства еще не открытого тогда элемента, и именно его Менделеев, основывая систему на атомной массе, определил ошибочно.
Элемент этот был открыт вскоре после прогноза Бора, в 1923 году, и назвали его гафнием, в честь Гафнии – так на латыни именуется родной город Бора, Копенгаген. С тех пор уж ни один физик (или химик) никогда больше не усомнится в истинности теории
Бора. Лет пятьдесят спустя имя Бора войдет в таблицу Менделеева – сто седьмой элемент получит название «борий». В тот же год бывший наставник, а иногда и критик датского физика будет удостоен той же чести: элемент 104 называется резерфордием.
Назад: Глава 10 Пределы человеческого опыта
Дальше: Глава 12 Квантовая революция

